我院参麦注射液上市后安全性再评价的研究*
2011-10-22柴世伟
刘 芳,马 瑛,柴世伟
(天津中医药大学第一附属医院,天津 300193)
天津市药品不良反应监测中心根据卫生部、国家食品药品监督管理局和国家中医药管理局联合下发的《关于进一步加强中药注射剂生产和临床使用管理通知》精神,组织开展中药注射剂的上市后再评价工作,正大青春宝药业有限公司的参麦注射液被选为第一批上市后安全性再评价的中药注射剂[1,2]。本院参与这一项研究工作,目的在于综合评价参麦注射液安全性,为完善参麦注射液推荐使用方案提供依据,并探索中药注射剂上市后安全性再评价的方法和模式[3,4]。
参麦注射液源于《症因脉治》的参麦饮,是由等量人参、麦冬提纯制备而成,具有益气固脱、养阴生津、生脉的功效。现代医学认为该药具有强心升压、扩张冠脉、增加心肌供血、抗心肌缺血、减少心肌耗氧量、去除氧自由基的作用,临床广泛用于心血管疾病、免疫功能低下、肌瘤及各种慢性疾病的辅助治疗。
1 资料与方法
1.1 研究资料 选取2009年6月—2010年1月本院入院患者中使用参麦注射液的患者为研究对象,过敏体质者除外,共观察371例。
1.2 研究方法
1.2.1 确定调查员和调查科室 药剂部主任为总的调查员,药剂部的6名临床药师为调查员。根据参麦注射液的临床适应证确定肿瘤科、血液科、ICU、急症病房、消化科为调查科室。
1.2.2 院内培训 总的调查员召集调查员和调查科室的医生和护士进行院内培训。培训内容包括:国家食品药品监督管理局发布的《关于开展中药注射剂安全性再评价工作的通知》和有关规范使用中药注射液、参麦注射液的药理作用和临床疗效、参麦注射液的不良反应文献报道和不良反应治疗措施等内容。
1.2.3 制定干预措施 临床药师为减少不良反应的发生,对参麦注射液的临床使用制定了干预措施:针对配液时间对护士进行培训,要求护士严格按照即配即用的配液原则,尽量缩短配液时间,配液后及时给患者使用;针对适应证、用量用法及联合用药3个因素对医生进行培训,要求医生从辨证论治的中医理论出发,严格按照说明书中提到的适应证、用量用法及联合用药的要求进行诊治。
1.2.4 填写筛选卡 对使用参麦注射液的患者填写由不良反应监测中心统一印制的《参麦注射液上市后再评价筛选卡》,筛选卡内容包括:患者基本情况[姓名、主诉、中(西)医诊断、舌脉象、过敏史等]、用药情况(用药时间、批号、联合用药情况等)、观察结果(是否出现不良反应、不良反应症状)。
1.2.5 观察时间 从用药开始至用药后15 d内为观察期。给药开始后的30 min内由临床药师进行密切观察,观察患者是否有不良反应发生,30 min后采用医护人员定期检查的方法进行观察,在观察期出院的患者进行电话随访,如发生不良反应及时进行处置。在观察期间同时接受病人主动反馈的情况。
1.2.6 判断标准 药品的用药剂量、适应证及给药间隔、给药速度及联合用药的合理性均以说明书为准,另外参考相关文献报道;患者的情况包括入院诊断、过敏史等以病历记录为准;不良反应判定标准:以说明书、《临床不良反应大典》及参考相关文献报道;疗效判断标准:以患者使用后症状的改变及实验室检查判断有效或无效。
1.2.7 不良反应处置 在观察期间未发生不良反应的患者,即观察结束。发生不良反应的病例纳入病例组,临床药师填写《参麦注射液上市后再评价监测表》(病例组),同时选择两个阴性对照为对照组,并填写《参麦注射液上市后再评价监测表》(对照组)。
1.2.7.1 病例组纳入标准 符合参麦注射液的适应证且使用参麦注射液的病人;出现与参麦注射液有关的不良反应或怀疑不良反应。
1.2.7.2 对照组纳入标准 与病例组同期(±7 d)使用参麦注射液的患者;未出现药品不良反应;与病例组原患疾病相同。
2 结果
2.1 用药剂量 参麦注射液的说明书规定用药剂量为20~100 ml,本院调查科室根据临床经验及患者的情况,分别给予20、40和60 ml 3种不同的剂量,具体情况及疗效见表1。
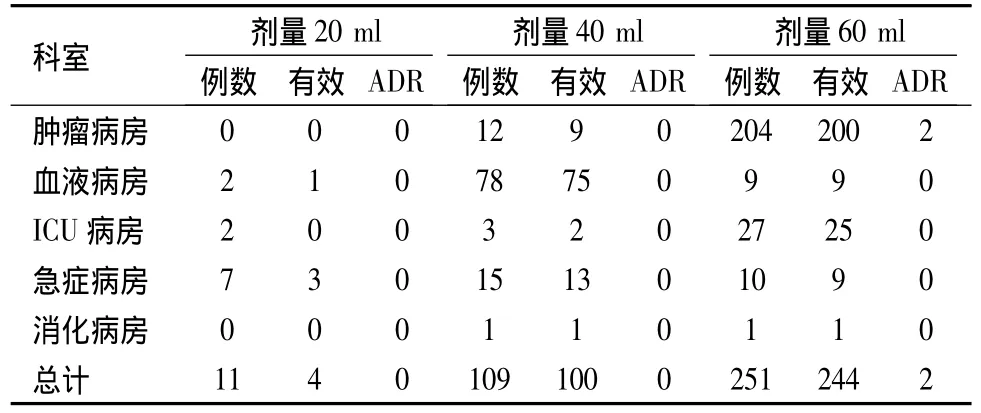
表1 参麦注射液用药剂量和分布情况
2.2 溶媒选择情况 参照参麦注射液说明书及文献报道,根据不同患者的情况使用了氯化钠注射液、5%葡萄糖注射液和果糖注射液作为溶媒,具体情况见表2。

表2 参麦注射液溶媒选择情况
2.3 参麦注射液发生不良反应的情况统计结果,见表3。

表3 应用参麦注射液后不良反应发生情况
3 讨论
3.1 本研究的重要性 中药注射剂是我国独创的中药新剂型,是从传统中药脱胎换骨演变出的新制剂,具有开拓国际市场的潜在优势。但随着中药注射剂在临床广泛应用,其不良反应事件不断出现,如“鱼腥草注射液”“完达山刺五加注射液”等事件,导致人们对中药注射剂的安全性产生质疑。为此,2009年1月,国家食品药品监督管理局发布了《关于开展中药注射剂安全性再评价工作的通知》,明确要求加强对中药注射剂安全性再评价的研究,以便进一步提高中药注射剂的安全性和质量可控性,确保临床用药的安全有效,并为医药行政管理部门制定政策提供依据,提高我国临床药品治疗水平。
3.2 参麦注射液的剂量 参麦注射液的常用剂量有20、40和60 ml,从本次研究纳入的病例看,随着剂量的增加患者的有效率增加,但不良反应也随着发生。
3.3 参麦注射液溶媒选择 参麦注射液药品质量标准pH规定为5.0~6.5,稀释时应选择与其pH值相近的溶媒,其成分和微粒才不会发生明显变化,保证临床用药的安全性。说明书规定使用5%葡萄糖注射液作为溶媒,糖尿病患者可选择氯化钠注射液。而对于糖和盐都限制的特殊患者(糖尿病合并高血压)有文献报道可选择果糖注射液作为稀释液。因果糖注射液pH值为4.59,与参麦注射液配伍后pH值为5.26,并可增加其澄明度[5],但2例不良反应使用的溶媒都为果糖。
3.4 患者个体、用药剂量和溶媒对不良反应发生率的影响 在此次研究中,共观察371例应用参麦注射液患者,发生不良反应2例,不良反应发生率只有0.54%。观察发现不良反应发生率与患者基础疾病、年龄、性别无相关联;溶媒和剂量对不良反应发生率也无影响。从目前纳入的研究病例发现,参麦注射液不良反应的发生主要与患者的个体差异有关。
由于时间的原因,本研究纳入的病例有限,可能对本研究的结果有影响。
1 周海燕,史新元,乔延江.关于提升中药注射剂安全性的几点思考.首都医药,2009,10:21
2 周超凡.关于中药注射剂安全性及再评价的探讨.药物不良反应杂志,2009,11(2):103
3 李静,郑新元,杨林娜.临床医师在中药安全性评价中的作用.中国药事,2009,23(5):421
4 屈建.中药注射剂安全性的再评价.中国执业药师,2009,6(5):3
5 余黎,朱荃,丰海能.果糖注射液与14种中药注射剂配伍的稳定性考察.中国中药杂志,2005,30(22):1778
