烟酸对滑子菇液体菌种菌丝体得率及胞外多糖的影响
2011-10-20田艳春王秀艳
田艳春,王秀艳
(赤峰学院 生命科学系,内蒙古 赤峰 024000)
烟酸对滑子菇液体菌种菌丝体得率及胞外多糖的影响
田艳春,王秀艳
(赤峰学院 生命科学系,内蒙古 赤峰 024000)
以不同浓度的烟酸作为刺激因子,对滑子菇液体培养后的菌丝体及胞外多糖得率进行研究,实验证明在液体培养基中加入不同浓度的烟酸均可刺激滑子菇菌丝体的生长及其他生物量的得率,当加入烟酸浓度为0.8ppm时,胞外多糖的得率、菌丝体的得率都为最佳,这就为滑子菇的工业化生产提供了较好的理论依据.
滑子菇;烟酸;菌丝体得率;胞外多糖得率
滑子菇隶属于真菌门、担子菌纲、伞菌目、丝膜菌科、鳞伞属.原产日本,因它的表面附有一层粘液,食用时滑润可口而得名.滑子菇不仅味道鲜美,富含有益于人体健康的蛋白质、氨基酸及糖类、矿物元素、维生素等营养保健物质,而且附着在滑菇菌伞表面的粘性物质是一种核酸,对保持人体的精力和脑力大有益处,并且还有抑制肿瘤的作用.据有关专家试验,其提取物对小白鼠s~180和艾氏腹水癌抑制率均为70%.
烟酸也称作维生素B3,或维生素PP,属于维生素B族.烟酸是人体必需的13种维生素之一,是一种水溶性维生素,属于维生素B族.烟酸在人体内转化为烟酰胺,烟酰胺是辅酶Ⅰ和辅酶Ⅱ的组成部分,参与体内脂质代谢,组织呼吸的氧化过程和糖类无氧分解的过程;另外烟酸还可以促进胰岛素的反应,使人远离糖尿病.缺乏烟酸主要有以下几种表现:前驱症状,体重减轻,疲劳乏力,记忆力差、失眠等,如不及时治疗会出现皮炎、腹泻和疾呆现象;皮肤症状,典型症状常风在肢体暴路部位,如手背、腕、前臂、面部、颈部、足背、踝部出现对称性皮炎;消化系统症状,初期很少出现,至皮肤和消化系统症状明显时出现,经症患者可有全身乏力、烦躁、抑郁、健忘及失眠等.重症则有狂躁、幻听、神志不清、木僵、甚至痴呆.
本实验研究了不同浓度烟酸对滑子菇液体菌种菌丝体干重、胞外多糖得率的影响,以期为生产合理添加有关营养成分,保证高产稳定提供参考.
1 实验流程
滑子菇母种扩大培养——→液体培养——→生长因子实验——→菌丝体得率和胞外多糖测定
2 材料与方法
2.1 滑子菇母种的扩大培养
2.1.1 实验材料
(1)实验菌种:
江苏省天达食用菌研究所提供
PDA培养基:马铃薯(去皮)200g、葡萄糖 20g、琼脂 20g、水1000mL.
2.1.2 实验方法
2.1.2.1 培养基的制作
将马铃薯去皮,挖掉芽眼,称200g切成薄片,加入1000mL蒸馏水.在电炉上煮沸15min,并不断搅拌,直至马铃薯煮至酥而不烂的程度,用4至6层纱布过滤,将滤液继续加热,同时加入琼脂20g,葡萄糖20g,煮沸,使药品全部溶解.
制备好后的PDA培养基趁热用漏斗分装于18mm×18mm或20mm×20mm的干燥试管中,装入量为试管高度的1/5,切勿使培养基黏附于试管口壁,如有黏附则用干净的纱布擦去.分装好后要使试管竖直放置,不能倾斜.塞上棉塞,棉塞在管内外长度约2:1,其作用是保证透气性,防止杂菌感染.
2.1.2.2 培养基灭菌
在分装好的试管棉塞外部包一层牛皮纸或两层报纸,以免灭菌时水蒸气浸湿棉塞.将捆扎好的试管培养基放入全自动立体式高压蒸汽灭菌锅,1.47×105Pa压力下灭菌30min.然后在灭菌完毕自然冷却至60℃左右时制备成斜面,斜面长度为试管长度的3/4为宜,待培养基冷却凝固后,随机抽取2-3支放入30±1℃恒温培养箱中培养3d,如培养基表面光滑无杂菌污染,可进行下步实验或备用.
2018年发展对象住建局办公室副主任王芳每次驿站活动结束后,都会写下心灵感悟。她在纪事本上写道:“我要珍惜难得机会,在驿站不断锤炼自己、让自己慢慢成长。”
2.1.2.3 滑子菇母种转管扩大培养
转管扩大培养工作在紫外灯杀菌环境的超净工作台中进行.接种前,将斜面培养基,接种工具,滑子菇母种,酒精灯,75%酒精棉等放入超净工作台,封闭进行紫外灯照射消毒30min,然后关闭紫外灯,打开吹风,进行扩繁.
首先将洗干净的双手伸入超净工作台中,用酒精棉球擦拭双手和菌种试管外壁,点燃酒精灯,灼烧接种铲.然后,左手拿斜面试管和菌种管,用右手小拇指和手掌夹住试管的棉塞拔出,将灼烧的接种铲在火焰上方慢慢伸入母种试管中,待温度不能灼伤菌种时,铲出绿豆大小的菌种块接入斜面试管的中央,保持菌丝朝上并轻压一下,移出接种铲(接种铲在伸入和移出试管过程中不能碰触试管壁),灼烧试管口和棉塞,塞好棉塞.即完成一支试管的接种,重复上述操作,接完后放入24±1℃恒温培养箱中生长.菌丝生长7—8d左右基本满管,挑选生长健壮、洁白、浓密且均匀的二级母种用于液体菌种的生产.
2.2 滑子菇液体菌种的培养
2.2.1 液体菌种培养试验流程图
初级液体培养基的制备——→菌种块的接入及静置培养——→摇床培养——→次级液体培养基的制备——→生长因子的添加——→菌种液的转接——→摇床培养——→菌丝体干重的测定和胞外多糖的测定
2.2.2 实验材料
液体基础培养基配方:玉米粉5%,蔗糖1%,硫酸镁0.3%,磷酸二氢钾0.15%,维生素B1微量.
2.2.3 实验菌种
母种以PDA培养基为承载的滑子菇二级母种.
2.2.4 实验方法
2.2.4.1 初级液体培养实验
首先按配方在70℃恒温水浴锅里乳化玉米粉,过滤后取其上清液分装到250ml锥形瓶内,每瓶100ml,然后每瓶加入硫酸镁0.3g、磷酸二氢钾0.15g、维生素B15mg、蔗糖1g、玻璃珠10粒、最后用8层纱布封口,用报纸包好后与接种铲、镊子、小托盘一起放入灭菌锅内灭菌30min.
将灭好菌的培养基连同扩大培养的菌种一同放入超净工作台中紫外灯灭菌30min.打开吹风无菌操作,向每一锥形瓶中接入一块1cm2大小的斜面菌种,接完后置于恒温箱中24±1℃静置培养36h,待菌丝延伸至液体培养基中,转入恒温摇床培养,条件为24±1℃,150r/min,摇床培养可以使菌丝体的菌龄一致,菌丝体保持正常的呼吸,均匀的生长.培养6—7d,当多数瓶内产生绒毛状分枝的菌丝球,培养液澄清并呈金黄色,散发淡淡菇香时,关闭摇床.
2.2.4.2 生长因子实验
次级液体培养基的配方:马铃薯20%,蔗糖1%,磷酸二氢钾0.15%,硫酸镁0.3%.
次级液体培养基的制备:制备20%马铃薯汁(方法同PDA培养基的制备)2800mL,然后加入蔗糖28g,磷酸二氢钾8.4g,硫酸镁4.2g,分装在28个锥形瓶内,每瓶均加入120mL.

表1 生长因子的添加
依次编号,分别加入7个不同浓度的烟酸作为刺激因子(每个浓度做4瓶,以保证实验的准确性),1号作为对照不加烟酸.向每一锥形瓶加入10颗玻璃珠,用八层纱布封口,外部再包扎一层牛皮纸或两层报纸放入自动高压蒸汽灭菌锅1.47×105Pa压力下灭菌30min.灭菌后,压强降到0,温度降到30℃左右取出,打开吹风无菌操作,向每个锥形瓶中接入生长良好的液体菌种的培养液10mL(含菌丝球,并尽量使其菌丝球大小和分布较为均匀),以此来保证每个浓度的烟酸所刺激的菌丝处于相同的起点,接完后置于恒温箱中24±1℃静置培养36h,转入恒温摇床培养,条件为24±1℃,150r/min,培养7d,当多数瓶内产生绒毛状分枝的菌丝球,培养液澄清并呈棕黄色,散发淡淡菇香时,关闭摇床.
考察指标:菌丝生长量(干重),胞外多糖含量.
考察因素:不同浓度的烟酸.
考察方法:单因子实验法
2.3 测定方法
2.3.1 菌丝干重的测定
将摇床培养的接入不同浓度的烟酸的菌丝体在超净工作台中过滤.滤液放入4℃冰箱中保存备用,菌丝体放入60℃烘干箱内烘干至恒重,以菌丝体干重(mg/mL)计算菌丝体得率,如表2所示.
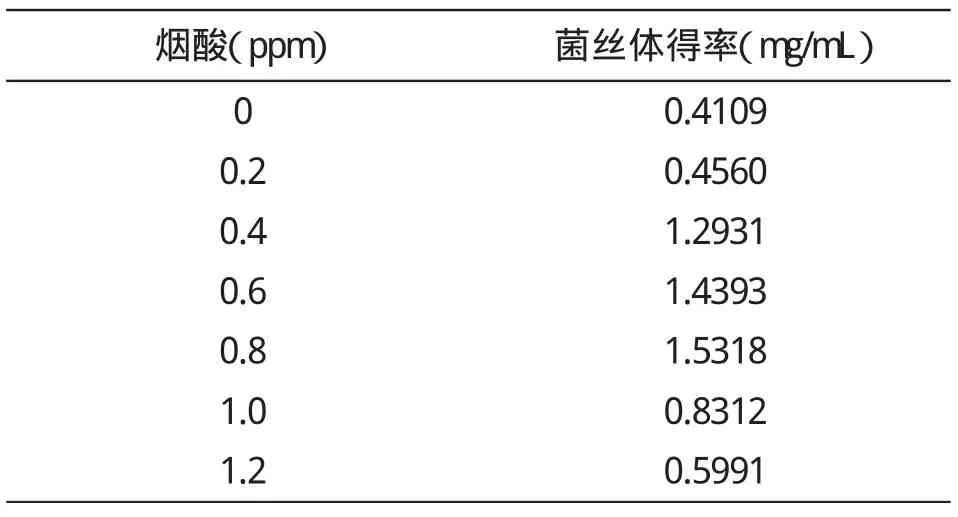
表2 不同烟酸浓度下菌丝体得率
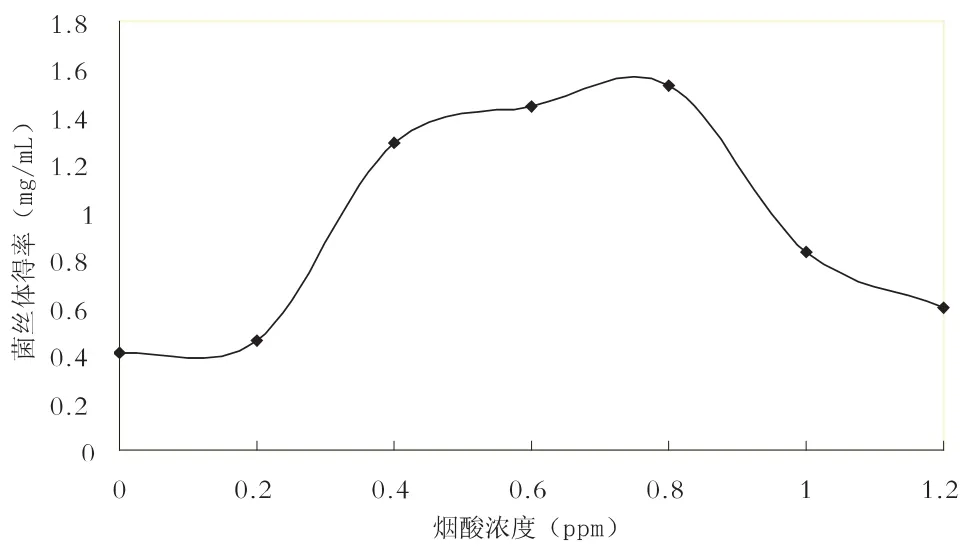
图1 不同烟酸浓度下菌丝体得率
2.3.2 胞外多糖的测定(苯酚-硫酸法)
2.3.2.1 苯酚-硫酸法测胞外多糖的原理
苯酚-硫酸试剂可与游离的寡糖或多糖中的己糖醛酸(或甲苯衍生物)起显色反应,呈橙黄色,且颜色稳定,在波长490nm处和一定的浓度范围内,其吸光度与多糖浓度呈线性关系,从而可以利用分光光度计测定样品吸光度,并利用标准曲线定量测定样品的多糖含量.
2.3.2.2 标准曲线绘制
准确称取干燥葡萄糖0.1g,用去离子水准确定容至100mL,得到1mg/mL葡萄糖溶液,摇匀后备用.准确称取苯酚9g,去离子水准确定容至60mL,即得到15%的苯酚溶液,棕色瓶中避光备用.取10支试管,第一支为空白对照试管,其余编号2-10,按表3方法操作:
按表3方法加入药品后震荡,摇匀,于25℃恒温水浴箱中保温20min,然后以1号作为空白对照,在490波长处测定吸光度.以葡萄糖浓度x为横坐标(ug/mL),吸光度y为纵坐标,绘制标准曲线如图2.

表3 绘制标准曲线所加药品列表

图2 葡萄糖标准曲线
图2为490nm处测定的葡萄糖标准曲线图,由图可知,其吸光度与葡萄糖浓度呈线性关系,方程表达式为y=0.0071x-0.132,将样品通过苯酚-硫酸法测出光吸收值,再根据标准曲线图求出样品中糖浓度.
2.3.2.3 样品多糖含量的测定
将过滤后保存的滤液从冰箱中取出,分别取各溶液0.05mL稀释500倍,吸取2mL稀释后的样品按上述步骤操作,测出其在490nm波长下的吸光值,再通过标准曲线计算出样品的多糖含量(mg/mL),制作表格4并绘制成图3.

表4 不同烟酸浓度下滑子菇胞外多糖得率
图3 不同烟酸浓度下滑子菇胞外多糖得率
3 结果分析
3.1 培养基灭菌效果的检测
灭菌后的斜面培养基取任意3—5支放入30±1℃恒温培养箱中培养3天,无任何生命生长迹象,可以确定所设置的灭菌条件达到无菌操作要求,培养基无杂菌污染.可用于下一步试验.
3.2 母种扩大繁殖菌丝体生长现象
接入PDA斜面培养基的滑子菇菌块48小时开始定植,7天左右菌丝满管,其日平均生长速度为1.42cm/d,菌丝洁白、浓密、粗壮、气生菌丝少、有菇香、为优良菌种,适合用于液体培养.
4 小结与讨论
4.1 在液体培养基中加入不同浓度的烟酸时对滑子菇菌丝体生长均有不同程度的影响.
由图1可知:当烟酸浓度在0-0.8ppm时,滑子菇菌丝体得率与其成正相关;当烟酸浓度为0.8ppm菌丝体率得率达到最高峰;当烟酸浓度为0.8-1.2ppm时,菌丝体得率与其成负相关.由此证明0.8ppm时是促进滑子菇菌丝体生长的最适烟酸浓度.
4.2 在液体培养基中加入不同浓度的烟酸时对滑子菇胞外多糖均有不同程度的影响.
由图3可知:烟酸浓度在0-0.8ppm时,滑子菇胞外多糖得率与其成正相关;烟酸浓度为0.8ppm时,胞外多糖得率达到最高峰;烟酸浓度在0.8-1.0ppm时,胞外多糖得率随烟酸浓度的增大而成负相关,但仍然促进胞外多糖的积累;烟酸浓度为1.2ppm时,抑制胞外多糖的积累.由此证明0.8ppm时是促进滑子菇胞外多糖积累的最适烟酸浓度.
通过本实验可得出,在液体培养基中加入不同浓度的烟酸可刺激滑子菇菌丝体的生长及其他生物量得率,当加入烟酸浓度为0.8ppm时,胞外多糖得率、菌丝体的得率都为最佳,这就为滑子菇的工业化生产提供了较好的参考价值.
〔1〕王桂芹,王秀艳.食用菌栽培[M].呼和浩特:内蒙古科学教育出版社,2001.
〔2〕林耀辉.灵芝GL8801液体发酵胞外多糖的提取和结构研究[J].福州大学学报,1997(1).
〔3〕宁慧清.苯酚硫酸法测定灵芝多糖的研究[J].太原师范学院学报(自然科学版),2006(1):105—107.
〔4〕刘伊强,吕凤华,石桂春.滑菇菌丝深层培养研究.食用菌,1990(5).
〔5〕余杰,崔鹏举,陈美珍,谢琼霞.鸡腿菇多糖的研究进展[J].安徽农学通报,2007(20).
S646.1
A
1673-260X(2011)12-0180-03
