含苯聚羟基脂肪酸酯的生物合成及其分子结构表征
2011-10-18黄锦标尚龙安
黄锦标,尚龙安
(1浙江大学宁波理工学院,浙江 宁波 315100;2浙江大学化学工程与生物工程学系,浙江 杭州 310027)
研究开发
含苯聚羟基脂肪酸酯的生物合成及其分子结构表征
黄锦标1,2,尚龙安1
(1浙江大学宁波理工学院,浙江 宁波 315100;2浙江大学化学工程与生物工程学系,浙江 杭州 310027)
聚羟基脂肪酸酯(PHA)具有可生物降解性和生物相容性,是潜在的医学材料。对聚羟基脂肪酸酯进行改性,可提高其应用范围.采用以苯戊酸和蔗糖为混合碳源培养基培养PseudomonasputidaKT2442,对其细胞内合成的聚羟基脂肪酸酯进行生物改性,并利用核磁共振、红外色谱和气相色谱分析方法表征了改性的PHA分子结构。结果表明合成的聚羟基脂肪酸酯为含有3-羟基苯戊酸单体的中长链聚羟基脂肪酸酯(PHPhA),该单体在PHA链中含量为1.04%,为进一步的研究打下基础。
聚羟基脂肪酸酯;生物改性;恶臭假单胞菌;混合碳源
聚羟基脂肪酸酯(PHA,其结构式如图 1)是细菌在营养不平衡下如氮元素限制或碳源充足的培养条件下在细胞内积累的一类作为碳源和能量储备的聚酯[1]。PHA因其具有可生物降性和生物相容性特点,并且通过改变 PHA中的单体可改变其热机械性能[2-4],因此近年来受到越来也多的关注。

图1 PHA分子结构通式(R1,R2为烷基,n=1~4)
PHA虽具有良好的应用前景,传统的PHA产品在性能上还存在某些缺陷,应用范围不广。如PHB在常温下的力学和耐溶剂性能很差;熔融状态下不稳定,容易分解,加工温度范围很窄。通过生物改性可在 PHA链中整合特定功能基团从而可以改善PHA的热机械性能并且可拓宽其应用范围。Shi等[5]利用Alcaligines eutrophus菌株,以 4-羟基丁酸和相对分子质量为 200的聚乙二醇(PEG-200)为混合碳源,首次在生物细胞内合成了端基为羟基的 PHA-PEG二元嵌段共聚物。Devang等[6]在发酵底物中加入乙二醇和 1,2-丙二醇,同样得到二元嵌段共聚物,TGA分析表明产物的热稳定性有较大的提高。Ward等[7]利用一系列含苯环的脂肪酸为碳源来合成PHA,当以苯戊酸为碳源时,Pseudomonas putidaCA-3合成的PHA中最高可含有98% 3-羟基苯戊酸单体,聚合物的玻璃化温度和熔点温度为 13.2 ℃和 51.5℃。以苯己酸为碳源时,得到的PHA中含有83%的 3-羟基苯己酸单体,其玻璃化温度和熔点温度为3.9 ℃和52.1 ℃。
含苯环基团的聚羟基脂肪酸酯(PHPhA)除了具有 PHA共有的生物相容性和生物可降解性等特点外,PHPhA能在体内缓慢降解,可作为药物载体起到药物缓释作用[8]。PHPhA在降解的过程中会缓慢释放诸如苯乙酸和苯丁酸这样的中间体,这些物质已被证明有抗肿瘤、止痛及化学防癌作用[9-11],因此具有潜在的医用前景。
本文利用以蔗糖和苯戊酸为混合碳源的发酵培养基来培养Pseudomonas putidaKT2442,通过在PHA聚合链上引进芳香基团对PHA进行生物改性,并利用红外色谱、核磁共振、气相色谱等分析手段对改性PHA进行分子结构表征。
1 实验部分
1.1 实验菌种及试剂
Pseudomonas putidaKT2442,本实验室保存。苯戊酸,Sigma公司。气相标准试剂:PHBV、甲基葵酸、甲基月桂酸、己酸,Sigma公司。其它试剂均为市售分析纯。
1.2 发酵培养基
蔗糖 15 g/L,KH2PO43 g/L,(NH4)2SO41 g/L,MgSO4·7H2O 1.2 g/L,柠檬酸 5 g/L,苯戊酸 0.5 g/L,pH值调至6.9~7.2。
1.3 分析仪器
傅里叶红外光谱仪 Tensor 27、核磁共振仪,Bruker公司;GC2010 plus气相色谱仪,日本岛津;UV-1800紫外分光光度计,上海美谱达仪器有限公司。
1.4 摇瓶发酵方法
菌种经LB培养基3次以上活化后,转接至500 mL装液量为200 mL的三角瓶中,在30 ℃,200 r/min的摇床中培养48~50 h,收集细胞并纯化。
1.5 分离纯化方法
发酵液在6000 r/min、10 min的条件下离心,得到的湿细胞用蒸馏水洗2~3次并离心,冻干。取10~20 g冻干细胞,以15 mL/g的比例与氯仿混合→放置恒温振荡器24 h→抽滤→恒温可调加热器上蒸发氯仿→待蒸发到15 mL,倒入10倍体积冰甲醇→对混合液离心 5 min→倒去上清液,沉淀再用少量氯仿溶解→倒入冰甲醇,离心,沉淀用少量氯仿溶解,重复 4~5次,可得到纯度 92%以上的发酵产物。
1.6 分析方法
紫外分光光度法:称取0.1 g干细胞于硝化管中,加入5 mL的浓硫酸,在85 ℃的水浴中反应1 h,冷却至室温,用去离子水稀释,在波长为208 nm条件下测其吸光度值,根据标准曲线换算成样品的浓度。红外吸收光谱采用KBr压片涂膜法。核磁共振光谱分析:溶剂CDCl3,内标TMS,基团的化学位移通过Shoolery公式[12]来确定。气相分析的样品处理:取0.1 g干细胞放入旋塞试管中,加入2 mL 酸化甲醇(含3% H2SO4,体积比)和2 mL氯仿,在100 ℃水浴条件下反应4 h,冷却至室温后,加入1 mL的去离子水,在漩涡混合器上震荡5 min,静置分层后,取下层进行GC分析。
气相分析条件:采用Restek公司RTX-1色谱柱(30 m×0.25 mm ID,填料为粒径0.25 μm的100%二甲基聚硅氧烷);氮气为载气;进样量1 μL;气化温度230 ℃;氢火焰检测池温度280 ℃。柱温:初始80 ℃保持2 min,再以10 ℃/min 的加热速率升温至180 ℃,保持2 min。
2 结果与讨论
2.1 不同苯戊酸浓度摇瓶发酵结果分析
图2 为在发酵培养基中分别加入浓度为0、0.2 g/L、0.5 g/L、1.0 g/L、1.5 g/L、2.0 g/L苯戊酸的摇瓶发酵结果。由图3可以知道,培养基中没有苯戊酸时, PHA在培养基的浓度最高,为0.658 g/L。随着培养基中的苯戊酸浓度的升高,所得 PHA的浓度逐次减少。当培养基中的苯戊酸浓度为 2 g/L时,PHA在培养基中的浓度仅为0.085 g/L,细胞浓度为0.21 g/L。由发酵结果来看,培养基中苯戊酸的含量对细胞生长和细胞内 PHA的积累有一定的影响。紫外分光法只能测定细胞内总PHA的含量,为确定苯戊酸是否对细胞合成的 PHA的结构有影响,须进一步对发酵产物进行结构分析。
2.2 发酵产物的结构分析
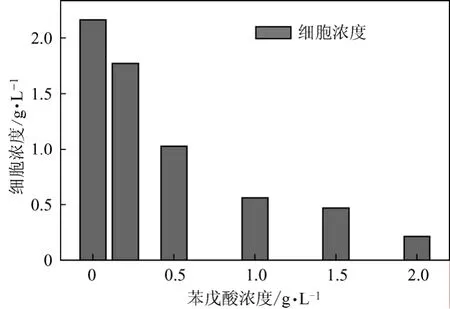
图2 苯戊酸浓度与细胞生长关系

图3 苯戊酸浓度与细胞内PHA含量关系
2.2.1 发酵产物红外光谱分析
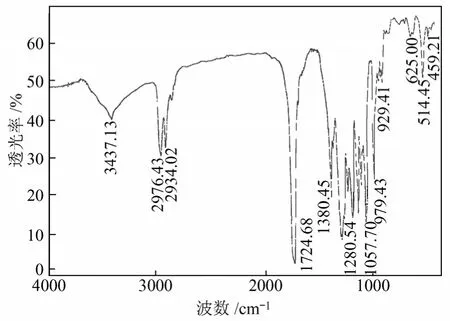
图4 单一碳源的发酵产物红外色谱图

图5 混合碳源的发酵产物红外光谱图
图4为以蔗糖为单一碳源的发酵产物红外色谱图,图5为以苯戊酸和蔗糖为混合碳源的发酵产物红外色谱图。由图可知,以蔗糖和混合碳源培养的到得发酵产物在1220~1760 cm-1处有吸收峰,表示发酵产物为内酯聚合物。对比图4和图5可知,以混合碳源发酵得到的产物在1467 cm-1处有吸收峰,此处为苯环内双键特征峰,所以Pseudomonas putidaKT2442以混合碳源为培养基的发酵产物为含有苯环的聚脂肪酸酯(PHPhA)。
2.2.2 发酵产物的核磁共振分析
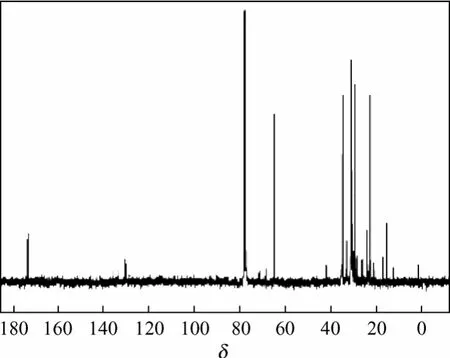
图6 发酵产物的100 MHz13C核磁图谱
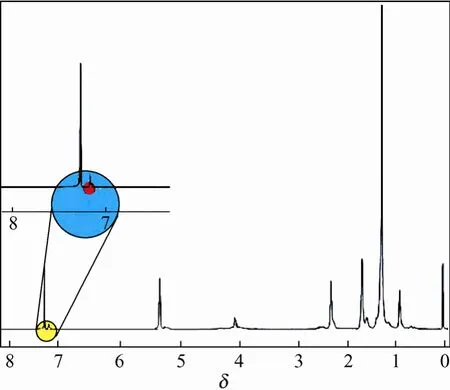
图7 发酵产物的400 MHz1H核磁图谱

表1 发酵产物各个碳的化学位移
图6和图7分别为纯度为92%发酵产物样品的核磁共振碳谱和氢谱图。由13C-NMR可知,在δ=173.6,129处有特征峰,1H-NMR谱δ=7.210有特征峰,显示样品为含有芳香基的聚酯物。对碳谱(图 6)上的各个峰进行归属和定位(表1),由化学位移可以确定发酵产物样品中含有 C4、C5、C6,苯环连接在C5上,此外,还存在C8、C10、C12中一种或几种。由1H-NMR谱(图7)在4.082处有特征峰可知,聚合物中 C4为 4-羟基丁酸单体。结合1HNMR谱的各化学位移(表2),发酵产物样品的分子式可表示为如图8[13-15]。
由此可以看出,Pseudomonas putidaKT2442与Pseudomonas fluorescensBM07[6]有相似之处,都能在含有芳香基团的混合碳源中生长并合成带有芳香基的PHA。当Pseudomonas fluorescensBM07在含有11-苯氧基十一烷酸混合碳源的培养基中培养时,Pseudomonas fluorescensBM07能合成带有3-羟基-11-苯氧基十一烷单体的中长链 PHA,该单体在PHA中的含量最高可达10%。Pseudomonas putidaKT2442在含有苯戊酸的混合碳源中合成得到的PHA中为3-羟基苯戊酸单体。

表2 核磁氢谱图中各峰化学位移

图8 发酵产物分子式
2.2.3 发酵产物气相图谱分析
为确定聚合物中含芳香基单体PHhv含量,对发酵样品进行气相色谱分析。气相分析采用内标法,内标物为苯甲酸,保留时间和对应的标准物如表3。图 9为以蔗糖为单一碳源培养基的发酵产物色谱图,图10为以苯戊酸和蔗糖混合碳源为培养基的发酵产物色谱图。对比图 9和图 10可以知道,Pseudomonas putidaKT2442在单一培养基和混合培养基的产物在气相色谱中有不同的响应峰,在混合培养基培养的发酵产物中除了含有C6、C10、C12外,C4在图谱中也有响应。苯戊酸附近存在响应峰,进一步显示发酵产物为带有苯环的聚合物(PHPhA)。经计算,PHhv在聚合物中的含量为1.04%(质量分数)。
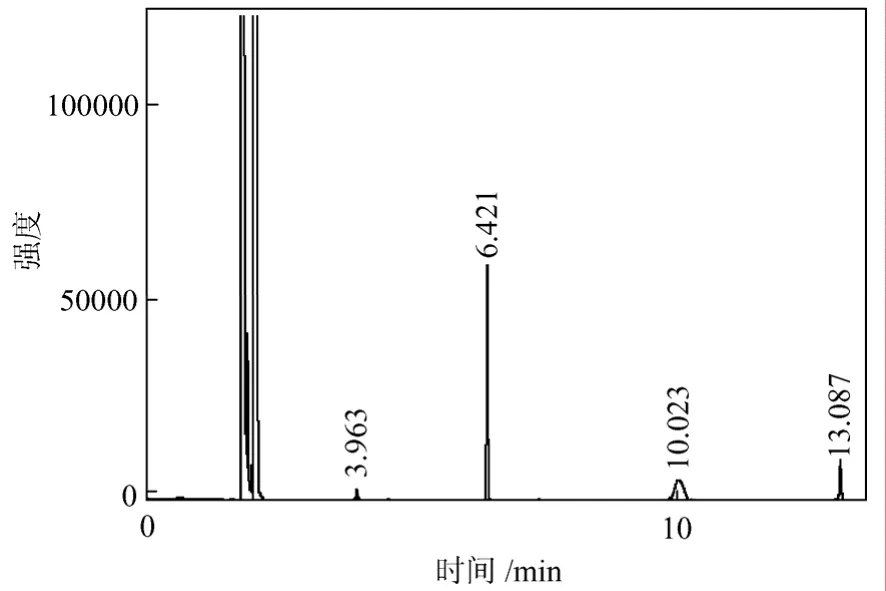
图9 单一碳源培养基的发酵产物气相色谱

图10 混合培养基发酵产物的气相图谱

表3 标准物在气相色谱中对应的保留时间
3 结 论
Pseudomonas putidaKT2442在以苯戊酸和蔗糖为混合碳源为培养基,经48~50 h的发酵培养,细胞内可积累含有中长链单体的聚羟基脂肪酸酯,且 PHA聚合链上含有苯环。经由核磁共振分析可知,苯环连接在PHA的C5亚甲基上。气相色谱显示该单含苯环单体在 PHA链中的含量不是很高,只有1.04%。
由于 PHA链上整合有苯环基团,从而可能赋予PHA新的物化性质,为PHA的改性和应用研究打下基础。
[1]Steinbüchel A. Polyhydroxyalkanoic acids//Byrom D ( Ed.) .Biomaterials:Novel Materials from Biological Sources [M]. New York:Stockto Press,1991:123-213.
[2]Feng L,Watanabe T. Wang Y,et al. Studies on comonomer compositional distribution of bacterial poly(3-hydroxybutyrate-co-3-hydroxyhexanoate)s and thermal characteristics of their fractions[J].Biomacromolecules,2002,3(5):1071-1077.
[3]Hartmann R,Hany R,Geiger T,et al. Tailored biosynthesis of olefinic medium-chain-length poly[(R)-3-hydroxyalkanoates]inPseudomonas putidaGPo1 with improved thermal properties[J].Macromolecules,2004,37:6780-6785.
[4]Hartmann R,Hamy R,Plestcher E,et al. Tailor-made olefinic medium-chain-length poly[(R)-3-hydroxyalkanoates]byPseudomonas putidaGPo1:Batch versus chemostat production[J].Biotechnology and Bioengineering,2006,93:737-746.
[5]Shi F Y,Richard A G. Microbial polyester synthesis:Effects of poly(ethylene glycol)on product composition,repeat unit sequence and group structure[J].Macromolecules,1996,29:10-17.
[6]Devang T S,MinHtien T,Piere A B,et al. Synthesis and properties of hydroxyl-terminated poly(hydroxyalkanoate)s[J].Macromolecules,2000(33):2875-2880.
[7]Ward P G,O’Connor K E. Bacterial synthesis of polyhydroxyalkanoates containing aromatic and aliphatic monomers byPseudomonas putidaCA-3[J].International Journal of Biological Macromolecules,2005,35:127-133.
[8]Olivera E R,Carnicero D,Jodra R,et al. Genetically engineered Pseudomonas:A factory of new bioplastics with broad applications[J].Environmental Microbiology,2001,3(10):612-618.
[9]Chung Y L,Lee Y H W,Yen S H,et al. A novel approach for nasopharyngeal carcinoma treatment uses phenylbutyrate as a protein kinase C modulator:Implications for radiosensitization and Ebv-targeted therapy[J].Clinical Cancer Research,2000,6(4):1452-1458.
[10]Kebebew E,Wong M G,Siperstein A E,et al. Phenylacetate inhibits growth and vascular endothelial growth factor secretion in human thyroid carcinoma cells and modulates their differentiated function[J].J. Clin. Endocrinol. Metab.,1999,84:2840-2847.
[11]Witzig T E,Timm M,Stenson Mary,et al. Introduction of apoptosis in malignant B cells by phenylbutyrate or phenylacetate in combination with chemotherapeutic agents[J].Clinical Cancer Research,2000,6(2):681-692.
[12]宁永成. 有机化合物结构鉴定与有机波谱学[M]. 北京:科学出版社,2000:28-30.
[13]Tsutomu Honma,Takeshi Imamura,Takashi Kenmoku,et al.Biosynthesis of novel poly(3-hydroxyalkanoates)containing benzoyl groups[J].Journal of Environmental Biotechnology,2004,4(1):49-55.
[14]Keenan Thomas M,Nakas James P,Tanenbaum Stuart W.Polyhydroxyalkanoate copolymers from forest biomass[J].Microbiol.Biotechnol.,2006,33:616-626.
[15]Wang Hong-hui,Zhou Xin-rong,Liu Qian,et al. Biosynthesis of polyhydroxyalkanoate homopolymers byPseudomonas putida[J].Appl. Microbiol. Biotechnol.,2011,89:1497-1507.
Biosynthesis and molecular structure characterization of polyhydroxyalkanoates containing benzoyl group
HUANG Jinbiao1,2,SHANG Long’an1
(1Ningbo Institute of Technology,Zhejiang University,Ningbo 315100,Zhejiang,China;2Department of Chemical and Biochemical Engineering,Zhejiang University,Hangzhou 310027,Zhejiang,China)
Polyhydroxyalkanoates(PHA)with the biodegradability and biocompatibility has become one of the potential medical materials. Its application fields can be enlarged by modifying the PHA’s properties. For this purpose,the PHA was synthesized by the culture ofPseudomonasputidaKT2442 with phenylvaleric acid and sucrose as mixed carbon source. The molecular structure of this biomodified PHA was characterized by NMR,IR and GC. The analysis result indicates that the biomodificated PHA is medium-length PHA which contains 3-hydroxyphenylvalerate monomer,and this monomer accounts for 1.04% of the PHA chain. This will be useful reference for further PHA study.
polyhydroxyalkanoates;biomodify;Pseudomonas putida;mixed carbon source
TQ 323.4
A
1000–6613(2011)10–2282–05
2011-04-04;修改稿日期2011-04-19。
宁波市自然科学基金项目(2006A61003)。
黄锦标(1982—),男,硕士研究生。E-mail huangke1206@163.com。联系人:尚龙安,教授,E-mail lashang@nit.net.cn。
