射干叶中异黄酮类化学成分的研究
2011-10-09张玉奎贾少华戴荣继孟薇薇邓玉林
张 良,张玉奎,陈 艳,贾少华,戴荣继,孟薇薇,李 良,邓玉林*
1北京理工大学生命学院;2北京理工亘元医药技术开发中心有限公司,北京 100081
射干叶中异黄酮类化学成分的研究
张 良1,2,张玉奎1,陈 艳2,贾少华1,2,戴荣继1,2,孟薇薇1,2,李 良1,2,邓玉林1,2*
1北京理工大学生命学院;2北京理工亘元医药技术开发中心有限公司,北京 100081
从海南产射干叶中分得 8个异黄酮类化合物,通过理化常数测定和光谱分析其化学结构分别鉴定为鸢尾黄酮新苷 A(iristectorin A,1)、野鸢尾苷 (iridin,2)、鸢尾苷 (tectoridin,3)、鸢尾苷元 (tectorigenin,4)、次野鸢尾黄素 (irisflorentin,5)、染料木素 (genistein,6)、染料木苷 (genistin,7)、樱黄素 (Prunetin,8)。所有化合物均为首次从射干叶中分离得到,其中化合物 7和 8为首次从鸢尾科植物中分离。
射干叶;鸢尾;黄酮
Abstract:Eight isoflavoneswere isolated from Leaves ofBelam canda chinensisgrown in Hainan Island.Their chemical structureswere determined by physical and chemical constants and the data of Spectroscopic identifications.They are iristectorin A(1),iridin(2),tectoridin(3),tectorigenin(4),irisflorentin(5),genistein(6),genistin(7),and Prunetin(8).All these compoundswere isolated from the Leaves ofBelam canda chinensisfor the first time,Compound 7 and Compound 8 were isolated from Iridaceae for the first time.
Key words:Leaves ofBelam canda chinensis;Iridaceae;flavone
射干 (Belam canda chinensis)为鸢尾科植物射干的干燥根茎,是临床常用中药,具有清热解毒,祛痰利咽,消痈散结的功效[1]。对射干药材的化学成分的研究很多,但射干叶的化学成分的报道十分少。本课题组对海南产射干叶进行研究,分离得到了 8种异黄酮类化合物:鸢尾黄酮新苷 A(1)、野鸢尾苷(2)、鸢尾苷 (3)、鸢尾苷元 (4)、次野鸢尾黄素 (5)、染料木素 (6)、染料木苷 (7)和樱黄素 (8)。所有化合物均为首次从射干叶中分离,其中化合物 7和 8为首次从鸢尾科植物中分离。
1 仪器与材料
Beckman DU7400型紫外可见光分光光度计;Agilent 1100 Series LC/MSD Trap(ESI源);Agilent 1200 SeriesLC/MSD TOF(ESI源 );Bruke rAR-500型核磁共振仪波谱仪 (T MS为内标);岛津 10Avp系列高效液相色谱仪:SPD-M10Avp(DAD)检测器;Classvp工作站;日本 Y MC制备柱 (ODS-A;250×20 mm;S-5μm,12 nm);岛津 20A系列高效液相色谱仪:Diamonsil色谱柱 (C18;5μm;250×4.6 mm)。葡聚糖凝胶 (Sephadex-LH20);HP20型大孔吸附树脂;聚酰胺薄层色谱及聚酰胺粉 200-400目 (浙江台州市路桥四甲生化塑料厂生产);色谱纯甲醇 (Mallinckrodt Baker,Inc.);其它试剂均为分析纯。
射干叶于 2006年 7月 15日采自海南省海口市东山镇,经北京大学医学部陈虎彪教授鉴定为鸢尾科 (Iridaceae)植物射干Belam canda chinensis(L.)DC.,标本收藏在北京理工亘元医药技术开发中心有限公司;样品号:No.20060715。
2 提取与分离
取射干叶 2 kg,粉碎成粗粉,加入 20 L蒸馏水,加热回流提取 1 h,过滤,滤渣重复以上操作 2次。合并滤液,回收溶剂至 5 L,加乙醇至含醇量为70%,离心,取上清液,减压回收溶剂至无醇味,并加水稀释至 20 L,过滤。滤液上 HP20型大孔吸附树脂,用 40%乙醇水溶液洗脱。回收溶剂得干浸膏约50 g。浸膏反复用聚酰胺色谱柱;葡聚糖凝胶色谱柱;半制备型 HPLC纯化。分离得到化合物 1(40.1 mg)、化合物 2(25.0 mg)、化合物 3(12.8 mg)、化合物 4(9.0 mg)、化合物 5(22.0 mg)、化合物 6(6.8 mg)、化合物 7(13.1 mg)和化合物 8(4.8 mg)。
3 结构鉴定
化合物 1 白色粉末,mp.212~214℃。FeCl3及Molish反应呈阳性。UVλmax(nm):268(MeOH)。ESI-MS:m/z491[M– H]–;分子式:C23H24O12。1H NMR(500 MHz,DMSO-d6)δ:12.98(1H,s,5-OH),9.20(1H,s,4′-OH),8.47(1H,s,2-H),7.19(1H,d,J=2.0 Hz,2′-H),7.01(1H,dd,J=8.0,2.0 Hz,6′-H),6.87(1H,d,J=8.0 Hz,5′-H),6.81(1H,s,8-H),3.80(3H,s,6-OCH3),3.77(3H,s,3′-OCH3)。上述理化性质和光谱数据与文献[2]报道一致,鉴定此化合物为鸢尾黄酮新苷 A(iristectorin A)。
化合物 2 白色粉末,mp.212~214℃。FeCl3及 Molish反应呈阳性。UVλmax(nm):266,330(MeOH)。ESI-MS:m/z521[M– H]–;分子式 C24H26O13。1H NMR(500 MHz,DMSO-d6)δ:12.91(1H,s,5-OH),9.28(1H,s,4′-OH),8.51(1H,s,2-H),6.99(1H,s,8-H),6.73(1H,d,J=2.0 Hz,2′-H),6.68(1H,d,J=2.0 Hz,6′-H),3.81(3H,s),3.78(3H,s),3.75(3H,s)。上述理化性质和光谱数据与文献[3]报道一致,鉴定此化合物为野鸢尾苷 (iridin)。
化合物 3 白色粉末,mp.272~273℃。FeCl3及Molish反应呈阳性,盐酸镁粉反应呈阴性,Gibb’s反应阳性,浓硫酸反应呈黄色。ESI-MS:m/z485[M+Na]+,463[M+H]+;分子式 C22H22O11。1H NMR(500 MHz,DMSO-d6)δ:12.91(1H,s,5-OH),9.61(1H,s,4′-OH),8.44(1H,s,2-H),7.39(2H,d,J=8.5 Hz,2′,6′-H),6.82(2H,d,J=8.5 Hz,3′,5′-H),6.88(1H,s,8-H),3.32(3H,s,6-OCH3),5.43(1H,d,J=5.0 Hz,1′′-H)。13C NMR(125 MHz,DMSO-d6)δ:154.8(C-2),122.3(C-3),180.6(C-4),157.8(C-5),139.8(C-6),157.6(C-7),94.2(C-8),153.1(C-9),106.3(C-10),122.6(C-1′),130.4(C-2′,6′),115.3(C-3′,5′),157.4(C-4′),60.4(-OCH3),100.4(glc-1),73.3(glc-2),77.5(glc-3),69.8(glc-4),76.9(glc-5),60.8(glc-6)。上述理化性质和光谱数据与文献[4]报道一致,鉴定此化合物为鸢尾苷 (tectoridin)。
化合物 4 浅黄色针晶,mp.215~216℃。盐酸镁粉反应呈阴性。ESI-MSm/z:299[M– H]–;分 子 式 C16H12O6。UVλmax(nm):265,322(MeOH)。1H NMR(500MHz,DMSO-d6) δ:13.09(1H,s,5-OH),10.77(1H,s,7-OH),9.58(1H,s,4′-OH),8.35(1H,s,2-H),7.39(2H,d,J=8.0 Hz,2′,6′-H),6.83(2H,d,J=8.0 Hz,3′,5′-H),6.51(1H,s,8-H),3.74(3H,s,6-OCH3)。上述理化性质和光谱数据与文献[5]报道一致,鉴定此化合物为鸢尾苷元(tectorigenin)。
化合物 5 白色针晶,mp.137~139℃。UVλmax(nm):265,320(MeOH)。ESI-MSm/z:408[M+Na]+,386[M+H]+;分子式 C20H18O8。1H NMR(500 MHz,DMSO-d6)δ:8.30(1H,s,2-H),7.02(1H,s,8-H),6.83(2H,s,2′,6′-H),6.18(2H,s,-OCH2O-),3.90(3H,s,5-OCH3),3.79(6H,s,3′,5′-OCH3),3.68(3H,s,4′-OCH3),上述理化性质和光谱数据与文献[6]报道一致,鉴定此化合物为次野鸢尾黄素 (irisflorentin)。
化合物 6 白色针晶,mp.265~267℃。高分辨质谱 (LC/MSD TOF)测定m/z269.0464[M–H]–(计 算 值:269.0447);分 子式 C15H10O5。1H NMR(500 MHz,DMSO-d6)δ:12.94(1H,s,5-OH),10.87(1H,s,7-H),9.60(1H,s,4′-OH),8.30(1H,s,2-H),7.33(2H,d,J=8.5 Hz,2′,6′-H),6.98(2H,d,J=8.5 Hz,3′,5′-H),6.37(1H,d,J=2.0 Hz,8-H),6.21(1H,d,J=2.0 Hz,6-H)。13C NMR(125 MHz,DMSO-d6)δ:180.6(C-4),164.9(C-7),162.2(C-5),157.8(C-4′),157.6(C-9),154.0(C-2),130.5(C-2′,6′),122.4(C-1′),115.2(C-3′,C-5′),104.6(C-10),99.7(C-6),91.0(C-8)。上述理化性质和光谱数据与文献[7]报道一致,鉴定此化合物为染料木素 (genistein)。
化合物 7 白色粉末,mp.250~251℃。盐酸镁粉反应呈阴性,硫酸反应呈黄色,Molish反应呈阳性。化合物经酸水解,产物通过 HPLC鉴定有染料木素,通过 PC鉴定有 D-葡萄糖。UVλmax(nm):264(MeOH)。ESI-MS:高分辨质谱 (LC/MSD TOF)测定m/z431.1081[M– H]–(计算值:431.0972)。分子式:C21H20O10。1H NMR(500 MHz,DMSO-d6)δ:12.88(1H,s,5-OH),9.62(1H,s,4′-OH),8.41(1H,s,2-H),7.42(2H,d,J=8.5 Hz,2′,6′-H),6.82(2H,d,J=8.5 Hz,3′,5′-H),6.70(1H,d,J=2.0 Hz,8-H),6.45(1H,d,J=2.0 Hz,6-H),5.13(1H,d,J=4.5 Hz,1′′-H),3.15-3.71(m,other sugar protons);13C NMR(125MHz,DMSO-d6)δ:154.3(C-2),122.7(C-3),180.4(C-4),161.6(C-5),99.6(C-6),163.1(C-7),94.8(C-8),157.3(C-9),106.0(C-10),121.0(C-1′),130.2(C-2′,6′),115.2(C-3′,5′),157.0(C-4′),99.9(C-1′′),73.1(C-2′′),77.5(C-3′′),69.4(C-4′′),76.4(C-5′′),60.7(C-6′′).上述理化性质和光谱数据与文献[8]报道一致,鉴定此化合物为染料木苷 (genistin)。
化合物 8 白色针晶,mp.242~243℃。UVλmax(nm):262(MeOH)。ESI-MSm/z:307[M+Na]+,285[M+H]+。高分辨质谱 (LC/MSD TOF)测定m/z283.0676[M–H]– (计算值 :283.0603)。分子式 C16H12O5。1H NMR(500 MHz,DMSO-d6) δ:12.91(1H,s,5-OH),9.95(1H,brs,4′-OH),8.35(1H,s,2-H),7.49(2H,d,J=8.5 Hz,2′,6′-H),6.99(2H,d,J=8.5 Hz,3′,5′-H),6.38(1H,d,J=2.0 Hz,8-H),6.22(1H,d,J=2.0 Hz,6-H),3.77(3H,s,7-OCH3)。13C NMR(125 MHz,DMSO-d6)δ:154.2(C-2),122.9(C-3),180.0(C-4),161.9(C-5),99.0(C-6),164.4(C-7),93.7(C-8),157.5(C-9),104.4(C-10),121.9(C-1′),130.1(C-2′,6′),113.7(C-3′,5′),159.1(C-4′),55.1(-OCH3)。上述理化性质和光谱数据与文献[9,10]报道一致,鉴定此化合物为樱黄素(prunetin)。
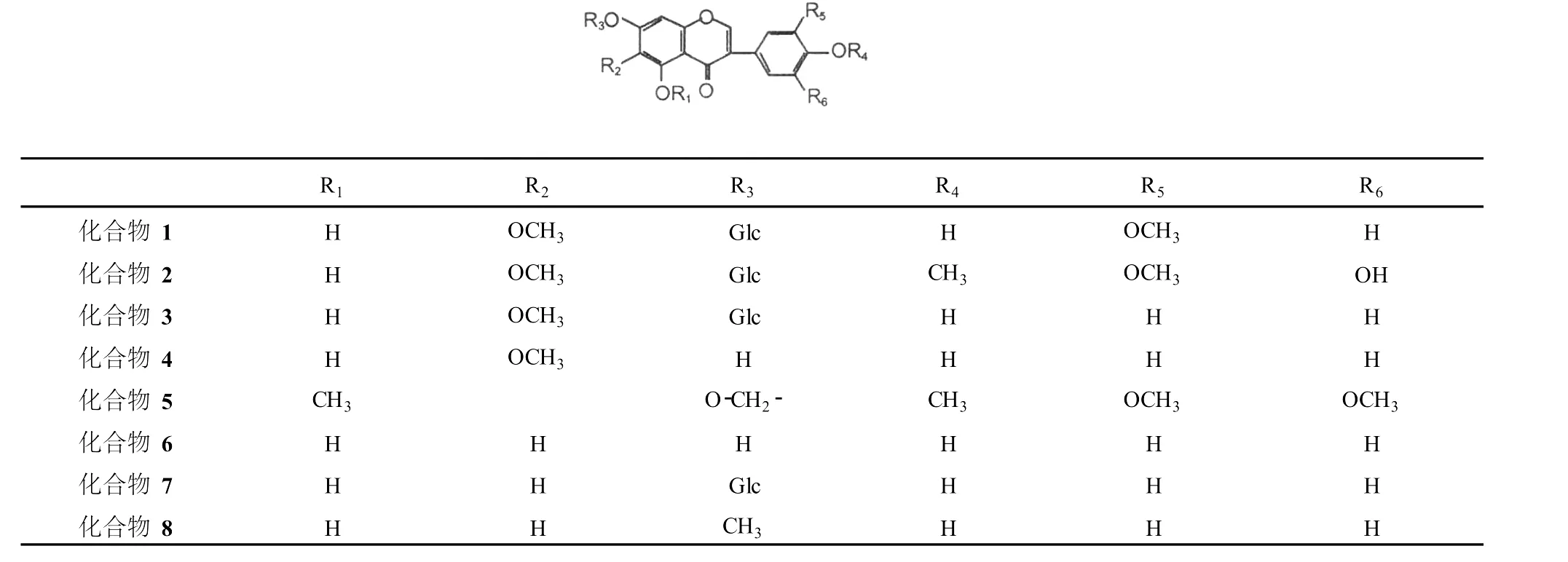
图1 射干叶中 8种异黄酮类化合物的结构式Fig.1 The structural for mulas of compounds 1-8
1 DingAW(丁安伟).Clinical Handbook of Modern Chinese Medicine(现代中药临床手册).Nanjing:Jiangsu Science and Technology Publishing House,2000.75-76.
2 Yuan CJ(袁崇均 ),Wang J(王笳 ),et al.Study on the chemical constituents ofIris tectorumMaxim.Nat Prod Res Dev(天然产物研究与开发),2008,20:444-446.
3 Li R(李蓉 ),Qin MJ(秦民坚 ).Studies on the constituents ofIris leptophylla.J China Pharm Univ(中国药科大学学报),2003,34:122-124.
4 Qiu YK(邱鹰昆),Xu BX(徐碧霞),et al.An NMR study of isoflavones extracted fromBelam canda Chinensis.Chin J Mag Res(波谱学杂志),2006,23:443-449.
5 LiL(黎路),QinMJ(秦民坚).Chemical constituents ofIris cathayensisMigo.J Chin Pharm Univ(中国药科大学学报),2005,36:111-113.
6 Agarwal VK,Thappa RK,Agarwal SG,et al.Isoflavones of twoIris species.Phytochem istry,1984,23:2703-2704.
7 Pa lme E,Bilia AR,Morelli I.Flavonols and isoflavones fromCotoneaster simonsii.Phytochem istry,1996,42:903-905.
8 Wang CT(王春桃),Tang YP(唐于平),Zhou L(周玲 ),et al.The study on the flavonoids in bark of pagoda.Jiangsu J Tradit Chin Med(江苏中医药),2008,40:65-67.
9 Peng T(彭腾 ),Tu YQ(涂永勤 ),Deng Y(邓赟 ),et al.Studies on chemical constituents ofPr imula sikk mensis.J Chin Med Mat(中药材),2008,31:44-46.
10 Rute FV,HelderM,Generosa T,et al.Flavonoids of an extract ofPterospartum tridentatumshowing endothelial protection against oxidative injury.J Ethnopha rmacol,2004,93:363-370.
Isoflavones in Leaves of Bela mcanda chinensis
ZHANGLiang1,2,ZHANG Yu-kui1,CHEN Yan2,J IA Shao-hua1,2,DA IRong-ji1,2,MENG Wei-wei1,2,L ILiang1,2,DENG Yu-lin1,2*1
1Life Science and Technology School,Beijing Institute of Technology;2Beijing B IT&GY Phar maceutical R&D CO.,LTD;Beijing 100081,China
R284.2;Q946.91
A
1001-6880(2011)01-0069-03
2009-07-27 接受日期:2009-09-08
*通讯作者 E-mail:deng@bit.edu.cn
