甘草酸单铵盐的制备及纯化新工艺研究
2011-10-09史高峰周宝华陈学福
史高峰,徐 静,周宝华,邓 丽,陈学福
(兰州理工大学石油化工学院,甘肃兰州730050)
甘草酸单铵盐的制备及纯化新工艺研究
史高峰,徐 静,周宝华,邓 丽,陈学福
(兰州理工大学石油化工学院,甘肃兰州730050)
考察了以甘草为原料,采用溶剂法制得甘草酸单铵盐,并利用工业乙醇和80%乙醇为重结晶溶剂对其精制纯化。通过对比实验,确定了新的溶剂法工艺条件为:热回流法提取的甘草酸,经工业乙醇浸提、浓氨水氨化,在酸化过程中,先加一定量冰乙酸调节pH到4.5,再加前述2倍量冰乙酸制得甘草酸单铵盐粗品,其含量达66.7%,得率为2.58%。获得了结晶精制纯化工艺为:经工业乙醇、80%的乙醇和工业乙醇对粗品交替重结晶三次,固液比分别为1∶40、1∶15和1∶40,最终甘草酸单铵盐含量达80.1%,得率为1.36%。
甘草酸,甘草酸单铵盐,冰乙酸,重结晶,乙醇
甘草酸单铵盐(monoammonium glycyrrhizinate,简称MAG)为白色针状结晶(稀乙醇),熔点212~217℃(分解),无臭,味甜[1],可溶于热水,极微溶于无水乙醇,几乎不溶于氯仿、乙醚、苯,不溶于冰醋酸。它是一种高甜度、低热量、安全无毒的甜味剂[2],而且可作为制备甘草次酸[3-4]、高纯度甘草酸[5]的中间体,因此被广泛用于食品、医药和化妆品等行业。当前MAG的制备主要采用溶剂法,即先冷浸制得甘草酸粗粉,再以它为原料经浸提、氨化、酸化等步骤制得,文献[2,6-8]对浸提所用溶剂及方法、氨化方法已作了改进,并采用柱分离得到精品,但依然存在操作时间长或产品含量低等缺点。本文以甘草为原料,热回流提取甘草酸,并对酸化方法作调整,最后通过不同浓度和固液比的乙醇重结晶得其精品,以高效液相色谱法测定其含量,旨在改进MAG的制备及纯化工艺,得到含量较高的产品,为工业化生产提供依据。
1 材料与方法
1.1 材料与仪器
胀果甘草 国外进口;工业乙醇(乙醇含量95%) 工业级;甲醇、乙腈 天津光复精细化工研究所,色谱纯;甘草酸单铵盐标准品(含量75%)
Sigma公司;其它化学试剂 均为分析纯。
SHZ-D(Ⅲ)型循环水泵 天津华鑫仪器厂;旋转蒸发仪RE-3000 上海亚荣生化仪器厂;电子分析天平 FA-1004 上海恒平科学仪器有限公司;Survwyor高效液相色谱分析仪 配有PDA检测器,美国Finnigan公司。
1.2 实验方法
1.2.1 工艺流程 甘草→热回流→抽滤→真空浓缩→酸沉→水洗→干燥→浸提→脱色→真空浓缩→氨化→酸化→过滤→洗涤→重结晶→过滤→干燥→成品
1.2.2 MAG含量的测定方法 以从Sigma公司购买的含量为75%的MAG标准品作为对照,采用高效液相色谱(HLPC)法测定制得的MAG的含量。
1.2.2.1 HPLC色谱条件 色谱柱为SB-C18色谱柱(150×2.1mm,Agilet);流动相:乙腈∶甲醇∶NH4Ac/HAc(0.1mol/L)=68∶32∶1;柱温:20℃;流速:0.2mL/min;进样量:5μL。
1.2.2.2 标准曲线的绘制 精密称取MAG标准品1.45mg,甲醇定容于10mL容量瓶中作为储备液,取该液1mL再以甲醇稀释定容于10mL容量瓶中;自动进样1、3、5、7、9μL,在上述色谱条件下检测,每个浓度的标准品平行测定3次,求出峰面积平均值。以峰面积(Y)对浓度(X)进行回归,得线性方程:Y=1387.7X+43749,R=0.9993。结果表明,MAG进样量在1~9μL范围内线性关系良好。

图1 峰面积与浓度的线性关系图
1.2.3 实验过程
1.2.3.1 甘草酸的粗提 称取甘草100.0g,切碎,加入含氨为 0.5%的 10%(质量分数)乙醇水溶液800.0g,于80℃回流提取两次,每次2h,过滤,合并提取液,真空浓缩至原体积的1/8,在剧烈搅拌下滴加经稀释过的硫酸(浓硫酸∶水=1∶1,V/V),调节pH至1.5~2.0,放置3h,减压过滤,滤饼用水洗涤pH至3.5,烘干得甘草酸粗品8.61g。
1.2.3.2 甘草酸的精提 将甘草酸粗品加入861.0g工业乙醇,于45~50℃回流提取两次,每次2h,减压过滤,合并滤液,加活性炭0.22g,于80℃煮沸20min,趁热过滤,真空浓缩至70mL,得精制的甘草酸乙醇溶液。
1.2.3.3 氨化 将精制甘草酸液冷却至室温,在搅拌条件下滴加浓氨水调节pH至7.5,待黄色沉淀(甘草酸三铵盐)不再产生后,放置0.5h。
1.2.3.4 酸化 将黄色沉淀先加入4.3mL的冰乙酸调pH至4.5,并于75℃保温5~10min,然后冷却至室温,再加8.6mL的冰乙酸,放置结晶1h,过滤,分别用少量冰乙酸和无水乙醇洗涤,烘干得 MAG粗品2.58g。
1.2.3.5 甘草酸单铵盐的精制纯化 将该粗品加入103.2g工业乙醇,于80℃热溶,趁热过滤,滤液冷却至室温,析晶1h,过滤;所得固体加入38.7g 80%乙醇,于80℃热溶,趁热过滤,冷却至室温,析晶2h,过滤;所得固体再加入103.2g工业乙醇,于80℃热溶,趁热过滤,冷却至室温,析晶1h,过滤,干燥得精品1.36g。
2 结果与讨论
2.1 热回流法提取甘草酸的确定
目前提取甘草酸的方法很多,如传统的冷浸、热浸、热回流、渗漉等以及近年来发展起来的超声波、微波辅提等方法[9-10]。冷浸、渗漉、热浸等工艺操作时间较长(30h以上),设备占用率高,增加了生产成本。超声波、微波萃取法提取具有效率高、选择性好、省时等优点,但目前还大多集中于实验室中的小批量研究[11]或中试研究,还没有研发出配套成熟的工业化提取设备[12]。而文献[7]认为只有冷浸法提取甘草酸适合用溶剂法制备MAG,为此分别考察以水冷浸和含氨0.5%的10%乙醇(质量分数)溶液热回流提取的甘草酸(固液比均为1∶8,g/g;次数均为两次)用溶剂法制备MAG(其中酸化过程均为改进后的,见2.2),结果如表1。
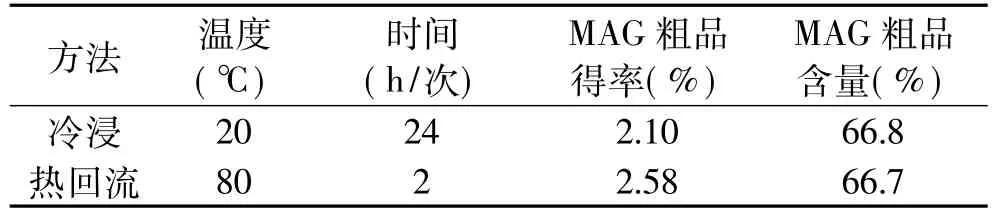
表1 冷浸与热回流提取甘草酸制备MAG的对比
通过表1可以看出,两种方法所制备的MAG粗品含量基本接近,但后者操作时间短,得率(以原草计,下同)较高,表明热回流较冷浸提取的甘草酸更适合用溶剂法制备MAG。
2.2 酸化方法的改进
热回流法提取的甘草酸粗品,经工业乙醇精提、浓氨水氨化后,向甘草酸三铵盐加入冰乙酸,除生成MAG外,还生成乙酸铵,它与反应剩余的乙酸形成乙酸铵—乙酸缓冲溶液。在该酸性缓冲体系中,随着酸度的提高,MAG的溶解度逐渐下降而较快地析出,若全为冰乙酸时,MAG不溶,即溶解度约为0;当调节pH到4.5时(理论计算[13]此时乙酸铵∶乙酸 =1∶1.4),MAG会缓慢析出,若再向其中加入一定量的冰乙酸调节该溶液酸度,MAG就会以合适的速度析晶,含量也会较高。需要注意的是,此过程中大量杂质也要逐渐析出,故控制析晶速度,尽可能有利于目标物的析出成为解决问题的关键。为此考察冰乙酸不同的再加入量对MAG粗品含量的影响,结果见表2。
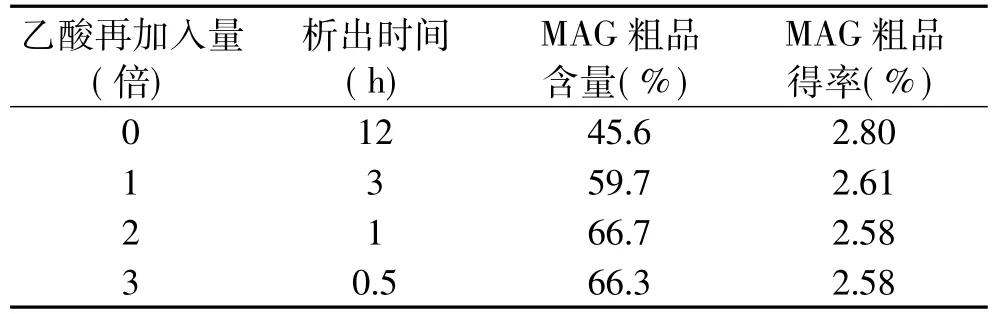
表2 乙酸不同再加入量对MAG粗品含量的影响
由表2可知,不再加冰乙酸与其他再加冰乙酸所得的粗品,其含量都低,可能是由于析出时间太长,析出速度太慢,大量杂质伴随析出;而冰乙酸加入越多,析出相对较快,所得粗品含量越高;同时,再加3倍与再加2倍的冰乙酸所得粗品相比较,含量都较高且析出时间短,但冰乙酸加入量越大,对设备的要求越高,成本越高,从经济和工业化的角度考虑,再加2倍的冰乙酸比较合理。
2.3 MAG的精制纯化
为了得到含量较高的MAG,以乙醇溶液重结晶溶剂,考察重结晶的最佳固液比、次数以及方法对其含量的影响。
2.3.1 重结晶溶剂对应的固液比的选择 由于MAG粗品在不同溶剂(80℃)中的溶解度不同,要求固液比也就不同,进而决定其溶解和析晶速度,导致含量不同。分别以工业乙醇和80%的乙醇溶液为溶剂重结晶(一次),考察其纯化效果,结果见表3。
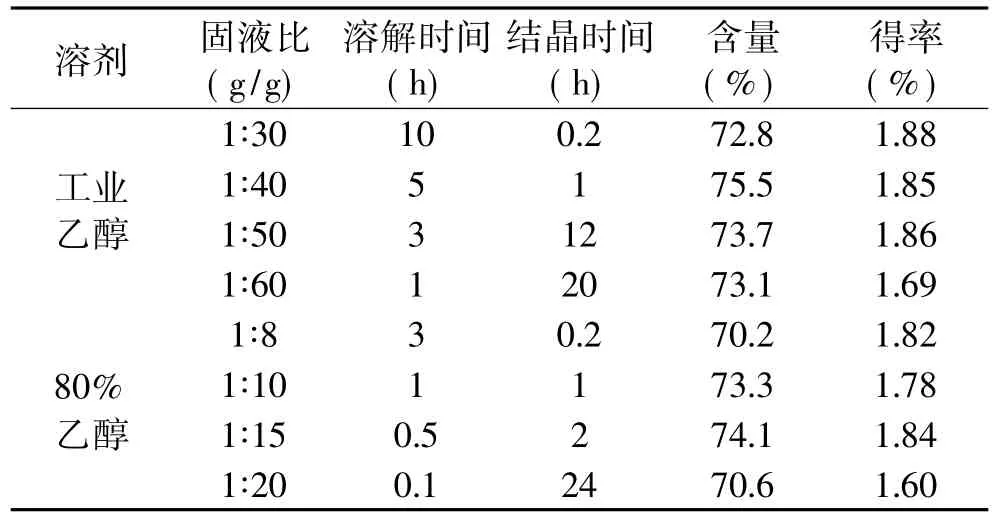
表3 工业乙醇和80%乙醇对MAG粗品结晶纯化效果的对比
从表3可看出,两种溶剂均可作为重结晶的溶剂,使MAG的含量提高;从产品含量、得率和操作时间上综合考虑,当选用工业乙醇时,最佳固液比为1∶40;当选用80%乙醇时,最佳固液比为1∶15。
2.3.2 重结晶(同种溶剂)次数对MAG含量的影响
对于上述两种溶剂,以确定的最佳固液比,分别考察重结晶次数对MAG纯化效果的影响,结果见表4和表5。

表4 重结晶(工业乙醇)次数对MAG含量和得率的影响

表5 重结晶(80%乙醇)次数对MAG含量和得率的影响
从表4、表5可以看出,在所用溶剂不变的条件下,增加重结晶的次数,其含量只有小幅度提高。
2.3.3 溶剂交替重结晶对MAG含量的影响 由于在同种溶剂条件下,难以用多次重结晶达到理想的纯化效果,考察使用两种溶剂交替重结晶对其纯化效果,结果见表6。醇、80%乙醇重结晶,以此类推。

表6 两种溶剂交替重结晶对MAG含量的影响
从表6可以看出,当交替使用这两种溶剂时,可以较大程度地提高MAG含量,特别是采用工业乙醇、80%乙醇和工业乙醇的顺序交替重结晶,含量提高到了80.1%。
2.3.4 精制纯化重现性效果验证 准确称取含量为66.7%的MAG粗品2.58g,依次按固液比1∶40、1∶15和1∶40加入工业乙醇、80%乙醇、工业乙醇三次重结晶,得MAG精品1.35g,含量为80.2%。精制纯化效果表明,该工艺重现性好。
3 结论
3.1 通过对比实验,确定了改进的溶剂法工艺条件为:热回流提取的甘草酸,经工业乙醇精提、浓氨水氨化后,在酸化过程中,先加一定量冰乙酸调节pH到4.5,再加前述2倍量冰乙酸制得MAG粗品,其含量达66.7%,得率为2.58%,该工艺操作时间短,粗品含量和得率高。
3.2 获得了MAG的精制纯化工艺为:用工业乙醇、80%乙醇和工业乙醇交替重结晶三次,固液比分别为1∶40、1∶15和1∶40,最终的MAG含量达80.1%,得率为1.36%,该工艺重现性好,可为工业化生产提供依据。
[1]刘淼.中草药成分提取分离与制剂加工新技术新工艺新标准[M].北京:中国教育出版社,2003:778-781.
[2]兰霞.甘草酸单铵盐的制备[D].江南大学,2009.
[3]L A Baltina,E V Vasil’eva,V A Davydova,et al.Synthesis and pharmacologicalpropertiesamidesofa seriesofnew heterocyclic and aromatic of glycyrrhizic acid[J].Pharmaceutical Chemistry Journal,1996,30(8):503-506.
[4]L A Baltina,O B Flekhter,Zh M Putieva,et al.Hydrolysis of β-glycyrrhizic acid[J].Pharmaceutical Chemistry Journal,1996,30(4):263-266.
[5]李仕坤,谢蓥.纯甘草酸结晶的提取[J].兰州医学院学报,1992,18(4):254-255.
[6]佟连生,田云.从甘草酸粗品制取甘草酸单铵盐[J].黑龙江医药科学,2004,27(4):51.
[7]吴安心,杨维东,陈世武.甘草酸单铵盐的工艺研究[J].中国医药工业杂志,1997,28(11):486-488.
[8]王金秋,周维纯,宋金表,等.甘草酸单铵盐的精制工艺研究[J].林产化工通讯,2001,35(1):8-13.
[9]王梅兰.甘草酸三铵盐的提取制备[J].海峡药学,1996,8(3):66.
[10]韩学哲.种植甘草中的甘草酸及黄酮提取纯化工艺研究[D].兰州理工大学,2009.
[11]苏佳华.微波萃取技术在中药有效成分提取中的应用[J].海峡药学,2008,20(7):123-125.
[12]白中明.工业化超声波中药提取装备研究[J].中草药,2005,36(8):50-52.
[13]国家标准委,卫生部.GB 5749-2006生活饮用水卫生标准[S].北京:中国标准出版社,2007.
Study on new process for the production and purification of monoammoniun glycrrhizinate
SHI Gao-feng,XU Jing,ZHOU Bao-hua,DENG Li,CHEN Xue-fu
(Institute of Petro-Chemical Technology,Lanzhou University of Technology,Lanzhou 730050,China)
Through solvent process,monoammoniun glycrrhizinate was gained from radix glycyrrhizae,and it was refined through recrystallization method using the solvent—industrial alcohol and 80% alcohol.The improve conditions of solvent process were found by the contrast experiment,they were glycrrhizin extracted hot reflux,and then digestioned by industrial alcohol,aminateed by stronger ammonia water,treated through first dropwise a certain quality of glacial acetic acid into triammonium glycyrrhizinate at pH 4.5 and then dropwise 2 times of glacial acetic acid mentioned earlier,purity and yield of crude monoammoniun glycrrhizinate were 63.3%and 2.58%.Following the optimum conditions,recrystallization were tested,they were treated by recrystaled in sequence of industrial alcohol,80%alcohol and industrial alcohol with solid-to-liqid ratio of 1∶40,1∶15,1∶40 for crude monoammoniun glycrrhizinate,purity and yield of monoammoniun glycrrhizinate were 80.1%and 1.36%after all.
glycrrhizin;glacial acetic acid;monoammoniun glycrrhizinate;recrystal;alcohol
TS201.1
A
1002-0306(2011)04-0324-03
2010-04-07
史高峰(1963-),男,博士,教授,主要从事天然药物、天然有机合成及生物化工等方面的研究。
