利用蒸锗残酸生产电池用氯化锌
2011-09-27苏飞
苏 飞
(韶关冶炼厂,广东 韶关 512024)
利用蒸锗残酸生产电池用氯化锌
苏 飞
(韶关冶炼厂,广东 韶关 512024)
利用蒸锗后的残酸和次氧化锌生产电池用液体氯化锌。残酸与次氧化锌反应得到粗氯化锌溶液,添加双氧水、高锰酸钾、锌粉等净化得到精氯化锌溶液,最后蒸发浓缩制成电池用氯化锌产品。用该方法制备的液体氯化锌既满足电池厂的要求,同时符合HG/T2323—2004标准,并且原料价廉,环保效益、经济效益明显。
蒸锗残酸;次氧化锌;氯化锌;电池
0 引言
韶关冶炼厂将含有铟、锗、镓、锑等有价稀有金属的各种物料采取不同的方法进行综合回收,其中锗、铟的回收主要采用盐酸浸出-氯化蒸馏-萃取提纯等工艺。在锗的回收中,氯化蒸馏是重要的生产过程,但是氯化蒸馏提锗后产生的含酸废液每年有近1 500 m3,残液含HCl约7 mol/L左右,折合成浓度30%的工业盐酸约1 250 t。以往残液的处理是稀释至含HCl 3~4 mol/L后萃铟,萃铟后液加石灰中和至pH为9时再送总厂污水处理站处理,石灰用量每天3~4 t。该方法相当于每年浪费1千多吨浓盐酸,同时消耗七八百吨的石灰,浪费严重。
液体氯化锌是一种生产电池的原料,而且氯化锌浓溶液能制成具有显著酸性能的一羟基二氯合锌配合酸,其能溶解金属氧化物例如氧化亚铁,广泛应用于焊接工业中。如果用蒸馏残酸和韶冶自产的次氧化锌做原料,生产可供电池用的液体氯化锌,不仅综合利用了残酸中的盐酸,节省了每年用于污水处理的近千吨石灰,环保效益、经济效益明显,而且对工厂的节能增效工作具有重要的意义。
1 实验部分
1.1 试验目的
蒸馏残液含HCl高达7 mol/L,其中还富集了铟,因此蒸馏残液稀释至3~4 mol/L用萃取剂萃铟,以实现有价稀有金属的全面回收。蒸馏残液萃铟后经过氧化、活性炭吸附等工艺处理的滤清液即为实验所用的原料之一;另一原料来源于韶冶鼓风车间产出的次氧化锌。处理后的蒸馏残液含HCl仍高达130 g/L,次氧化锌含锌53%左右,以二者为原料制备氯化锌,既利用了残液中的酸又节省了处理残液的大量石灰。
1.2 原料及辅料
原料:经过处理的蒸馏残酸及次氧化锌,组成见表1、表2。

表1 处理后的蒸馏残液的化学成分 g/L
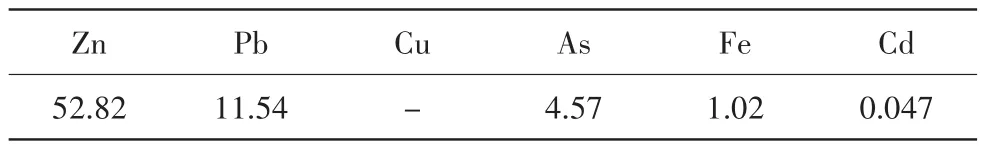
表2 次氧化锌的化学成分 %
辅料:锌粉,100~150目;盐酸(28%~30%),工业级;高锰酸钾(99%),工业级;氯化钡(99%),工业级;六水氯化铁(99%),工业级;双氧水(27%),工业级。
1.3 工艺流程
制备液体氯化锌的工艺流程见图1。次氧化锌与处理后的蒸馏残液首先通过浸出反应产出粗氯化锌溶液,然后分阶段添加适量的双氧水、氯化铁、高锰酸钾、锌粉等净化得到精氯化锌溶液,最后蒸发浓缩制成电池用氯化锌产品。
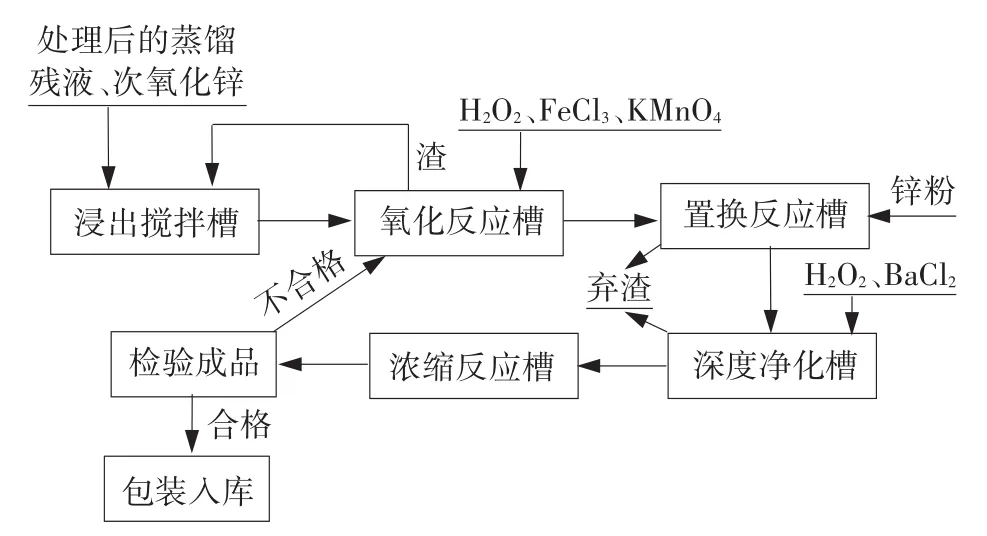
图1 制备液体氯化锌的工艺流程图
2 工艺过程控制
2.1 浸出
次氧化锌和处理后蒸馏残液(含HCl 3~4mol/L)按固液比1:4连续投入到浸取反应器,在80~90℃条件下充分反应,反应时间>2 h,反应终点用次氧化锌调整pH=4。为获得较高浓度的氯化锌溶液,要求原料次氧化锌含锌>50%。随着锌的浸出,杂质Fe、Cu、Cd、Pb、As等也进入溶液。pH的控制对浸出过程有较大影响,pH越小,浸出率越高,溶液澄清效果越好,但是进入溶液的杂质也明显增多,增加净化工序处理量。pH高,溶液澄清较困难,浸出液ZnCl2含量降低,但是进入溶液的杂质相对较少。多次试验证明,浸出终点pH控制在4左右比较合适。浸出结束,通过压滤使渣液分离。
浸出过程主要反应如下:

浸出液的化学成分见表3。

表3 浸出液化学成分 g/L
渣液分离后,浸出液进入净化工序除杂,滤渣用工业盐酸再次浸出以使原料反应完全。
2.2 净化除杂
2.2.1 氧化沉淀除As、Mn、Fe
根据原料的特性和化学成分,在一个净化搅拌槽内分两步氧化去除砷、铁、锰。第一次氧化加入适度过量的H2O2和FeCl3,浸出液pH为4.5,在60℃下保温搅拌3h[1],目的是使低价的As转化为高价态的As,基于Fe3+与砷有较好的亲和性,Fe3+与As3+可生成无毒无害的FeAsO3沉淀或FeAsO3与Fe(OH)3的复合体沉淀而被除去。
主要反应如下:

试验表明:Fe3+可有效去除As(Ⅲ),去除率达98%以上;As(Ⅲ)去除率受Fe3+加入量和溶液pH等因素的影响,调节pH值和增加Fe3+的加入量可有效提高As(Ⅲ)的去除率;延长搅拌时间对As(Ⅲ)的去除率几乎无影响。
第二次氧化反应先用少量锌粉调整溶液pH至5.5,然后加入氧化剂KMnO4和适量的FeCl3将温度升高至90℃下保温搅拌2 h,进一步除去As、Mn、Fe等杂质,然后进行压滤。
2.2.2 置换除杂去除其他重金属杂质
在60~80℃搅拌条件下,按照检测出的滤液中Pb2+,Cu2+、Cd2+等重金属离子浓度理论量的120%加入锌粉,使其中的重金属杂质置换出来。
主要反应如下:

锌粉置换各金属离子的界限浓度见表4[2]。

表4 锌粉置换各金属离子的界限浓度 mol/L
锌粉投料应缓慢,搅拌时间不应低于2 h,之后静置陈化、过滤即可,此过程产生的废渣主要成分为Pb、Cu及部分未反应的Zn粉,积累一定数量后由冶炼厂的综合回收系统再处理,回收其中的铅、铜。
2.2.3 深度除Fe、SO42-
锌粉置换去除重金属杂质后,ZnCl2溶液中的大部分杂质已除去。由于电池用液体氯化锌对Fe离子和SO42-的含量要求比较严格,所以需要深度除Fe离子和SO42-。这一过程主要是添加适度的氧化剂H2O2将Fe2+转化成Fe3+,然后控制溶液pH4.5左右,使Fe3+水解后沉降分离,同时加入适量的BaCl2溶液去除SO42-。
主要化学反应如下:
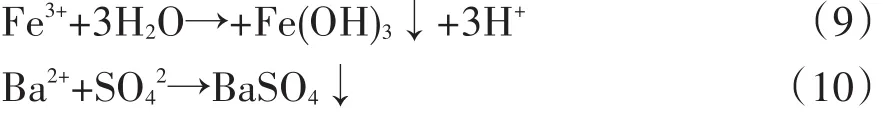
溶液pH与残存Fe3+浓度的关系见表5[2]。

表5 溶液pH与残存Fe3+的关系
操作时先加入双氧水,后加入氯化钡。双氧水应缓慢加入,溶液温度<40℃,添加完成后将溶液温度升高至90℃搅拌2 h,然后加入BaCl2溶液继续搅拌1 h,深度净化后上清液取样化验,结果见表6。

表6 深度净化液的成分
2.3 蒸发浓缩
要满足电池厂和国家标准要求,液体氯化锌还需进一步浓缩处理。加热蒸发溶液,在热态下测量氯化锌溶液的比重为47~50Be,即可,常温下氯化锌液的比重就可达到52~53Be,,已满足电池厂的要求(广东某电池厂对液体氯化锌比重的要求是达到52Be,)。氯化锌的浓缩过程要求在酸性环境中进行,以防水解生成碱式盐而影响产品质量。因此,浓缩前应调整溶液pH在3左右,并提高浓缩温度,使之快速浓缩以防失酸,导致产品结块。在试生产时,加热蒸发溶液,在热态下一定时间隔取样测试比重,达到47~50Be,时即可停止加热,取样分析化学成分,杂质含量满足要求时即为合格产品转入成品储槽,若杂质含量超标则再处理或者转入上一阶段净化过程继续处理,直至产品合格。
根据小试优化条件,试生产的产品质量技术指标完全符合国家标准[3]和电池厂的要求,见表7。
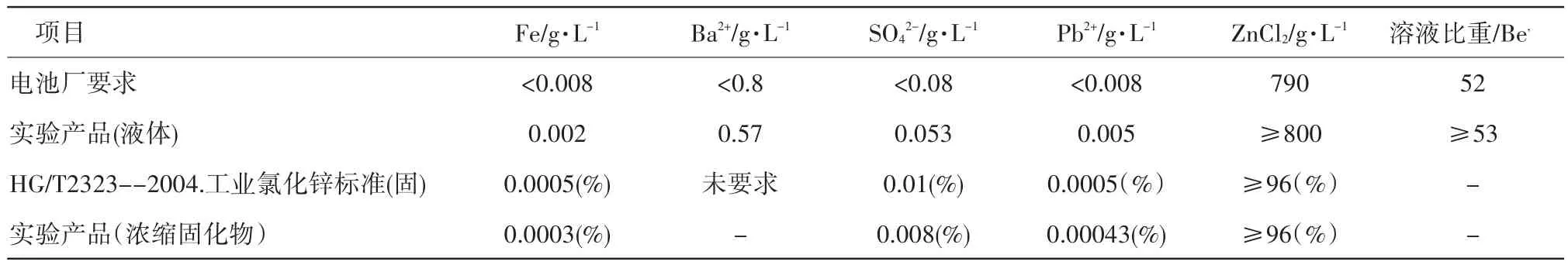
表7 液体氯化锌产品质量指标
2.4 产品质量的保证
最终产品的质量取决于每一道工序的质量控制,因此各工序都应有相应的化学检验要求,定时定点取样化验。最终产品是比重53Be,的液体氯化锌(常温),当生产出现中浓缩过度、浓度过高的情况时,可用蒸馏水稀释;当成品中SO42-、Pb2+、Ba2+分别超标时,可根据化验结果分别向浓缩搅拌槽中添加适量的氯化钡、锌粉、硫酸搅拌净化,直至化学成分符合要求再进行过滤;成品中Fe2+超标时,要返回氧化槽重新氧化净化。
3 结束语
用处理过的蒸馏残液和本厂自产的次氧化锌生产电池用氯化锌的工艺条件为:浸取温度85~90℃,pH3.5~4.0;一次净化温度60~70 ℃,pH5.1;二次净化温度60~80℃,锌粉用量为理论量的120%。制备的电池用氯化锌质量符合HG/r12323—2004标准。本工艺不仅为企业开辟了一条生产电池用氯化锌的新途径,而且避免了HCl的浪费,节约了大量的水处理用石灰,具有较高的实用价值、环保价值和经济价值。
[1]赵文斌.电池级液体氯化锌脱除铁和硫酸根的新工艺[J].河南化工,2000,(6):20—21.
[2]张从良,吕斯濠,王 岩.由锌焙砂生产电池用氯化锌的工艺研究[J].无机盐工业,2007,39(7).
[3]HG,T2323--2004.工业氯化锌标准[S].
Abstract:Battery used zinc chloride was produced with residual acid and secondary zinc oxide.First,secondary zinc oxide was used to react with residual acid to prepare impure zinc chloride solution.Then the pure leaching solution was obtained by purifying solution with potassium permanganate,hydrogen peroxide and zinc powder etc.At last,the battery used zinc chloride was made by distilling and concentrating the pure solution.The products are not only suitable for the requirements of battery materials,but also meets the standard of HG/T2332-2004.This process can obtain zinc chloride from cheap raw materials,and solve the problem of residual acid.There⁃fore,it has better practical value.
Key words:residual acid after Ge distilling;secondary zinc oxide;zinc chlorine;battery
Production of battery used zinc chloride with residual acid after Ge distilling
SU Fei
TF813
B
1672-6103(2011)01-0055-03
苏 飞(1975—),男,广东韶关人,大学本科学历,工程师,主要从事有色冶金工艺及有价金属综合回收研究。
2010-09-22
