2%成人AB型血清扩增的骨髓间充质干细胞的分化潜能研究
2011-08-13胡建立赵春华
胡建立 李 健 李 静 马 杰 陈 斌 赵春华*
1(中国医学科学院基础医学研究所,北京协和医学院基础学院,北京 100005)
2(清华大学第一附属医院,北京 100016)
引言
间充质干细胞(mesenchymal ctem cells,MSCs),是一群存在于身体各个组织内具有贴壁能力的多潜能干细胞,具有成骨、成脂肪、成软骨和成肌等的分化能力,具有很强的应用潜能[1-4],研究最多的是具有取材方便、扩增迅速、可自体移植并具有多向分化潜能等特点的骨髓间充质干细胞(bone marrow mesenchymal stem cells,BMSCs)。BMSCs可以稳定和修复造血微环境,促进造血干细胞增殖、分化,调节淋巴细胞免疫功能,减轻移植排斥反应,因此具有重要的临床应用价值。传统的培养方法通常采10%~15%的胎牛血清作为营养支持,但由于临床应用中增加了病毒感染及异种蛋白所致的异基因免疫应答可能及伦理学问题,严重制约了其临床应用。本实验通过研究在与以往不同的培养基中扩增BMSCs的分化潜能,探索一种完全不加动物源性产品的符合临床需要的人BMSCs体外培养体系,为组织工程产品用于临床奠定基础。
1 材料和方法
1.1 材料
Ficoll分离液(比重 1.077 g/mL,Pharmacia 公司),细胞培养液有L-DMEM、IMDM、DF12(GibcoBRL公司);胎牛血清(Hyclone公司);胶原酶、胰蛋白酶、谷氨酰胺(GibcoBRL公司);β-巯基乙醇(Merck公司)、碱性成纤维细胞生长因子(basic fibroblastic growth factor,bFGF;Sigma公司)、内皮细胞生长因子 (vascular endothelial growth factor,VEGF;Sigma公司)、表皮细胞生长因子 (epidermal growth factor,EGF;Gibco公司)、血小板衍生生长因子(platelet-derived growth factor BB,PDGF-BB;Sigma公司)、地塞米松(Sigma公司)、β-甘油磷酸钠(Sigma 公司)、抗坏血酸(Sigma 公司)、1-甲基-3-异丁基-黄嘌呤(Sigma公司)、人凝血酶(上海莱士血制品有限公司),骨髓(解放军307医院)、AB型脐带血浆(北京市脐带血造血干细胞库)、AB型血清(健康志愿者)。所有标本均来自签订知情同意书的捐献者。
1.2 方法
1.2.1 从健康成人全血中制备血清
无菌采集AB型健康志愿者静脉血15 mL,室温静置 30 min,1500 r/min,离心 15 min,将上清10份混匀,56℃水浴箱 30 min,0.22 μm 滤器过滤除菌,8 mL/支分装,-20℃冻存备用。
1.2.2 成人BMSCs分离
无菌采集健康志愿者的骨髓10 mL,用D-Hanks液适当稀释,计数,调整细胞浓度107/mL,离心管内Ficoll和细胞悬液,比例为1∶1,1500 r/min室温离心20 min,无菌吸取白膜层(含单个核细胞),DHanks液洗涤2次,计数。
1.2.3 成人BMSCs培养
单个核细胞以1×106/cm2接种于25 cm2的培养瓶中,培养体系:58%DMEM/F12+40%MCDB-201、2%AB 型成人血清(AS-AB)]、10 ng/mL EGF、10 ng/mL PDGF,1 × 胰岛素-转铁蛋白-亚硒酸、1 ×亚油酸-牛血清白蛋白,50 μmol/L β 巯基乙醇,2 mmol/L L-谷氨酰胺,100 μg/mL青霉素和 100 U/mL硫酸链霉素。37℃、5%CO2、95%湿度的培养箱培养。24 h后,去除悬浮细胞,补充培养基,每3 d换液1次,待细胞长至70% ~80%汇合时,0.125%胰蛋白酶 -0.01%EDTA 消化传代[5-6]。
1.2.4 多向分化潜能
分别取第三代、第七代的BMSCs诱导。
1)成骨分化。BMSCs在含有10-7mol/L地塞米松、10 mmol/L β-磷酸甘油、0.05 mmol/L抗坏血酸和10%FCS的IMDM中诱导培养,每3 d半量换液一次。
2)成骨分化的检测。碱性磷酸酶(alkaline phosphatase,ALP)染色试剂盒染色。具体步骤按照试剂盒操作如下:配制作用液;倾出培养皿中的培养液,PBS洗细胞2次;加固定液2 mL/皿,室温固定1 min,流水漂洗2 min;加作用液2 mL/皿,置湿盒内于37℃孵育2 h,流水冲洗2 min;加5号液2 mL/皿,复染5 min,流水冲洗2 min;70%甘油封固,倒置显微镜下观察,胞浆出现蓝紫色沉淀的为阳性细胞。
3)VonKossa染色。中性甲醛溶液固定1 h,去离子水洗净后,加入2%硝酸银溶液,37℃避光反应10 min,去离子水冲洗后曝光15 min,光镜下观察钙化基质沉淀。对照细胞为在扩增培养基中培养的BMSCs细胞。
4)成脂肪分化。BMSCs在含有10-6mol/L地塞米 松、 0.5 mmol/L 3-isobutyl-1-methylxanthine(IBMX)、0.1 mmol/L抗坏血酸和 10%FCS的 IMDM中诱导培养,每3 d半量换液一次。显微镜下观察脂肪滴的形成。
5)成脂肪分化的检测,油红O染色。细胞以中性甲醛固定10 min后,蒸馏水冲洗;油红O染色工作液作用5 min;明矾苏木素复染细胞核,1 min,蒸馏水冲洗;甘油明胶封片,显微镜下观察并照相。脂滴红染,胞核蓝色。对照细胞为在扩增培养基中培养的BMSCs细胞。
2 结果
2.1 BMSCs的分离培养
原代培养中,在接种后数小时即可见部分细胞贴壁,贴壁细胞开始基本呈圆形。3 d后,贴壁细胞明显增多,并逐渐伸展成为纺锤形。换液弃去未贴壁的细胞,贴壁细胞形态为成纤维样细胞,呈梭形,散在生长,分布不均匀。7 d时,细胞基本贴满培养瓶底部,呈鱼群状、漩涡状、网状或辐射状排列。原代培养9 d左右,非贴壁细胞基本全部去除,贴壁细胞形态较为一致,可进行第1次传代培养。传代培养的BMSCs在形态学上更加趋于一致,为成纤维细胞样细胞,生长旺盛。
2.2 成骨诱导的结果
2.2.1 碱性磷酸酶染色
扩增后不同代次的BMSCs(P3、P7)在成骨诱导体系中培养4~5 d,细胞形态发生明显改变,细胞由原来的成纤维细胞样变为多角形。诱导l周,80%以上的细胞为不规则形;诱导2周,细胞间相互融合。碱性磷酸酶染色显示,阳性细胞(成骨细胞)胞浆内出现沉淀(见图1(b)、(d),箭头所指),而对照组细胞未能出出现阳性(见图1(a)、(c))。在2%的成人AB型血清添加的扩增体系中扩增的BMSCs,第三代、第七代仍然具有很好的成骨分化潜能,可以诱导分化成成骨细胞。
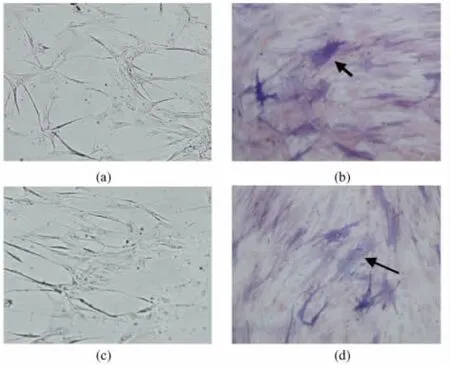
图1 ALP染色结果(40×,箭头所指为阳性)。(a)P3阴性对照;(b)P3第三代;(c)P7阴性对照;(d)P7第七代Fig.1 ALP staining (40 × , arrows indicate the positive).(a)P3 negative control;(b)P3 the third generation;(c)P7 negative control;(d)P7 the seventh generation
2.2.2 Vonkossa染色
扩增后不同代次的BMSCs(P3、P7)经成骨诱导培养3周,Vonkossa银染色后,钙盐沉积区域呈黑色(见图2(b)、(d),箭头所指),而对照组细胞同样染色处理未见明显钙盐沉积(见图2(a)、(c))。在2%的成人AB型血清添加的扩增体系中扩增的BMSCs,第三代、第七代仍然具有很好的成骨分化潜能,可以诱导分化成成骨细胞。

图2 Vonkossa染色(20×,箭头所指为钙基质沉积)。(a)P3阴性对照;(b)P3第三代;(c)P7阴性对照;(d)P7第七代Fig.2 Vonkossa staining (20 × , arrows indicate calcium matrix deposition).(a)P3 negative control;(b)P3 the third generation;(c)P7 negative control;(d)P7 the seventh generation
2.3 成脂诱导
两组不同代次的 BMSCs(P3、P7),在加入脂肪诱导体系后约7 d,少数细胞内就出现微小明亮的脂肪滴。随着诱导时间延长,BMsCs体积变大,呈椭圆形,胞内正常结构消失,呈现空泡结构和大量脂肪油滴。培养至2周,融合的脂肪滴几乎充满整个细胞,油红O染色呈阳性(见图3(b)、(d),箭头所指)。对照级细胞于培养第7 d即铺满瓶底,镜下观察呈成纤维样整齐排列,未发生形态改变,经油红O染色、苏木素复染后,胞浆未见明显脂肪滴(见图3(a)、(c))。实验结果提示:在2%的成人 AB型血清添加的扩增体系中扩增的 BMSCs,第三代、第七代仍然具有很好的成脂分化潜能,可以诱导分化成脂肪细胞。
3 讨论和结论

图3 油红O染色(20×,箭头所指为油红O染色阳性)。(a)P3阴性对照;(b)P3第三代;(c)P7阴性对照;(d)P7第七代Fig.3 Oil red O staining(20 × ,arrows indicate the positive of oil red O staining).(a)P3 negative control;(b)P3 the third generation;(c)P7 negative control;(d)P7 the seventh generation
随着干细胞工程及其相关生物技术研究的发展,以及对干细胞本身特性的认识,使得研究者在体外培养人BMSCs、体外定向诱导分化为所需的不同细胞成为可能。BMSCs作为干细胞,具有多向分化潜能、自我更新特点,具有独特的来源以及简便的分离培养方法,被认为是有临床应用价值的组织工程种子细胞。BMSCs与其他干细胞相比,具有显著的优越性:第一,骨髓易于获得,在同一个体可多次抽取;第二,具有多向分化潜能,体外易于分离纯化、增殖;第三,可进行自体移植,避免了伦理道德和免疫排斥的困扰。
目前,针对体外扩增人BMSCs的传统方法主要是应用10%~15%的胎牛血清作为主要的血清添加,但是异种或异体蛋白对人体细胞的负面影响阻碍了其扩增产品、组织工程产品的临床推进。
近年来,针对体外扩增人的BMSCs培养基的血清替代品,所进行的研究已经很多。本小组已系统地比较了在2%的AB型健康成人血清、脐带血清、胎牛血清所制得的培养基中BMSCs的生长特性[7],证实了2%的AB型健康成人血清可以代替胎牛血清在体外有效地扩增BMSCs。在本试验中,继续研究2%成人AB型血清配制的培养基中BMSCs的分化潜能。
Friedenstein的实验发现,通常情况下10%人血清的生长状况好于10% 胎牛血清的生长状况。Anselme等、Yamamoto等和Spees等认为,人血清与胎牛血清相当[8-10]。Oreffo et al等认为,在培养的产物中,人血清在诱导成骨、成脂方面优于胎牛,而Yamamoto等报道成骨能力方面二者类似,Anselme等在无胎牛血清的扩增培养体系中加入15%的AB血清或自体血浆[8]。Mizuno等认为,扩增BMSCs人的自体血清要远优于胎牛血清[11]。有结果显示,适度低血清用量有利于细胞生长[12]。本实验中采取的是只添加了2%的人源化AB型血清,通过观察第三、第七代次的 BMSCs的分化潜能,发现仍然具有很好的成骨成脂潜能。实验说明,在该配方中,2%的血清添加就达到了与以往10%~15%的血清添加的相同效果,可以消除以动物源性的血清(如胎牛血清)或蛋白为添加因子、外源性蛋白被细胞内化而引起的许多潜在问题,如病毒、朊病毒的感染免疫排斥反应[13]。
本研究显示,培养基中以2%的成人AB型血清添加扩增 BMSCs,至少能和胎牛血清是一样的效果,证实获得的 BMSCs保持有分化潜能,确实可以向成骨、成脂方向成功分化。在不改变扩增效率的情况下,通过降低培养基中血清的浓度,大大降低了扩增成本。
有关培养基的进一步优化尚待更进一步研究,以期为找到一种可以很好替代胎牛血清用于有效扩增并达到临床治疗用量的细胞产品的血清[14],实现扩增体系的完全人源化。
BMSCs高度的自我更新能力和强大的可塑性以及取材方便、低免疫原性,使其成为组织工程中理想的种子细胞。许多研究者以其为种子细胞,在骨、软骨、肌腱损伤的修复方面做了较深入的研究,如关节软骨修复的促进、骨损伤的修复等都取得了可喜的成果,预示着BMSCs在组织工程方面巨大的应用价值。骨髓间充质干细胞有望作为种子细胞与支架材料,在复合之后移植到创伤部位修复骨缺损[15],具有作为软骨组织工程种子细胞来源的可能[16]。有学者将骨髓间充质干细胞直接注射到梗死区或经静脉注射后,在损伤区均能见到骨髓间充质干细胞,并分化成为心肌细胞,使心功能得到明显改善,还能预防有害的重构[17-18]。研究表明,在适当的条件下,人骨髓间充质干细胞能向神经元和神经胶质细胞等分化,可以在体外经过扩增诱导后作为神经细胞移植的供体,为神经系统疾病的治疗开辟一条新的途径[9]。
总之,BMSCs作为一种在组织工程中有着广阔应用前景的干细胞,其实验研究如火如荼,其中包括培养条件、定向分化等研究,目前国内外已有部分实验室和医疗机构在进行小规模的临床实际应用的论证。相信在前期基础研究准备完善后,大规模临床应用就要到来,希望本研究对此有一定的帮助。
[1]Pittenger MF, Mackay AM,Beck SC,et al. Multilineage potential of adult human mesenchymal stem cells[J].Science,1999,284(5411):143-147.
[2]Deans RJ,Moseley AB.Mesenchymal stem cells:biology and potential clinical uses[J].Exp Hematol,2000,28(8):875-884.
[3]Prins HJ,Rozemuller H,Vonk-Griffioen S,et al.Bone-forming capacity of mesenchymal stromal cells when cultured in the presence of human platelet lysate as substitute for fetal bovine serum[J].Tissue Eng Part A.2009,15(12):3741-3751.
[4]Jiang Y,Jahagirdar BN,Reinhardt RL,et al.Pluripoteney of mesenchymal stem cells derived from adult marrow[J].Nature,2002,418(6893):41-49.
[5]Guo H, Fang B, Zhao RC, et al. Hemangioblastic characteristics of fetal bone marrow-derived Flk1+CD31-CD34-cells[J].Exp Hematol,2003,31:650-658.
[6]Reyes M,Lund T,Lenvik T,et al.Purification and ex vivo expansion of postnatal human marrow mesodermal progenitor cells[J].Blood,2001,98:2615-2625.
[7]胡建立,李静,陈斌,等 成人 AB型血清取代胎牛血清在体外有效扩增骨髓间充质干细胞[J].基础医学与临床,2010,30(6):576-581.
[8]Anselme K,Broux O,Noel B,et al.In vitro control of human bone marrow stromal cells for bone tissue engineering[J].Tissue Eng,2002,8:941-953.
[9]Yamamoto N,Isobe M,Negishi A,et al.Effects of autologous serum on osteoblastic differentiation in human bone marrow cells[J].J Med Dent Sci,2003,50:63-69.
[10]Spees JL,Gregory CA,Singh H,et al.Internalized antigens must be removed to prepare hypoimmunogenic mesenchymal stem cells for cell and gene therapy[J].Mol Ther,.2004,9:747-756.
[11]Mizuno N,Shiba H,Ozeki Y,et al.Human autologous serum obtained using a completely closed bag system as a substitute for fetal calf serum in human mesenchymal stem cell cultures[J].Cell Biol Int,2006,30:521 e4.
[12]Montzka K,Führmann T,Wöltje M,et al.Expansion of human bone marrow-derived mesenchymal stromal cells:serum-reduced medium is better than conventional medium[J].Cytotherapy,2010,12(5):587-592.
[13]Spees JL,Gregory CA,Singh H,et al.Internalized antigens must be removed to prepare hypoimmunogenic mesenchymal stem cells for cell and gene therapy[J].Mol Ther,2004,9:747-756.
[14]Sensebé L,Krampera M,Schrezenmeier H,Mesenchymal stem cells for clinical application[J].Vox Sang,2010,98(2):93-107.
[15]Ouyang HW,Cao T,Zou XH,et al.Mesenchymal stem cell sheets revitalize nonviable dense grafts:implications for repair of largebone and tendon defects[J].Transplant,2006,82(2):170-174.
[16]舒朝锋,崔磊,刘伟,等.人骨髓间充质干细胞向软骨细胞诱导分化的实验研究[J].中华创伤骨科杂志,2004,6(2):194-198.
[17]Pittenger MF,Martin BJ.Mesenchymal stem cells and their potential as cardiac therapeutics[J].Circ Bes,2004,95(1):9-20.
[18]Wang FS,Treater C.Bone marrow cells and myocardial regeneration[J].Int J Hematol,2004,79(4):322-327.
[19]Long X,OlszewskiM,Huang W,et al.Neural cell differentiation in vitro from adult human bone marrow mesenchymal stem cells[J].Stem CellsDev,2005,14(1):65-69.
