AB型离子晶体结构的几何因素
2019-09-09姚远石小倩杨旭东
姚远 石小倩 杨旭东


摘要: 以AB型离子晶体为例,阐释以正离子为中心,构建不同结构晶体的原因;从数学上提出统一公式,导出几种典型的等价型临界正、负离子半径比,由此得出正、负离子半径比是决定离子晶体结构的重要因素,同时提及离子间的极化作用也可对晶体结构产生影响。
关键词: AB型; 离子晶体结构; 正、负离子半径比
文章编号: 10056629(2019)7008204中图分类号: G633.8文献标识码: B
1 问题的提出
人教版选修3《物质结构与性质》第79页指出:“……NaCl和CsCl是两种不同类型的晶体结构。晶体中正负离子的半径比r+r-是决定离子晶体的重要因素,简称几何因素。”为什么晶体中正、负离子的半径比是决定离子晶体结构的重要因素呢?除电荷因素外,为什么教材中又提到还取决于离子键的纯粹程度(简称键性因素)呢?
2 结构分析
2.1 正离子为中心
配位多面体是以正离子为中心的多面体,一般不使用以负离子为中心的配位多面体[1]。例如
在氯化钠结构中,Na+和Cl-的配位数都是6,将Cl-周围的6个Na+的中心连结起来,其实也可以得到与以Na+为中心相似的正八面体。应该说,作为离子晶体的一个基本特征,它确实具有正、负离子在空间上相间的分布,即每个正离子周围邻接若干个负离子,而每个负离子周围邻接若干个正离子。但由于正、负离子在电价和半径上的差异以及正离子种类多而负离子种类少,因此它们在晶体结构中“扮演”了不同的“角色”。
一般正离子因其半径相对较小并可能呈现高价而产生较强的电位,易吸引负离子,使之在形成配位多面体中占主导地位,而负离子(如O2-、 OH-、 F-)因其半径大、电价低,占据空间大,在形成密堆积中起主导作用。若在大半径的负离子周围接触并排满多个正离子,则势必会造成配位的小半径、高电荷正离子之间有较强的互斥作用,从而使体系能量上升。如Cl-的半径是1.81,若仅考虑其圆周长应是11.4,即可容纳6个半径为0.95的Na+;若考虑Cl-的球面,从几何上可容纳更多的Na+,则相斥作用会更强。总之,低价、大半径配位负离子之间的排斥作用远较高价、小半径的正离子之间的排斥作用为小,对晶体的构建有利。
若从低价Na+过渡为半径更小、电价更高的正离子,如Be2+(半径0.31)、Al3+(半径0.50)、Si4+(半径0.41)等,则正离子在组织配位多面体中的主导作用将更加突出。
另外,在NaCl晶体中,Cl-配位数为6与Na+配位数为6相比较,是有质的差别的。因为前者实际上是被动的,是以Na+为中心按半径比选择配位数为6,以及二元离子晶体中配位数之比与组成之比成反比的晶体化学规律共同制约而导致的结果。
负离子配位数正离子配位数=C.N.-C.N.+=正离子数负离子数
C.N.+、 C.N.-分别表示正、负离子的配位数,因C.N.+=6和正负离子数量比为1∶1,则必有C.N.-=6×(1÷1)=6。
2.2 晶体的构建
以正离子为中心,晶体中的离子排列[2]总是希望正、负离子互相接触,正离子周围的负离子互不接触,配位数尽量高,这样引力大、斥力小、排列紧密、规整,势能低。由此形成的三维空间体系能量最低、最稳定。显然,正离子半径越大,或负离子半径越小,则配位数C.N.也就愈高,即C.N.不同,导致晶体种类繁多,结构多样。
现取正、负离子及负、负离子都互相接触的等价型临界情况加以讨论。
3 统一公式的导出及半径比推算
3.1 统一公式的导出
正离子与两个相同的负离子相接触的关系的一个截面图[3]如图1所示。
必须指出,在任何类型的离子晶体中都存在着这样的关系,只不过是在不同类型晶体中,离子的堆积方式不同,而使得连线间的夹角不同而已。图中中心为O的圆是正离子的截面,其半径为r+、中心为C和D的圆是相同的负离子的截面,半径为r-,显然有下列关系:
①、②、③式均为AB型离子晶体中离子半径比r+r-统一的计算公式,并且是等效的。在前文所述等价型临界情况下,只要以其结构推知相切的离子中心间连线间之夹角θ值或α值,并代入①式或②式或③式,就可算出相应的正、负离子半径比。
3.2 半径比的推算及分析
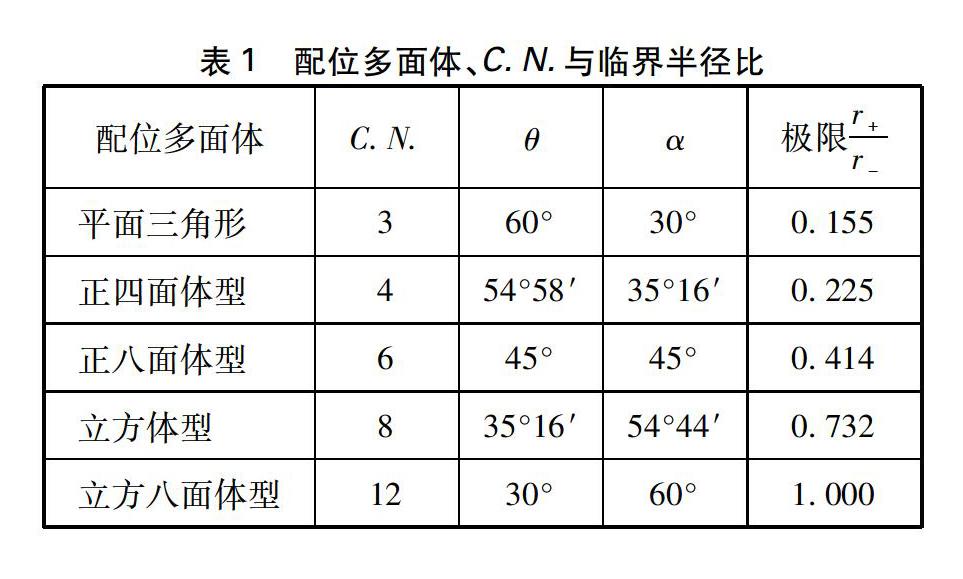
配位多面体确定之后,配位数C.N.就是多面体角顶数,①、 ②、 ③式中的θ、 α值可由简单的立体几何知识得到,见表1。
当r+r->0.225时,则正、负离子互相接触,而负离子之间互不接触,这样比较稳定,即C.N.=4的必要条件是r+r-≥0.225,此時,正离子周围尚可再容纳负离子,达到正负离子都互相接触的临界情况,是为C.N.=6的NaCl型;
当r+r-<0.225时,只有负、负离子相互接触,正离子处于负离子的空隙之中,不能与负离子充分接触,这样由于静电引力不足以与静电斥力相抗衡,晶体变得不稳定。显然,负离子减少,即负离子配位数C.N.由4减少到3或2,可消除这种影响,是C.N.=3的正三角形结构或C.N.=2直线型结构,此不满足三维空间结构[4],不讨论。依次类推:
4 键性因素
应用半径比规则,对AB型简单离子化合物的配位数和结构预测是正确的。但由于规则把离子间看成刚性的“小球”接触,当含有复杂离子,又有双晶现象以及负离子较大,易被正离子极化时,半径比规则就可能失效,其准确性很差。如CO2-3离子,由于不同方式配位,可以方解石和霞石两种矿石存在[6];又如CuI, r+r-=96216=0.44,按半径比规则属于NaCl型结构,但由于Cu+是18e-结构,有较强极化力,而I-半径又大,有较大变形性,离子间相互极化作用,使核间距缩短,由典型离子晶体转变为共价性很大的晶体,这是键性因素的改变导致晶格配位数降低,晶体类型由NaCl型转变成ZnS型。
再如鹵化银,由于AgI晶体内离子间的极化作用比AgCl、 AgBr要强得多,Ag+和I-核间距离大为缩短了,按离子半径之和应是(126+216)pm=342pm,实验测定却是299pm,缩短了43pm。离子间距离的缩短,也减小了晶体的配位数,如AgI的离子半径比r+r-约为0.58,按半径比规则应属于配位数为6的NaCl型晶体,实际上AgI晶体却属于配位数为4的ZnS型。其原因也是在于Ag+和I-之间有显著的极化作用。极化作用使Ag+部分地钻入I-的电子云中,犹如减小了离子半径之比r+r-,使之不再等于正、负离子未极化时的比值0.58,而减小到小于0.414。由于极化而改变晶型、减小配位数的现象是很普遍的(见表3)。
5 结语
值得一提的是,离子半径数据有多种[8],如Goldschmidt离子半径、Pauling离子半径、Shannon有效离子半径、热化学半径等。这些离子的半径值本身也并不是非常精确的数据。我们在进行计算和比较时,宜采用同一组数据,则相对准确。本文采用的是Pauling离子半径数据。
参考文献:
[1]邵美成. 鲍林规则与键价理论[M]. 北京: 高等教育出版社, 1993: 3~5.
[2]张淑民. 基础无机化学(上册)(第四版)[M]. 兰州: 兰州大学出版社, 65.
[3]王万林. 简单离子晶体半径比的计算[J]. 张家口师专学报, 2003, (3): 20~22.
[4][英]R. B. 海斯洛普著. 温元凯译. 戴安邦校. 无机化学中的定量关系[M]. 北京: 人民教育出版社, 1979: 93.
[5]Weller Overton Rourke Armstrong著. 李珺, 雷依波, 刘斌, 王文渊, 曾凡龙等译. 无机化学(第6版)[M]. 北京: 高等教育出版社, 2018: 96.
[6]尹钦林. 无机化学规则导论[M]. 杭州: 浙江大学出版社, 2002: 112.
[7]史轶漪, 邹宗柏. 普通化学解疑[M]. 南京: 江苏科学技术出版社, 1987: 154~155.
[8]袁万钟, 隋亮. 无机化学教学笔谈[M]. 北京: 高等教育出版社, 1991: 89~92.
