室内质量控制在EMIT法监测他克莫司血药浓度中的应用
2011-08-07蒋艳邹素兰夏宗玲苏州大学附属第三医院江苏常州市第一人民医院药剂科常州市213003
蒋艳,邹素兰,夏宗玲(苏州大学附属第三医院/江苏常州市第一人民医院药剂科,常州市213003)
室内质量控制(Indoor quality control,IQC)是由实验室的工作人员采用一系列统计学的方法,连续地评价本实验室测定工作的可靠程度,判断检验报告是否可发出的过程。IQC常用质控图控制质量。起初,质控图应用于生产制造业,目前已推广到更广泛的领域,如实验室开展治疗药物监测(Therapeutic drug monitoring,TDM)的质量控制,可较直观地对监测质量进行控制,尽快发现问题并及时纠正[1,2]。我院自2009年引进药物浓度分析仪Viva-E,该仪器是一种采用酶放大免疫分析技术(Enzyme multiplied immunoassay technique,EMIT)的仪器。为了提高该法在本实验室条件下监测他克莫司(FK506)血药浓度的质量,笔者对FK506血药浓度监测过程中的质控品的实测值绘制质控图,进行回顾性质量控制。
1 仪器与试药
1.1 仪器
Viva-E药物浓度分析仪(德国Dade Behring公司):微量加样器、5417R高速冷冻离心机(德国Eppendorf公司);Vortex-Genie涡旋振荡器(美国Vortex公司);低温冰箱(日本Sanyo公司)。
1.2 试药
FK506检测试剂盒,包括:(1)抗体试剂(含抗FK506鼠单克隆抗体、烟酰胺腺嘌呤二核苷酸、葡萄糖-6-磷酸盐、氯化钠、牛血清白蛋白、表面活性剂和防腐剂),(2)缓冲试剂(含三羟甲基氨基甲烷缓冲液、牛血清白蛋白、表面活性剂和防腐剂),(3)酶试剂(含细菌的葡萄糖-6-磷酸脱氢酶标记的FK506、磷酸缓冲液、牛血清白蛋白和防腐剂),(4)FK506定标液、FK506样本前处理液、FK506质控品等,以上试剂均为西门子医学诊断产品有限公司提供;甲醇为色谱纯。
2 方法
2.1 质控品的测定方法
在监测临床患者样本的同时,随行测定FK506的质控品。取出在-28℃保存的质控品,放至室温,于离心管中分别加入甲醇200 μL和FK506样本前处理液50 μL,于振荡器上快速振荡,充分混匀,14000 r·min-1离心5 min。离心结束后,倾倒离心管内上清液于样品管中,上机检测。
2.2 温度影响因素试验
日常监测过程中,对温度的要求是与定标准曲线(以下简称定标)时的温度保持一致。为考察温度对测定值的影响程度,作如下试验:取低、中、高浓度(简称L、M、H)质控品各5份,按“2.1”项下方法操作,分别在21、22、23、24、25℃5个温度下各测定浓度5次,其中23℃为定标时的温度。监测数据结果采用双侧配对t检验进行分析。
2.3 判定标准
质控品为已有靶值的全血样品,按说明书要求,L、M、H质控品的靶值及允许误差范围分别为4.3 ng·mL-1(2.1~6.5 ng·mL-1)、8.9 ng·mL-1(5.3~12.5 ng·mL-1)、18.0 ng·mL-1(14.0~22.0 ng·mL-1)。实测值在允许误差范围内,判定为“合格”;反之则为“不合格”,判定为“失控”,需重新定标,再次监测质控,至3浓度(水平)质控实测值均在允许误差范围内为止。
2.4 质控图的绘制
在Excel表中建立1个以“FK506质控图”的文档,在文档中输入日期、质控值,利用Excel的自动计算功能,分别求出L、M、H质控品实测值的平均值(x)、标准偏差(s)、相对标准偏差(RSD)、几倍标准偏差[3]。利用Excel的自动作图功能,以“测定次数”为横坐标,以“浓度”为纵坐标,绘制FK506实测值质控图。
3 结果
3.1 温度影响因素试验结果
监测结果见表1。
表1 不同温度下3水平质控品的实测浓度结果(±s,n=5)Tab 1Concentration determination of three level quality control under different temperature(s±s,n=5)
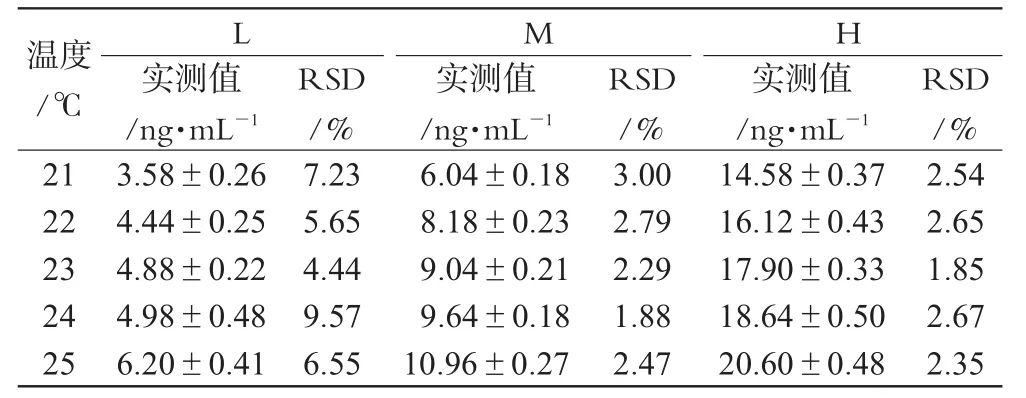
表1 不同温度下3水平质控品的实测浓度结果(±s,n=5)Tab 1Concentration determination of three level quality control under different temperature(s±s,n=5)
统计学结果表明:L质控品在温差2℃时,测定结果与定标温度(23℃)时的测定结果之间差异具有显著统计学意义(P<0.001);在温差1℃时,与定标温度的测定结果之间差异无统计学意义(P>0.05)。M、H质控品在温差1℃和2℃时,测定结果与定标温度时的测定结果之间差异均有统计学意义(P<0.05)。由此可见,测定温度对结果的影响显著,且温差越大,测定结果之间的差异就越显著。
温度/℃2122232425 L M H实测值/ng·mL-1 3.58±0.264.44±0.254.88±0.224.98±0.486.20±0.41 RSD/%7.235.654.449.576.55实测值/ng·mL-1 6.04±0.188.18±0.239.04±0.219.64±0.1810.96±0.27 RSD/%3.002.792.291.882.47实测值/ng·mL-1 14.58±0.3716.12±0.4317.90±0.3318.64±0.5020.60±0.48 RSD/%2.542.651.852.672.35
3.2 质控品的监测结果
共测定FK506质控品255个,其中L、M、H质控品各85个,L、M、H质控品实测值的±s分别为(5.2±1.2)ng·mL-1、(9.4±1.4)ng·mL-1、(18.3±2.3)ng·mL-1,RSD分别为22.6%、14.5%和12.8%。本实验室条件下测得的质控品平均值与靶值较为接近,3水平质控品的RSD值均小于质控品说明书允许的误差范围,说明室内质量控制良好。
3.3 3水平质控品的质控图
3.3.1 L质控品实测值范围为2.5~8.0 ng·mL-1,其中第13、26、36、48、49、52、59、69、81点“失控”,超出质控品允许误差范围上限,结果见图1A。
3.3.2 M质控品实测值范围为6.6~12.7 ng·mL-1,其中第81点“失控”,超出质控品允许误差范围上限,结果见图1B。
3.3.3 H质控品实测值范围为14.0~24.1 ng·mL-1,其中第5、17、37、49、59点“失控”,超出质控品允许误差范围上限,结果见图1C。
4 讨论
在FK506质控品的监测过程中,笔者发现温度对试验结果影响较大。以L质控品为例,第13、28、34、52、69点实测值偏离靶值较远,查阅试验记录后发现,温度控制不理想,与定标时的温度相差较大,重新调整温度后监测结果满意。同时进行的温度因素影响试验更好地验证了温度对测定值有显著影响。因此,监测时实验室里的温度应尽量控制在恒温,温差不能太大,且操作时的温度与定标时的温度要保持一致。
有资料[4]显示,应用EMIT法监测血药浓度时,会发生“试剂瓶底效应”(Bottom of the reagent bottle effect)影响试验结果,即测定时若试剂盒内剩余少量试剂时,此时用于测定样品,则得到的结果会明显偏高。本试验过程中也发现了这一现象,以M质控品为例,第16、26、37、48、49、59、72、81点质控品的实测值偏高,这些点正是每批试剂盒即将用完、剩余试剂量偏少的时候出现的;当更换新的试剂盒后,结果偏高的现象消失。所以试剂盒在长时间反复使用后,需要及时更换新的试剂盒,以防测定结果的漂移,从而保证结果的准确性。
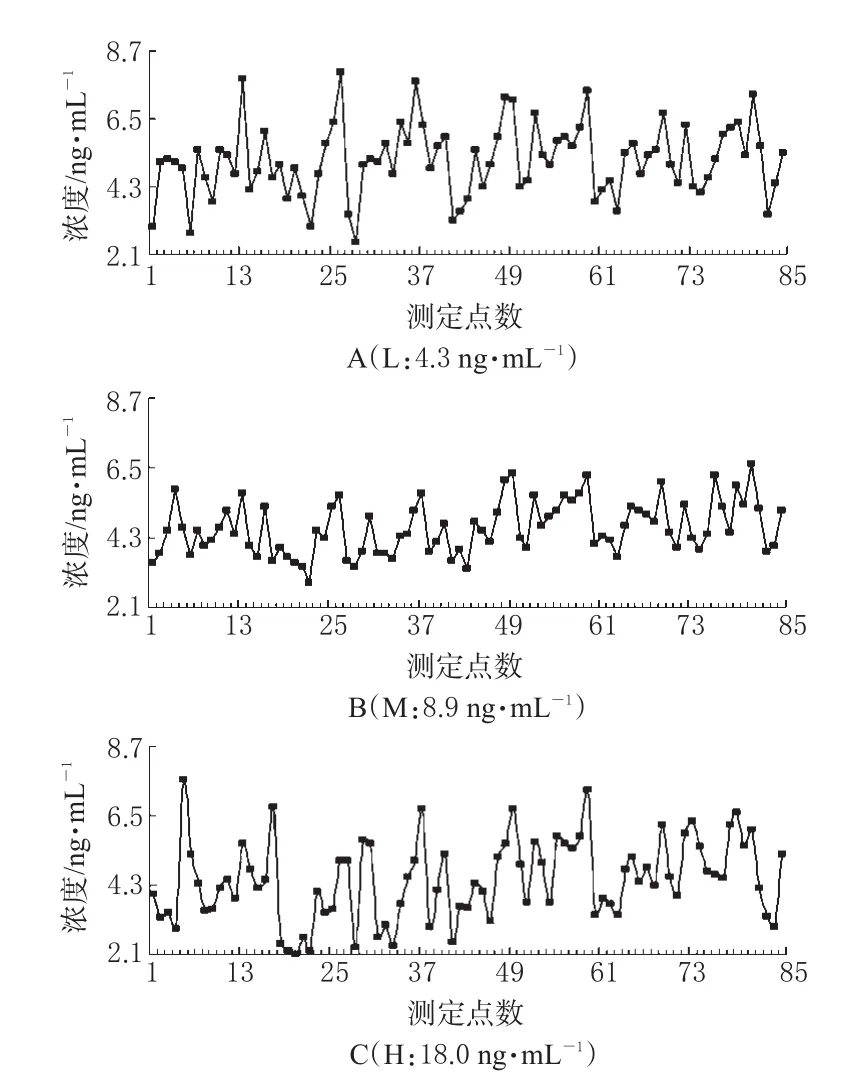
图1 3水平质控图Fig 1Quality control graph of three level quality control
此外,通过对质控图的回顾性质量分析,笔者发现L、H质控品较M质控品相对难控制,质控曲线容易发生飘移,“失控”次数较多,分析原因与定标曲线有关。定标曲线是以浓度为横坐标、吸光度值为纵坐标拟合而成,L、H质控品的靶值及允许误差范围正好落在标准曲线趋势相对平缓的地方,M质控品则在曲线趋势变化较大的地方,所以相同的吸光度值变化,前者会比后者有更大的浓度值变化。
通过对质控图的分析来寻找误差规律和失控时查找原因,均需要对有关情况进行详细记录才能顺利进行。因此,需养成良好的实验记录习惯,对试剂批号、定标的日期和实验室环境、仪器的校正及故障、测定过程中的异常现象等均应详细记录。
因此,在实验室进行TDM的同时进行IQC,能及时发现各种测定误差。通过分析找出引起误差的原因,及时纠正,以确保实验室的工作质量,为参与室间质控打下良好基础[5]。同时,精确的监测结果才能为开展个体化药学服务、提高临床合理用药水平提供可靠的依据。
综上所述,IQC对于应用EMIT法监测FK506的血药浓度很重要,可及时预防并纠正各类误差,提高监测结果的精确性,从而对监测结果作出更精确的判断。
[1]蔡和平,王卓,徐慧欣,等.质控图分析及其在环孢素治疗药物监测中的应用[J].世界临床药物,2009,30(10):612.
[2]李金恒.临床治疗药物监测的方法和应用[M].北京:人民卫生出版社,2009:145.
[3]黄永庆.应用Excel制作自动室内质控图[J].浙江预防医学,2008,20(4):94.
[4]张君仁,臧恒昌.体内药物分析[M].北京:化学工业出版社,2002:92.
[5]杨炳所,唐薇,史建琼,等.治疗药物监测的质量控制[J].中国药房,2003,14(5):287.
