花生壳吸附Cr(Ⅵ)过程中扩散方程的研究
2011-07-25张庆芳胡显峰贾小宁孔秀琴
张庆芳,胡显峰,贾小宁,孔秀琴
(兰州理工大学石油化工学院,甘肃 兰州 730050)
数学模型对预测吸附行为、优化吸附过程是十分重要的,因此,建立适当的数学模型是开展生物质吸附剂吸附重金属离子研究的重要内容之一。
研究表明,花生壳占花生质量的2.6%~36.0%,其中含粗纤维65.7%~79.3%、粗蛋白4.8%~7.2%、粗脂肪1.2%~2.8%、无氮浸出物10.6%~21.2%[1]。纤维素是由上千个单糖以1,4-糖苷键相连形成的高聚体,每个单糖有3个醇羟基,醇羟基的氢原子具有活泼性,因而具有脱除重金属离子的能力,某些纤维素还具有螯合金属离子的作用。同时,花生壳中的单宁类化合物,是极为有效的离子交换物质,容易与重金属离子发生置换反应,以达到吸附重金属离子的目的[2]。因此,花生壳是有效的重金属离子吸附剂。
作者在此进行了花生壳吸附Cr(Ⅵ)过程中扩散方程的研究。
1 吸附动力学理论
1.1 吸附机理
多孔吸附剂的吸附过程,一般认为由“串联”的三个连续步骤完成,包括颗粒外扩散(又称为膜扩散)阶段、颗粒内扩散阶段、吸附反应阶段。吸附过程的总速率取决于其中最慢的步骤(即速率控制步骤)。一般而言,吸附反应速度很快,可迅速在微孔表面各点上建立吸附平衡。因此,总的吸附速率由颗粒外扩散或颗粒内扩散控制,分为以下三种情况:颗粒外扩散>颗粒内扩散;颗粒外扩散<颗粒内扩散;颗粒外扩散≈颗粒内扩散。对于前两种情况,吸附速率分别由颗粒外扩散或颗粒内扩散控制。通常情况下,颗粒内扩散控制整个吸附过程的条件是:混合效果良好、吸附质浓度高、颗粒粒径大、吸附质和吸附剂之间的亲和力差;反之,吸附过程则由颗粒外扩散控制。
1.2 颗粒内扩散方程
假设颗粒外扩散可以忽略并且颗粒内扩散是唯一的速率控制步骤,那么颗粒内扩散模型[3~5]可表示为:
qt=kidt0.5
(1)
式中:kid为颗粒内扩散速率常数,mg·g-1·min-0.5;qt为t时刻的吸附量,mg·g-1;t为吸附时间,min。
2 实验
2.1 材料与试剂
花生壳,市售。经粉碎过筛后选出粒径为0.25~0.50 mm的颗粒,用去离子水浸泡24 h,去除悬浮细小物质和可溶性物质,在80℃下烘干后放入干燥器中备用。
重铬酸钾(K2Cr2O7),优级纯。
2.2 改性花生壳的制备[6]
称取50 g花生壳置于2.5 L的大烧杯中,加入500 mL 1 mol·L-1磷酸溶液,搅拌1 h,离心,取沉淀,在50℃下烘干,然后升温至180℃加热1.5 h。用75℃的去离子水清洗(去除游离的磷酸),于50℃下烘干备用。
2.3 Cr(Ⅵ)溶液的配制
(1)铬标准储备液的配制:称取于120℃干燥2 h的K2Cr2O70.2829 g,加水溶解,移入1000 mL容量瓶中,用水稀释至刻度,摇匀。即得Cr(Ⅵ)浓度为100 mg·L-1的铬标准储备液。
(2)铬标准溶液的配制:吸取5.00 mL铬标准储备液,置于500 mL容量瓶中,用水稀释至刻度,摇匀。即得Cr(Ⅵ)浓度为1.00 mg·L-1的铬标准溶液。此溶液作为铬标准曲线使用液。
(3)铬实验储备液的配制:称取于120℃干燥2 h的K2Cr2O72.8287 g,加水溶解,移入1000 mL容量瓶中,用水稀释至刻度,摇匀。即得Cr(Ⅵ)浓度为1000 mg·L-1的铬实验储备液。实验所用到的Cr(Ⅵ)溶液在此基础上稀释。
2.4 Cr(Ⅵ)吸附实验
称取一定量的花生壳放入150 mL碘量瓶中,加入50 mL已知浓度的Cr(Ⅵ)溶液,用0.10 mol·L-1HNO3或NaOH调节溶液的pH值,然后将碘量瓶置于水浴恒温振荡器中,于140 r·min-1进行振荡,在一定的温度下吸附一定时间,经定量滤纸过滤,依据二苯磺酰二肼分光光度法[7],用紫外可见分光光度计测定Cr(Ⅵ)浓度。Cr(Ⅵ)的吸附量(q)和吸附率(Re)依下式计算。
(2)
(3)
式中:c0为吸附前Cr(Ⅵ)的浓度,mg·L-1;ce为吸附平衡时Cr(Ⅵ)的浓度,mg·L-1;V为吸附溶液的体积,mL;m为吸附剂的质量,g。
2.5 扩散实验
称取1.0 g花生壳放入50 mL浓度分别为50 mg·L-1、75 mg·L-1、100 mg·L-1、125 mg·L-1、150 mg·L-1的Cr(Ⅵ)溶液中,用0.10 mol·L-1HNO3或NaOH调节溶液的pH值为2.0,控制温度为30℃、振荡速率为140 r·min-1,吸附不同时间(10 min、30 min、60 min、120 min、180 min、240 min、300 min、360 min、420 min),过滤,测定滤液的Cr(Ⅵ)浓度。
3 结果与讨论
3.1 Cr(Ⅵ)标准曲线
测定不同浓度铬标准溶液的吸光度,绘制Cr(Ⅵ)的标准曲线,如图1所示。拟合线性回归方程为:y=0.015x+0.0314,线性相关系数R2=0.9998。实验过程中通过测定溶液的吸光度来计算吸附前后溶液中Cr(Ⅵ)的浓度。
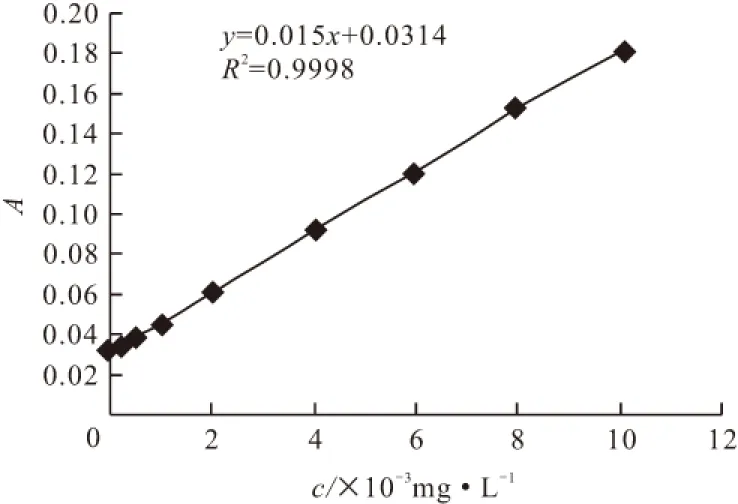
图1 铬(Ⅵ)标准曲线
3.2 颗粒内扩散方程
不同初始浓度Cr(Ⅵ)溶液吸附率随时间的变化曲线见图2。

图2 不同初始浓度Cr(Ⅵ)溶液的Cr(Ⅵ)吸附率随时间的变化曲线
由图2可以看出,180 min之前吸附迅速,之后吸附逐渐变缓。可以认为吸附过程分为两步:第一步是180 min前的颗粒外扩散,Cr(Ⅵ)从溶液迅速扩散到花生壳外表面;第二步是180 min后的颗粒内扩散,Cr(Ⅵ)向花生壳内层毛孔扩散。如果控速步骤由颗粒内扩散决定,那么以qt对t0.5作图应该呈线性关系。据颗粒内扩散方程(1)对图2中180 min后的数据进行处理,结果见图3,拟合参数见表1。
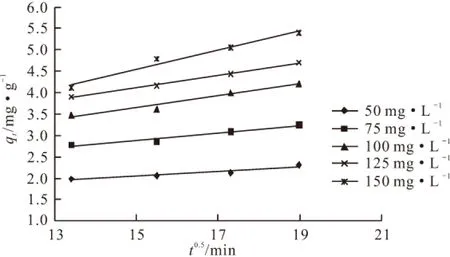
图3 不同初始浓度下,花生壳吸附Cr(Ⅵ)的qt~t0.5曲线
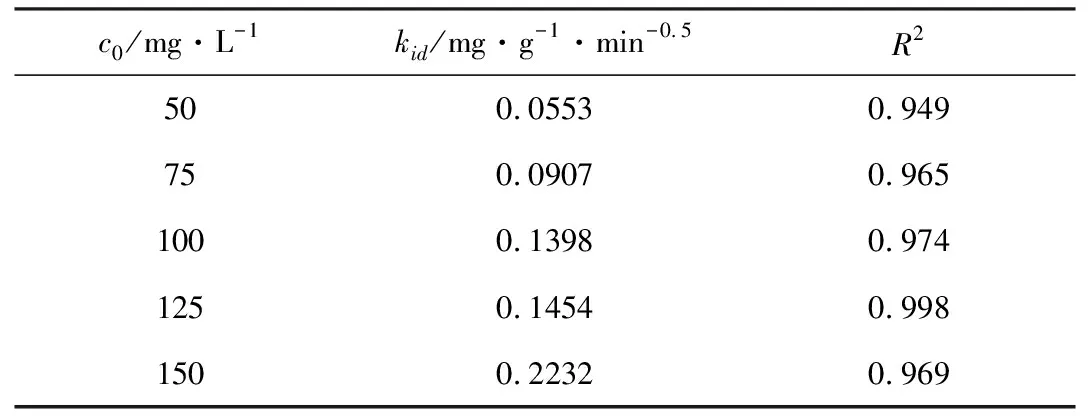
表1 颗粒内扩散方程拟合参数
由图3和表1可看出,花生壳吸附Cr(Ⅵ)的颗粒内扩散方程拟合结果的线性关系较好,说明180 min后吸附过程受颗粒内扩散控制。由此判断,180 min前吸附过程受颗粒外扩散控制,180 min后吸附过程受颗粒内扩散控制。由于图1中的直线均不过原点,表明颗粒内扩散并不是唯一的反应速率控制步骤,反应中同时发生的其它步骤都有可能控制反应速率[8]。
4 结论
在花生壳用量为1.0 g、pH值为2.0、温度为30℃、振荡速率为140 r·min-1的条件下,研究了不同初始浓度Cr(Ⅵ)溶液中Cr(Ⅵ)的吸附率随时间的变化情况。经颗粒内扩散方程验证,可以认为吸附过程在180 min前受颗粒外扩散控制,180 min后受颗粒内扩散控制,但颗粒内扩散并不是唯一的反应速率控制步骤,反应中同时发生的其它步骤都有可能控制反应速率。
(致谢:感谢2010年度国家大学生创新实验课题组的大力支持!)
[1] 杨性坤,钟黎,井强山.浅谈花生壳的综合开发利用[J].信阳师范学院学报(自然科学版),1998,11(2):188-192.
[2] 洪礼法,郭玮伟,许春凤.提取黄色素后的花生壳在重金属废水处理中的应用[J].苏州科技学院学报(工程技术版),2003,16(1):44-48.
[3] Lazaridis N K,Karapantsios T D,Georgantas D.Kinetic analysis for the removal of a reactive dye from aqueous solution onto hydrotalcite by adsorption[J]. Water Research,2003,37(12):3023-3033.
[4] Venkata Mohana S,Chandrasekhar Rao N,Karthikeyan J.Adsorptive removal of direct azo dye from aqueous phase onto coal based sorbents:A kinetic and mechanistic study[J].Journal of Hazardous Materials,2002,90(2):189-204.
[5] Fukuda Toshihiro,Aramata Akiko. The kinetic study of specific adsorption of phosphate species on Pt (Ⅲ)in acidic solutions[J]. Journal of Electroanalytical Chemistry,1997,440(1-2):153-162.
[6] 章明奎,方利平.利用非活体生物质去除废水中重金属的研究[J].生态环境,2006,15(5):897-900.
[7] 国家环境保护局.水和废水监测分析方法(第四版)[M].北京:中国环境科学出版社,2002:344-349.
[8] Yeddou Nacera,Bensmaili Aicha. Kinetic models for the sorption of dye from aqueous solution by clay-wood sawdust mixture[J].Desalination,2005,185(1-3):499-508.
