正交试验优选槐角总黄酮的提取工艺及不同来源槐角中总黄酮的含量测定*
2011-07-12韦华梅闫腾蛟林宜沛王剑波第四军医大学药学系药物研究所西安710032
韦华梅 闫腾蛟 林宜沛 王剑波 第四军医大学药学系药物研究所 (西安 710032)
中药槐角为豆科植物槐(Sophora japonica L.)的干燥成熟果实,又名槐实(《本经》),槐子 (陶弘景 ),槐豆 (《本草原始》),槐连灯、九连灯、天豆 (《河南中药手册》),槐连豆(《中药材手册》)[1]。传统中药学认为其性寒、味苦;归肝、大肠经,具有清热泻火,凉血止血的功效。临床主要用于肠热便血、痔肿出血,肝热头痛、眩晕目赤[2],为《中华人民共和国药典》历版收载品种。近年来国内外医药工作者对其进行多方面的研究。尤其是槐角中富含异黄酮类化合物的特点,使其成为国际上研究和开发的热点。国内外学者对槐角属药用植物的化学成分及生物活性进行了一系列研究,从槐角中提取主要含黄酮类和异黄酮类化合物,其中有染料木素、槐属苷、槐属双苷、山奈酚糖苷-C、槐属黄酮苷和芸香苷,芸香苷的含量很高,另含槐糖、油酸、亚油酸和亚麻酸等一些化学物质[3]。本文参考有关文献[4-7],采用正交试验法优化槐角提取物中总黄酮含量的提取工艺,用优化出的最佳工艺对陕西不同时期不同产地槐角提取物中总黄酮含量进行测定。
1 仪器与材料 1.1 仪器 紫外可见分光光度计(SPECORD200),电子天平(LT202E,常熟市天量仪器有限公司),旋转蒸发仪(陕西泰康生物科技有限公司),Sartorius电子分析天平(德国沙多利斯公司)等。
1.2 材料 槐角苷对照品(中国药品生物制品检定所批号:111695-200501);槐角样本(陕西地道中药材种植有限公司)等。
2 方法与结果 2.1 正交设计提取因素与水平
在考察单因素影响的预试验的基础上,选择乙醇作为提取溶剂,以乙醇浓度、提取次数、提取时间和溶媒体积为考察因素,各因素设定 3个水平,见表1。
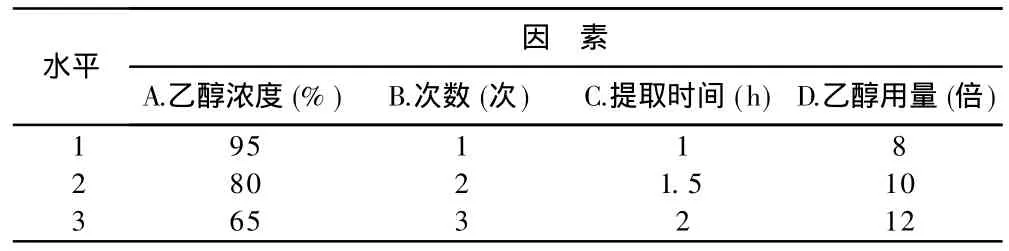
表1 因素与水平
2.2 总黄酮含量测定方法学研究 2.2.1 供试品溶液的制备:称取槐角 A2药材 60.05g,置 100m L圆底烧瓶中,用8倍量60%乙醇加热回流提取3次,每次2h,趁热抽滤,合并滤液,减压回收溶剂,浸膏减压干燥至恒重。将槐角提取物在研钵中研碎后精密称取槐角提取物1mg至10m L容量瓶中,加70%乙醇适量,50℃水浴加热溶解,冷却至室温,稀释至刻度。精密量取1m L于 10m L容量瓶中,加 70%乙醇稀释至刻度,摇匀,即制得供试品溶液。
2.2.2 对照品溶液的制备:精密称取置五氧化二磷减压干燥器中干燥 12h以上的槐角苷对照品 4.13mg置 100m L容量瓶中,加 70%乙醇稀释至刻度,摇匀,即制得对照品溶液。
2.2.3 测定波长的选择:以 70%乙醇作空白对照,在200~400波长范围内扫描供试品溶液和对照品溶液,结果表明二者均在 263nm处有最大吸收,因此确定263nm为测定波长。
2.2.4 标准曲线的制备:精密量取对照品溶液0.2,0.4,0.6,0.8,1.0,1.2,1.4,1.6 m L分别置于10m L容量瓶中,加70%乙醇稀释至刻度,摇匀。以70%乙醇作空白,于 263 nm处测定吸光度,以对照品的浓度和吸光度数据经回归处理,线性回归方程为 y=0.0846x+0.0143,r=0.9995。结果表明:槐角苷质量浓度在0.826mg/L~6.608mg/L范围内线性良好。实验数据见表2。

表2 标准曲线数据
2.2.5 精密度试验:取浓度为 1.652mg/L的槐角苷标准品溶液,重复测定 6次,吸光度值均为 0.16,计算 RSD为0.00%,结果表明仪器的精密度良好。
2.2.6 稳定性试验:取供试品溶液分别于0,0.5,1,1.5,2,2.5 h测定其吸光度值,吸光度值均为0.19,RSD为 0.00%,结果表明本法所测样品在 2.5h内稳定。
2.2.7 重复性试验:分别精密称取8倍量 60%乙醇槐角提取物 1mg,平行 5份,按“2.2.1”项下操作,测定吸光度值,计算总黄酮的百分含量,RSD为 1.58%,结果所测样品的重复性良好。
2.2.8 加样回收率试验:精密称取8倍量 60%乙醇槐角提取物 0.00123g、0.00087g、0.00135g分别置10m L容量瓶中,加 70%乙醇适量,50℃水浴加热溶解,冷却至室温,稀释至刻度。分别精密量取两个1m L于两个 10m L容量瓶中 ,编号为 1、2、3、4、5、6,依次加入槐角苷标准溶液 0.70m L、0.75m L、0.50m L、 0.53m L、0.61m L、0.68m L,加 70%乙醇稀释至刻度 ,摇匀,即得。测定吸光度值并计算回收率和RSD。结果见表3。

表3 回收率试验结果
上述结果表明,紫外分光光度法测定总黄酮含量,方法可靠,定量准确。
2.3 正交试验结果 称取槐角 A2药材每份50g,按L9(34)正交表4设计方案进行试验[2]。结果见表4和表5。

表4 L9(34)正交表试验结果
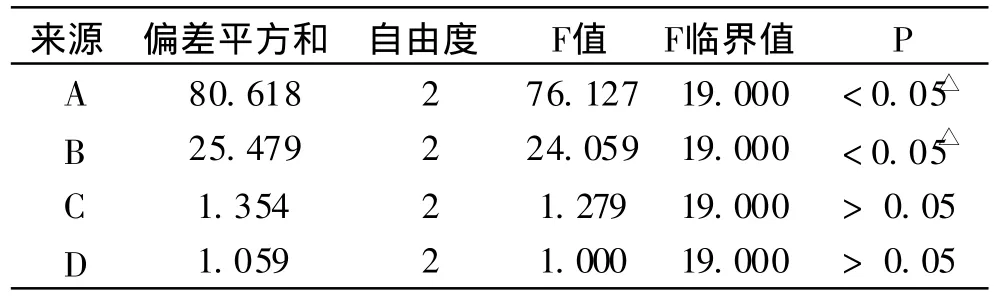
表5 方差分析
根据表4对测定结果进行直观分析数据可知,各因素对提取效果的影响程度为 A>B> C>D,即乙醇浓度>提取次数>提取时间>乙醇用量,A3 B3 C2 D1为最佳工艺。方差分析可知,乙醇浓度A和提取次数B槐角总黄酮的提取有显著性影响,提取时间和乙醇用量对总黄酮的提取没有太大的影响,考虑生产中节约成本,节省时间,提高效率,提取时间和乙醇用量对其总黄酮含量影响不是非常大,所以用 C1代替 C2,即A3 B3 C1 D1为最优工艺,即 8倍量65%乙醇回流提取 3次 ,每次 1h。
2.4 验证试验 为进一步考察优化工艺的可靠性,取 3份药材,每份 50g,按上述最佳提取工艺A3 B3 C1 D1进行验证试验,操作方法同上,测定结果见表6。结果表明此最佳工艺条件合理,同时也表明此工艺具有较好的稳定性。

表6 验证试验结果
2.5 总黄酮的含量测定 2.5.1 样品来源及编号:将延安宜川、榆林清涧、渭南蒲城、咸阳旬邑、宝鸡陇县5个地区作为采集供试样点。供试样的要求为不同产地同一时间采集,并且 8月一个产地 1个样(开花期,样本多缺失),9、10、11月为一个产地不同时期(上、下旬)2个样。将产地按 A榆林、B延安、C渭南、D咸阳、E宝鸡进行编号,每个产地的 7个样编为 0~6号。编号见表7。

表7 槐角样品编号情况
2.5.2 总黄酮的含量测定:按照优化工艺优选的方法对各个槐角样品进行提取,并对提取物中的的总黄酮含量进行测定,测定结果见表8。

表8 总黄酮含量测定结果
2.6 讨 论 通过测定陕产槐角总黄酮含量,发现不同来源的样品总黄酮的含量有一定差异。经比较陕北黄土高原沟壑区榆林清涧与延安宜川 9月下旬槐角总黄酮含量最高,渭北黄土高原沟壑区11月上旬槐角总黄酮含量较高,这可能与日照时间、温度、海拔和干旱等因素有关。此研究为陕西产槐角的资源利用和开发提供实验依据。
[1] 南京中医药大学.中药大辞典 [M].上海:科学技术出版社,2437.
[2] 中华人民共和国药典委员会.中国药典(2010版一部)[S].北京:化学工业出版社,2010:334.
[3] 王景华,唐于平,楼凤昌,等.槐角化学成分与药理作用 [J].国外医药:植物药分册,2002,17(2):58-60.
[4] 冯卫生,赵献敏,王彦志,等.正交设计优选卷柏中总黄酮的提取工艺研究 [C].中草药,2009,40(6):893-895.
[5] 张芸兰,王文渊.正交设计法优选杜鹃花中总黄酮的提取工艺 [J].广州化工 ,2009,37(3);134-136.
[6] 冉晓燕,胡德禹,薛 伟.槐角中总黄铜的提取工艺研究 [J].贵州教育学院学报 ,2009,20(6):22-24.
[7] 庄志军,钟方丽,杨英杰,等.刺玫果中总黄酮的提取与分析 [J].中成药,2007,29(9):1394-1396.
