多巴胺电化学传感器的研究进展
2011-06-26钟桐生雷存喜
刘 蓉,钟桐生,雷存喜
(湖南城市学院化学与环境工程系,湖南益阳413000)
0 引言
多巴胺(Dopamine,DA)的化学名称为3,4-二羟基-β-苯乙胺,是一种广泛存在于脊椎和非脊椎动物中的重要神经递质。1910年,英国科学家George首次在实验室合成了多巴胺。1958年,瑞典科学家Nils-Åke在化学实验室首次发现多巴胺可以作为神经传递素。得到DA不只是甲状腺素和去甲肾上腺素的前驱,而是脑内信息传递者的这一结论使Carlsson获得了2000年的诺贝尔奖[1]。
DA是一种神经传导物质,用来帮助细胞传送脉冲,神经功能失调是精神分裂症和帕金森氏症的重要原因。此外,多巴胺为拟肾上腺素药,具有兴奋心脏、增加肾血流量的功能,广泛用于治疗神经紊乱、支气管哮喘、高血压、先天性心血性及感染性休克。根据研究,多巴胺还能够治疗抑郁症;而DA不足则会令人失去控制肌肉的能力,严重时会令病人的手脚不由自主地颤动或导致帕金森氏症。因此,对其在脑、血液、尿和组织中的含量测定方法的研究无论是在生理功能研究还是在临床应用方面都具有重要的实际意义。
测量DA浓度的方法很多,如滴定法[2]、分光光度法[3]、液相色谱法[4]等。因为DA的苯环上连有两个羟基,能够被氧化生成醌后再还原成酚,从而具有电化学活性,可以用电化学方法进行测量。电化学方法具有灵敏度高、选择性好等优点,尤其是电化学型生物传感器能够进行活体分析,这一优点是其它方法无法比拟的。DA在电极表面的反应式为:
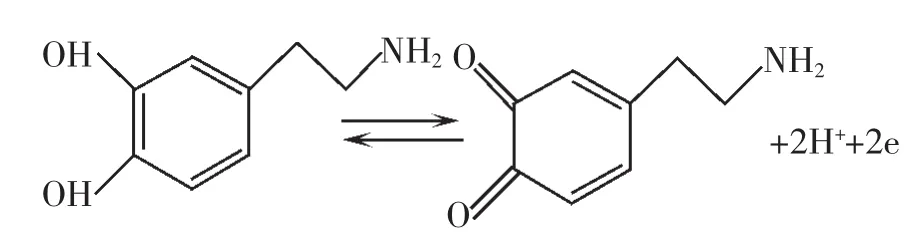
抗坏血酸(Ascorbic acid,AA)、多巴胺常共存于大脑和体液中,AA的浓度一般从10-7~10-3mol/L不等且易被氧化失去两个氢原子而转变成脱氢抗坏血酸,而DA的浓度为10-8~10-6mol/L,AA的浓度远高于DA的浓度,而且在裸电极上两者的氧化电位相近而使氧化峰重叠,如何在高浓度AA存在下测量DA的含量一直是电化学分析家非常感兴趣的并成为电化学分析研究的重要课题之一。另外,尿酸(UA)也与DA和AA共存于体液中,但是因为其含量较低,所以对DA的干扰远不如AA明显,只有少部分的学者在研究AA干扰的同时也研究了UA的影响。
化学修饰电极是以导体或半导体为基底电极,在电极表面嫁接或涂敷具有选择性的单分子、多分子、离子或聚合物的化学物薄膜(从单分子到几个微米),借Faraday(电荷消耗)反应而呈现出此修饰簿膜的化学、电化学及光学等性质[5],因其具有高选择性和高灵敏性的检测特点,使得化学修饰电极在分析化学中得到了广泛的应用。在DA的测定中,常见的电极修饰分为以下几大类:聚合膜、Nafion膜、碳纳米管、碳纳米管/纳米粒子/聚合膜和氨基酸法。
1 化学修饰多巴胺传感器的分类
化学修饰电极除了可以在高浓度的AA中测定DA外,还能增加DA的传质速率,从而提高测定DA的灵敏度。为了提高测定DA的选择性,目前出现的修饰膜有很多,诸如:聚合膜、Nafion膜、碳纳米管和氨基酸膜等,所有这些化学修饰膜的主要思路基于两条:一是将阳离子选择性膜通过各种方法修饰在电极表面以达到排除抗坏血酸阴离子干扰的目的,由于这些修饰膜在一定的pH值下带负电荷,同时使得AA(pKa=4.1)带负电荷,而DA(pKa=8.87)带正电荷,通过静电相互作用,可选择性地对DA阳离子进行响应,而抑制阴离子AA在电极表面的氧化反应,从而达到选择性测定多巴胺的目的;二是选择适当修饰剂的化学修饰电极,该修饰膜的骨架带有正电荷,通过静电吸引力使带负电荷的AA的氧化峰负移,使带正电荷的DA的氧化峰正移,尽可能地将两者的氧化峰分开而实现对两物质的同时检测。
1.1 聚合膜
聚合膜因为具有良好的稳定性和重现性,在近几年的DA测量中受到广泛的应用。聚合在电极表面的聚合膜对DA的测定原理主要是以下两种:(1)聚合以后,聚合膜在待测溶液中带负电荷,使得AA没有响应,而直接测 DA;(2)将 AA和DA的峰分开而选择性测定DA或者分别测定DA和AA。
1.1.1 AA没有响应,而直接测DA
孙登明等[6]用掺杂聚L-酪氨酸修饰玻碳电极同时测定DA和AA,两种组分同时测定的线性范围分别为 5.0×10-6~1.0×10-4mol/L 和3.0×10-5~1.0×10-3mol/L。 Zhao 等[7]在玻碳电极上聚合聚(2-吡啶甲酸)膜,在pH为7.0的PBS中,加入 1.0×10-3mol/L AA 对测量 1.0×10-4mol/L DA的结果无明显影响,进一步实验表明150倍AA不干扰其DA的结果。陈伟等[8]研究了DA在聚刚果红修饰电极上的电化学行为,此电极对DA有明显的电催化作用,并能有效消除AA对DA测定的干扰。咸洋[9]采用层层自组装方法应用无机介孔材料SBA-15,高分子聚合物聚丙烯酸(PAA)和聚二甲基二烯丙基氯化铵(PDDA)制备了层层组装修饰电极,结果表明通过利用SBA-15的离子筛功能,PDDA(PAA/SBA-15)5层层自组装膜成功实现了AA共存条件下神经递质DA的选择性测定。即使AA浓度高达1.0×10-4mol/L时仍无响应,对2.0×10-5mol/L的DA无干扰。该研究通过调节溶液的pH值和离子强度来有效的控制离子通道的“开关”状态,达到了排除阴离子AA的干扰,提高了测定DA的选择性和灵敏度的目的。Li等[10]用分子印迹法,以DA为模板分子,在金电极上电聚合邻氨基酚法制备了多巴胺分子印迹膜传感器。传感器线性范围为2.0×10-8~0.25×10-6mol/L,检出限为 1.98×10-9mol/L。 该传感器可在高浓度抗坏血酸(AA)存在下测定DA(DA与AA摩尔比为1/1 000),因为制得的印迹聚合膜具有特定形状的识别孔穴,能够选择性识别多巴胺,多巴胺进入识别位点后会引起电流变化,而大大提高了其选择性。
1.1.2 将AA和DA的峰分开测定
Balamurugan等[11]利用聚(3,4-乙烯二氧噻吩-连-(2-磺酸萘))(PEDOT-PANs)测得DA和AA的氧化峰分别为 0.33 V和 0.1 V,PEDOTPANs膜中的磺酸基团可以使得AA的峰电位负移,从而使得AA和DA的峰分开。Zhang等[12]采用聚(氨基磺酸)对 1.0×10-5mol/L DA 和 1.0×10-3mol/L AA的混合溶液进行测量,DA和AA的氧化峰分别为0.163 V和-0.012 V。Jin等[13]利用聚(氨基苯磺酸)膜修饰电极同时测定DA和AA,差示脉冲伏安法(DPV)的结果,DA和AA的氧化峰分别为0.196 V和0.008 V。Ensafi等[14]用聚偶氮砜测得AA、DA和UA的氧化峰分别为0.17 V、0.35 V和0.50 V。万其进等[15]研究了聚茜素红膜修饰电极(PARE)的制备及其对DA和AA的电催化性能表明,二者的氧化峰电位分开近200 mV,可通过控制不同的电位范围进行分步扫描,实现了对同一体系中DA和AA的分别测定。Roy等[16]用聚(N,N-二甲基苯胺)修饰玻碳电极可以同时测定DA和AA,且将两者的氧化峰分开约300 mV。Lin等[17]用对硝基偶氮间苯二酚(NBAR)修饰玻碳电极,在pH为4.0的磷酸缓冲溶液中,当AA和UA的浓度比DA分别高30和3倍时,不影响对DA的测定结果,在NBAR修饰玻碳电极上DA和AA的峰分别出现在0.390 V和0.195 V。还有用通过电聚合聚苯二胺[18]、甲酚红[19]可以通过将二者的峰分开来测定DA。
1.2 Nafion膜
近年来研究得比较多的阳离子交换剂中,使用最多并且最成功的就数Nafion膜。Nafion膜是典型的全氟磺酸质子交换膜,具有优异的电化学性能、良好的化学和机械稳定性,经过Nafion膜修饰后,传感器对AA的响应灵敏度随着吸附时间的延长而逐渐降低,而DA的响应则逐渐上升。另外Nafion膜具有渗透性,根据溶液中分子或离子的大小、荷电及空间结构等差异能有选择地使某些分子或离子透过膜孔起到“分子筛”的作用,从而达到使待测物富集的目的,同时Nafion膜中存在阳离子传递通道,有利于DA分子的扩散,从而提高了传感器的灵敏度,缩短了响应时间。
方禹之等[20]根据碳纤维表面的多孔性,用Nafion来修饰碳纤维微电极表面,在AA共存下选择性测定神经递质去甲肾上腺素和DA,不仅有效地消除了高含量AA的干扰,而且大大降低了电极的噪音,使电极测定DA的灵敏度大大提高。林祥钦等[21]制备了胆碱(Ch)共价键植的碳纤维电极(Ch/CFE),进而吸附涂敷一薄层Nafion膜得到了Nafion/Ch/CFE。使用DPV法,该电极能良好抵抗AA的干扰而选择性测量DA,适用于活体监测。张亚等[22]用Nafion和亲水性离子液体溴化1-辛基-3-甲基咪唑([OMIM]Br)作修饰剂制作了Nafion-离子液体-修饰碳糊电极,在0.1 mol/L PBS(pH=7.40)中,该修饰电极降低了DA氧化、还原反应的过电位,增大了其氧化、还原反应的峰电流,而AA和UA在该修饰电极上无响应,该法可用于注射液和模拟生物样品中DA的测定。
1.3 碳纳米管
1991年日本科学家Iijima[23]用真空电弧蒸发石墨电极,并对产物作高分辨透射电镜观察,发现了具有纳米尺寸的碳纳米管 (Carbon nanotubes,CNTs)。作为一维纳米材料,重量轻,直径细,结构多变,六边形结构连接完美,有独特的物理、化学特征,在纳米材料科学与加工技术、分子电子器件及生命科学领域中吸引了人们的广泛注意。
王宗花等[24]制备了碳纳米管(CNT)修饰电极(镶嵌、涂层),并首次研究了电分离DA和AA的机理,结果表明,该电极的表面有一个多孔性的立体界面层,不仅对DA和AA具有较强的电催化作用,而且二者的氧化峰电位差达250 mV以上。用酸处理后的多壁碳纳米管修饰的石墨电极可以使DA和AA的氧化峰明显地分开,对两者的氧化均具有明显的电催化作用,可以同时测定DA和AA。但碳纳米管在用酸处理时,酸的氧化性不宜太强,否则将不利于在AA存在下对DA的测定。这是因为酸的氧化性越强,碳纳米管表面生成的羧基和羟基越多,使碳纳米管的电负性增强,碳纳米管与AA的静电斥力增大,这使AA的峰电位正移,与DA的峰电位差减小,影响DA的测定[25]。Baldrich等[26]用磁性纳米粒子(MP)吸附CNT制得MP/CNT电极,这样的电极既继承了CNT将DA和UA之间分开的优点,又继承了MP纳米粒子增敏的特点。与一般电极相比,MP/CNT电极上的峰电流可增大2.6~5倍。杨瑞兰[27]将CNT制成糊状电极(CNTPE),研究了该电极在DA和AA共存时的电化学行为,并且将其与传统的碳糊电极(CPE)作了比较。结果表明,CNTPE比CPE具有更明显的催化作用,而且使DA的氧化峰位正移,两者的氧化峰位分离达200 mV,并在AA存在的情况下成功的测定了DA的含量。羧基化CNT将AA和DA的峰分开,且使得AA和DA的峰电流明显增大,主要原因有:(1)MWNT特有的管、空腔及携带的-COOH和-OH基团,容易与DA分子酚羟基中的氢形成氢键,电子通过O-H-O键传递,从而使酚羟基活化,削弱了苯环上O-H键之间的键能,使DA更容易被氧化,因而降低了氧化过电位[28];(2)MWNT上特有的空腔及-COOH和-OH基团,提供较多的反应位点和传输空间,MWNT上带点较多的含氧基起着质子的接受体的作用,同时空间界面有利于质子、电子的传输[29],从而使DA和AA在该修饰电极上的峰电流显著增大。
1.4 碳纳米管/纳米粒子/聚合膜
纳米金粒子有大的比表面积和良好的导电性,是优良的电子导线和活性催化剂[30],可显著提高现有分析方法的灵敏度。在多层膜中,金纳米粒子作为电子导线大大加快了电子传递速率。另外,金属纳米粒子还具有提高电化学敏感膜中电活性物质氧化还原可逆性的功能。
近年来,将能够分别测定DA的聚合膜和碳纳米管联用,并加入具有良好的催化活性性能的纳米粒子制成碳纳米管/纳米粒子/聚合膜,其优点在于形成了新的复合材料,并通过协同效应保留了单种组分的性能。现已研究出的此类复合材料有聚苯胺/多壁碳纳米管(PAN I/MCNT),聚对苯乙烯/碳纳米管(PPV/CNT)、聚二氧乙基噻吩/碳纳米(PEDOT/CNT)等,目前有部分已经用于DA的测定。
1.4.1 AA没有响应,而直接测DA
李春香等[31]利用2,6-吡啶二甲酸(PDA)与多壁碳纳米管(MCNT)共聚修饰玻碳电极,制成了聚2,6-吡啶二甲酸/多壁碳纳米管(PPDA/MCNT)修饰电极,并将其应用于DA的测定,与MCNT修饰电极相比,前者更具有响应灵敏、检出限低、选择性高及基线电流低的优势。该实验发现在DA 浓度为 1.0×10-7mol/L 时,AA(2.0×10-5mol/L)对DA测定无明显干扰。当AA浓度为DA浓度的1 000倍时,能使DA峰电流降低7.2%。这表明该修饰电极具有良好的选择性,能用于实际样品的检测。Zhang等[32]制备的聚苯乙烯磺酸/单壁碳纳米管成功地测得了DA的含量,在pH为7.0的PBS中,带负电荷的聚苯乙烯磺酸可以吸引带正电荷的DA,并排斥带负电荷的AA从而消除AA的干扰。马曾燕等[33]在玻碳电极上通过电聚合制备了聚L-半胱氨酸/多壁碳纳米管 (poly-LCys/MWNT)复合修饰电极,实验表明,poly-LCys/MWNT修饰电极对DA有良好的电催化作用,且AA对DA检测无干扰。郑娜等[34]研究了聚磺基水杨酸/多壁碳纳米管修饰玻碳电极的制备及DA在此修饰电极上的电化学行为,pH=7.4 PBS中,在1.0×10-3mol/L AA共存的条件下,DA氧化峰电流与其浓度在5.0×10-7~1.0×10-4mol/L范围内分段呈线性关系,结果表明:聚磺基水杨酸/多壁碳纳米管修饰电极结合了多壁碳纳米管灵敏度高和聚磺基水杨酸选择性好的优点,可用于AA共存条件下DA的测定。马曾燕等[35]制备了聚吡咯/多壁碳纳米管(PPy/MWNT)复合膜修饰电极。pH=4.10的0.2 mol/L醋酸-醋酸钠缓冲溶液中,DA在该修饰电极上的CV曲线于0.31 V和0.28 V处出现一对灵敏的氧化还原峰,峰电位差ΔEp比裸玻碳电极降低58 mV,比PPy修饰电极低28 mV,峰电流显著增加。
1.4.2 将AA和DA的峰分开分别测定
王宗花等[36]采用电聚合方法将茜素红修饰到碳纳米管上,制备了聚茜素红/碳纳米管修饰电极,该电极能显著提高电极的灵敏度和分子识别性能,DA和AA的氧化峰位分离达240 mV,在AA的存在下,DA的差分脉冲伏安法峰电流在10-7~10-5mol/L范围内呈良好的线性关系。
1.5 氨基酸法
黄燕生[37]将L-赖氨酸玻碳修饰电极上,通过DPV测得AA和DA的氧化峰峰间距为460 mV;L-酪氨酸玻碳修饰电极的DPV图上峰间距为408 mV,实验结果表明玻碳电极上DA和AA重叠的单氧化峰在氨基酸修饰玻碳电极上分开成为两个完全独立的氧化峰,从而实现了选择性检测DA。张雷等[38]采用电氧化法制备了一种新型γ-氨基丁酸(ABA)修饰的玻碳电极,DA与AA分别于0.45 V和0.07 V出现独立的阳极方波伏安峰,表明此修饰电极可用于这两种物质的同时测定。陈贤光等[39]表明L-半胱氨酸(L-Cys)自组装金电极对多巴胺有明显的电催化氧化作用,DA与AA的氧化峰均可以得到足够大的分离,用CV和DPV测得其电位差分别为385 mV和400 mV,进一步的试验结果表明,在相对误差±5%以内,3倍的AA不影响3.3×10-4mol/L DA的循环伏安法测定[39]。
1.6 其他方法
连靠奇[40]研究了在强碱溶液中活化粗糙玻碳电极(ARE)的制备方法及其对DA和AA电催化性能。表明ARE使DA和AA的氧化峰得到了很好的分离,在pH=5.72的溶液中峰位差为200 mV,在pH=1.98的溶液中峰位差达230 mV,实现了DA和AA共存时的同时测定。Zhao等[41]研究了DA、AA在离子液体1-辛基-3-甲基咪唑六氟合磷(OMIMPF6)/多壁碳纳米管凝胶修饰电极上的电化学行为,实现了对DA、AA的催化、分离,发现可同时检测这两种生物小分子而互不干扰。Milczarek等[42]利用2,2-双(3-氨基-4-羟基苯基)六氟丙烷修饰电极测得DA和AA的氧化峰分别是 -0.073 V 和 0.131 V, 溶液中 4 000倍 AA 不干扰DA的测定结果。 Li等[43]用 β-环糊精在5 mmol/L的AA中,在1~200 μmol/L的范围内,DA的氧化峰电流与其浓度成正比。Li等[44]制得DTPA(二亚乙基三胺五乙酸)/Cys(半胱氨酸)/Au,相比5.0×10-6mol/L DA的氧化峰的峰电流值,此电极对 5.0×10-5mol/L UA 和 5.0×10-5mol/L AA几乎不响应,在pH值为7.4的PBS中,具有五个羧基的DTPA带大量负电荷可吸引带正电荷的DA分子,使得DA在电极上的氧化峰非常明显;同时带负电荷的DTPA能够排斥带负电荷的AA,使得AA无法靠近修饰电极而无法显现明显的氧化峰,这样就达到了消除AA干扰的目的。
2 多巴胺传感器的展望
建立具有选择性好、灵敏度高的DA测定方法在临床应用、探讨其生理机制方面具有重要的实际意义,从该综述中可以看出虽然其研究已经取得了较多成果,但理论方面不是非常具体,而且实际应用也是处在发展之中。聚合物修饰电极的发展将对DA检测起重大作用;纳米金属或金属氧化物颗粒掺杂聚合物修饰电极因其对DA有较好的电催化活性,在DA检测中有较大的应用前景。纳米结构的电极上电催化氧化机理的深入探索,灵敏度高、选择性好和稳定性好的DA传感器的制备不仅在实际应用中得到进一步地发展,而且其理论内容也越来越丰富。
[1]Benes F M.Carlsson and the discovery of dopamine[J].Trends in Pharmacological Sciences,2001,22(1):46~47.
[2]Salem F B.Spectrophotometric and titrimetric determination of catecholamines[J].Talanta,1987,34 (9):810 ~812.
[3]Mamiński M,Olejniczak M,Chudy M,et al.Spectrophotometric determination of dopamine in microliter scale using microfluidic system based on polymeric technology[J].Analytica Chimica Acta,2005,540(1):153~157.
[4]Guan C L,Ouyuang J,Li Q L,et al.Simultaneous determination of catecholamines by ion chromatography with direct conductivity detection[J].Talanta,2000,50(6):1 197~1 203.
[5]董绍俊,车广礼,谢远武.化学修饰电极 [M].北京:科学出版社, 1995.210.
[6]孙登明,田相星,马伟.银掺杂聚L-酪氨酸修饰电极同时测定多巴胺、肾上腺素和抗坏血酸[J].分析化学,2010,38(12):1 742~1 746.
[7]Zhao H,Zhang Y Z,Yuan Z B.Electrochemical determination of dopamine using a poly(2-picolinic acid)-modified glassy carbon electrode[J].Analyst,2001,126(3):358~360.
[8]陈伟,林新华,黄丽英,等.多巴胺在聚刚果红修饰电极上的伏安行为及其测定[J].福建医科大学学报,2005,39(1):61~64.
[9]咸洋.新型纳米生物传感器界面的设计与应用研究[D].上海:华东师范大学硕士学位论文,2007.
[10]Li J,Zhao J,Wei X.A sensitive and selective sensor for dopamine determination based on a molecularly imprinted electropolymer of o-aminophenol[J].Sensors and Actuators B:Chemical,2009,140(2):663~669.
[11]Balamurugan A,Chen S M.Poly(3,4-ethylenedioxythiophene-co-(5-amino-2-naphthalene sulfonic acid))(PEDOT-PANS)film modified glassy carbon electrode for selective detection of dopamine in the presence of ascorbic acid and uric acid[J].Analytica Chimica Acta,2007,596(1):92~98.
[12]Zhang Y,Jin G,Yang Z.Determination of dopamine in the presence of ascorbic acid using poly(amidosulfonic acid)modifed glassy carbon electrode[J].Microchimica Acta,2004,147(4):225~230.
[13]Jin G,Zhang Y,Cheng W.Poly(p-aminobenzene sulfonic acid)modifed glassy carbon electrode for simultaneous detection of dopamine and ascorbic acid[J].Sensors and Actuators B:Chemical,2005,107(2):528~534.
[14]Ensafi A A,Taei M,Khayamian T,et al.Highly selective determination of ascorbic acid,dopamine,and uric acid by differential pulse voltammetry using poly(sulfonazoⅢ)modified glassy carbon electrode[J].Sensors and Actuators B:Chemical,2010,147(1):213~221.
[15]万其进,喻玖宏,王刚,等.聚茜素红膜修饰电极控制电位扫描法分别测定多巴胺和抗坏血酸[J].高等学校化学学报,2000,21(11):1 651~1 654.
[16]Roy P R,Okajima T,Ohsaka T.Simultaneous electroanalysis of dopamine and ascorbic acid using poly(N,N-dimethylaniline)-modified electrodes[J].Bioelectrochemistry,2003,59(1-2):11~19.
[17]Lin X H,Zhang Y F,Chen W,et al.Electrocatalytic oxidation and determination of dopamine in the presence of ascorbic acid and uric acid at a poly (p-nitrobenzenazo resorcinol)modified glassy carbon electrode[J].Sensors and Actuators B:Chemical,2007,122(1):309~314.
[18]Ekinci E, Erdogdu G,Karagozler A E. Preparation,optimization,and voltammetric characteristics of poly(ophenylenediamine)film as a dopamine-selective polymeric membrane[J].Journal of Applied Polymer Science,2001,79(2):327~332.
[19]Chen W,Lin X H,Huang L Y,et al.Electrochemical characterization of polymerized cresol red film modified glassy carbon electrode and separation of electrocatalytic responses for ascorbic acid and dopamine oxidation[J].Microchimica Acta,2005,151(1-2):101~107.
[20]方禹之,于雁灵,何品刚.Nafion修饰电化学活性碳纤维微电极测定去甲肾上腺素[J].分析化学,1995,23(12):1 440~1 443.
[21]林祥钦,康广凤,柴颖.Nafion/胆碱双层膜碳纤维电极探测小白鼠大脑内的多巴胺[J].分析化学,2008,36(2):157~161.
[22]张亚,张宏芳,郑建斌.Nafion-离子液体-修饰碳糊电极在抗坏血酸和尿酸存在下选择性测定多巴胺[J].分析试验室,2008,27(12):34~37.
[23]Iijima S.Helical microtubes of graphite carbon[J].Nature,1991,354:56~58.
[24]王宗花,刘军,颜流水,等.碳纳米管修饰电极的孔性界面对电分离多巴胺和抗坏血酸的影响[J].高等学校化学学报,2003,24(2):236~240.
[25]袁倬斌,王月伶,张君,等.碳纳米管在电分析中的应用[J].化学通报,2004,67(7):473~476.
[26]Baldrich E,Gómez R,Gabriel G,et al.Magnetic entrapment for fast,simple and reversible electrode modification with carbon nanotubes:Application to dopamine detection[J].Biosensors and Bioelectronics,2011,26(5):1 876~1 882.
[27]杨瑞兰.碳纳米管修饰电极在电化学生物传感器中的应用研究[D].吉林:东北师范大学,2008.
[28]Dalmia A,Liu C C,Savinell R F.Electrochemical behavior of gold electrodes modified with self-assembled monolayers with an acidic end group for selective detection of dopamine[J].Journal of Electroanalytical Chemistry,1997,430(1-2):205~214.
[29]王歌云,王宗花,肖素芳,等.碳纳米管修饰电极对多巴胺和肾上腺素的电分离及同时测定[J].分析化学,2003,31(11):1 281~1 285.
[30]Xiao Y,Patolsky F,Katz E,et al.“Plugging into Enzymes”:Nanowiring of redox enzymes by a gold nanoparticle[J].Science,2003,299(5614):1 877~1 881.
[31]李春香,曾云龙.聚2,6-吡啶二甲酸/多壁碳纳米管修饰电极的电催化性能[J].分析化学,2006,34(7):999~1 002.
[32]Zhang Y Z,Cai Y J,Su S.Determination of dopamine in the presence of ascorbic acid by poly (styrene sulfonic acid)sodium salt/single-wall carbon nanotube film modified glassy carbon electrode[J].Analytical Biochemistry,2006,350(2):285~291.
[33]马曾燕,李将渊,向伟.多巴胺在聚L-半胱氨酸/多壁碳纳米管修饰电极上的电化学行为及其伏安测定[J].应用化学,2009,26(2):224~227.
[34]郑娜,侯书荣,周霞,等.聚磺基水杨酸/碳纳米管修饰电极在抗坏血酸共存时测定多巴胺[J].分析试验室,2009,28(5):6~10.
[35]马曾燕,李将渊,向伟.聚吡咯/多壁碳纳米管修饰电极对多巴胺的测定[J].化学研究与应用,2008,20(12):1 570~1 574.
[36]王宗花,张旭麟,张菲菲,等.聚茜素红功能化碳纳米管修饰电极对多巴胺和抗坏血酸的电化学研究[J].分析实验室,2007,26(10):17~20.
[37]黄燕生.L-赖氨酸、L-酪氨酸单分子层玻碳修饰电极在杭坏血酸共存下对多巴胺的检测[D].北京:首都师范大学,2006.
[38]张雷,林祥钦.单分子层γ-氨基丁酸共价修饰玻碳电极同时测定多巴胺、尿酸和抗坏血酸[J].高等学校化学学报,2003,24(4):591~594.
[39]陈贤光,张素娟,欧阳良琪,等.L-半胱氨酸自组装电极循环伏安法测定多巴胺[J].分析试验室,2007,26(4):30~33.
[40]连靠奇.神经递质多巴胺与小分子药物的电化学研究[D].河北:河北大学,2005.
[41]Zhao Y F,Gao Y Q,Zhan D P,et al.Selective detection of dopamine in the presence of ascorbic acid and uric acid by a carbon nanotubes-ionic liquid gel modified electrode[J].Talanta,2005,66(1):51~57.
[42]Milczarek G,Ciszewski A.2,2-Bis(3-amino-4-hydroxyphenyl)hexafluoropropane modified glassy carbon electrodes as selective and sensitive voltammetric sensors.Selective detection of dopamine and uric acid[J].Electroanalysis,2004,16(23):1 977~1 983.
[43]Li J P,Wu X Z,Yu Y,et al.Self-assembled sulfonated β-Cyclodextrin layer on gold electrode for the selective electroanalysis of dopamine.Journal of Solid State[J].Electrochemistry,2009,13(12):1 811~1 818.
[44]Li J P,Liu R,Yu J G,et al.A gold electrode modified with self-assembled diethylenetri-aminepentaacetic acid via charge-based discrimination[J].Analytical scienes,2009,25(11):1 289~1 293.
