较大剂量阿托伐他汀对择期PCI 术者心肌保护作用
2011-06-22马树人
马树人
(南京医科大学附属淮安第一医院 心内科,江苏 淮安 223300)
他汀类药物是目前最有效的降胆固醇药物,诸多研究证实他汀类药物可显著减少心血管事件,他汀药物的这种效益并不局限于降脂,而且有抗炎等多重效应,这可能是他汀类药物围手术期心肌保护的机制之一。目前认为他汀类药物强化降脂减少重大心血管事件优于常规降脂[1]。但大剂量他汀类药物应用其副作用也明显增高,如肝损害、肌病等,临床应用中因副作用而出现的撤药率大剂量组明显高于常规剂量组,同时由于个体差异,国人对大剂量他汀的耐受性可能较差。本研究旨在探讨较大剂量阿托伐他汀对择期经皮冠状动脉介入(PCI)术后心肌的保护作用及其安全性。
1 资料与方法
1.1 病例选择
2009年6月至2011年1月我科住院病人中经CT冠状动脉成像确诊冠心病并择期行PCI术患者300例,平均年龄66.70岁。具有下列情况者不予入选:急诊PCI及静脉溶栓;入院前2周内服用过降术脂药物;肝、肾功能不全及有肌病的患者;入院时合并有感染、肿瘤、免疫系统疾病等情况。
1.2 研究方法
1.2.1 分组及用药方法 入选患者随机给予不同剂量阿托伐他汀(辉瑞公司提供,商品名立普妥),分为常规剂量组(阿托伐他汀20 mg·d-1)和较大剂量组(阿托伐他汀 40 mg·d-1),每组 150例。入选患者3~5 d后行PCI,同时按照指南常规使用其他药物进行综合治疗,包括抗血小板、硝酸酯类、血管紧张素转化酶抑制剂(ACEI)、血管紧张素转化酶受体拮抗剂(ARB)以及β受体阻滞剂等。术后7 d随访病人,测肝、肾功能指标,超敏C-反应蛋白(hs-CRP),肌酸激酶同工酶(CK-MB),肌钙蛋白I(cTn-I)等。观察指标:患者一般情况:年龄、性别、身高、体重;合并用药情况;实验室检查:肝功能、肾功能;心肌标志物:CKMB、cTn-I;炎症标志物:hs-CRP;他汀药物的不良反应:肌无力、肌痛、消化道反应、过敏。终止标准:服药期间出现肌痛病人不能耐受或肌酸激酶(CK)≥5倍正常高限(ULN)、丙氨酸氨基转移酶(ALT)≥3ULN、肌酐(CR)≥221 μmol·L-1等严重副反应。
1.2.2 血标本采集和检测 全部患者清晨空腹取静脉血,采用日本OLYMPUS AU2700全自动生化分析仪测定肝肾功能、肌酸激酶等指标。检测hs-CRP采用透射免疫比浊法进行定量分析,所用试剂购自德国HUMAN公司,操作步骤严格按操作指南进行。
1.3 统计学处理
采用SPSS 12.0统计学软件进行统计学分析,所有计量数据均使用±s表示,手术前后组内比较采用配对t检验,率的比较采用卡方检验,P<0.05为差异有统计学意义。
2 结 果
2.1 入选患者基本情况
符合研究入选标准病例300例,其中常规剂量组150例,较大剂量组150例。两组基本情况比较见表1、2。
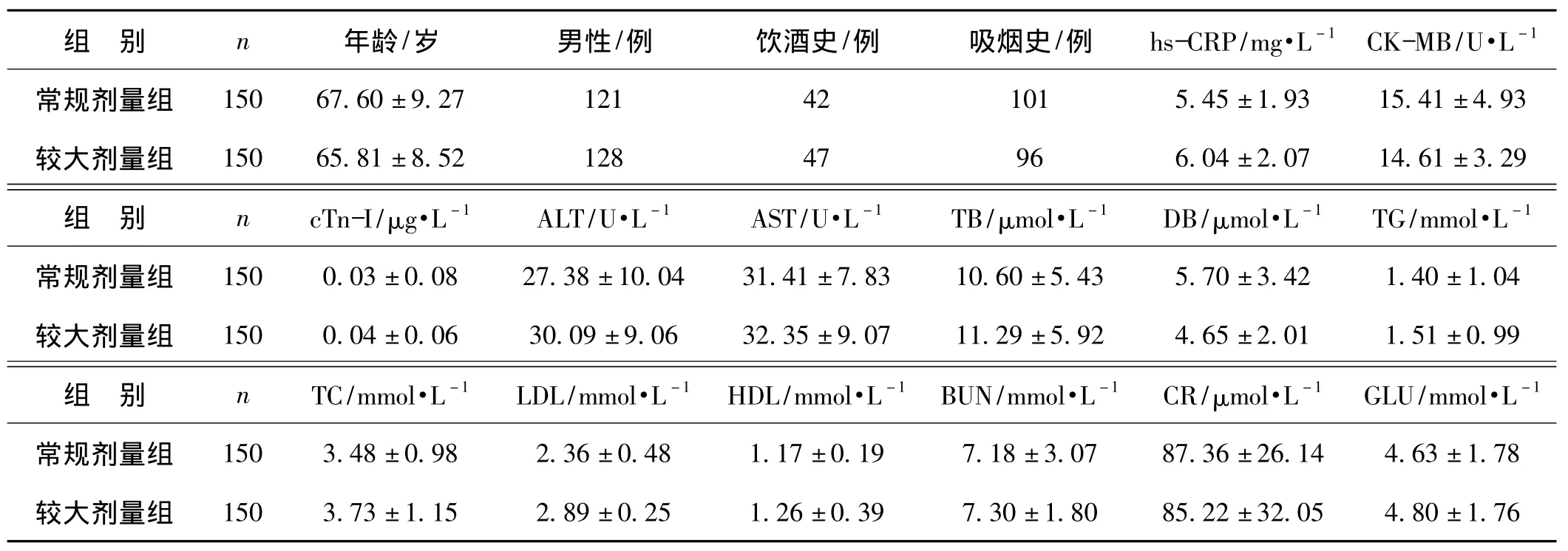
表1 病人的分组及临床资料和基线状况
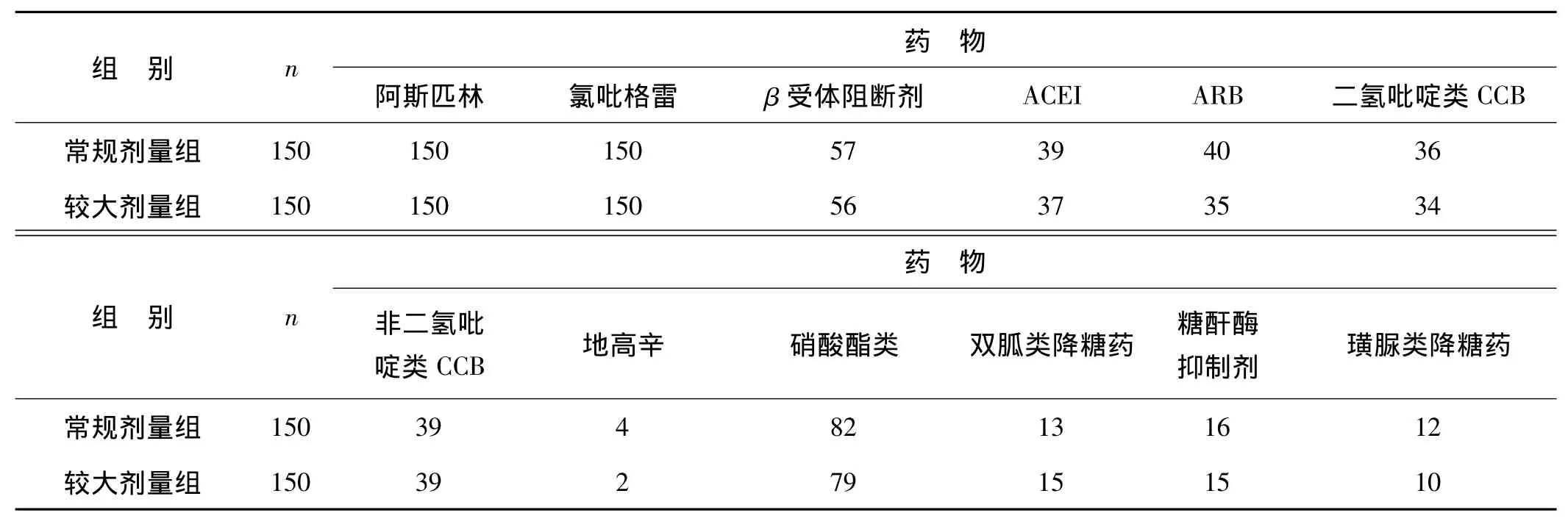
表2 两组患者用药情况例
2.2 他汀对炎症因子及PCI术后心肌损伤的影响
常规剂量组PCI术后和基线比较hs-CRP、CK-MB、cTn-I水平升高(P<0.05),较大剂量组则有所下降,但差异无统计学意义(P>0.05)。两组PCI术后hs-CRP水平比较差异无统计学意义(P>0.05),CK-MB、cTn-I水平较大剂量组均高于常规剂量组(P<0.05),见表3。
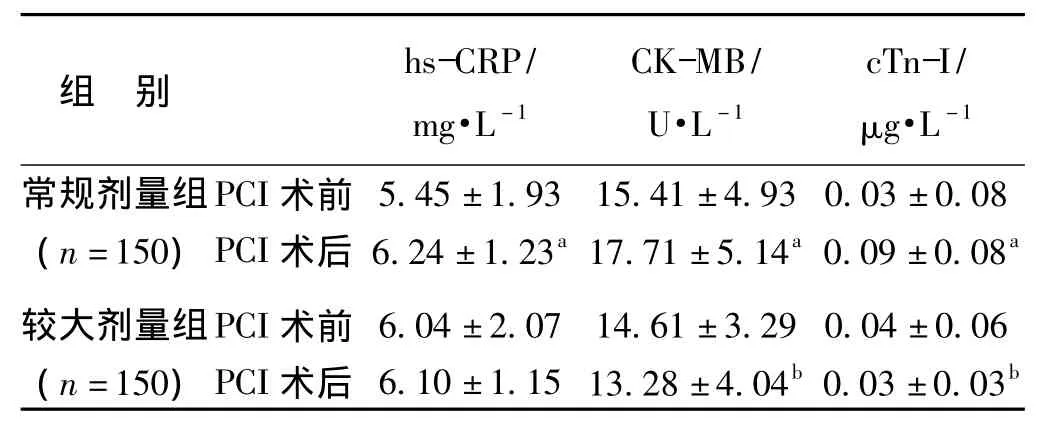
表3 两组服他汀前后hs-CRP、CK-MB、cTn-I水平变化情况
2.3 两组患者PCI术后心血管事件和不良反应发生率比较
两组患者PCI术后严重心血管事件及他汀不良反应发生率比较差异无统计学意义(P>0.05),见表4。

表4 不同剂量他汀对PCI术后心血管事件影响及安全性比较 例
3 讨 论
研究发现,成功的PCI术后,约5% ~30%的患者血浆心肌酶水平升高,提示心肌损伤[3-4],通常心肌损伤标志物只表现为术后轻微的增高,不伴有临床症状、心电图改变或心功能异常,但心肌损害可能与后期心血管事件增加、远期死亡率增高相关[5-6]。经皮球囊扩张、支架植入等操作诱发血小板激活、聚集致血栓形成均导致炎症反应,PCI术后心肌损伤与炎症状态密切相关[6-7]。这是围手术期心肌损伤的重要病因之一。hs-CRP是反映体内炎症状态的指标并与冠脉病变严重程度相关[7],血hs-CRP有能提供LDL以外的预测心血管事件的意义,降低hs-CRP可能更为重要[8-10]。他汀类的抗炎作用有助于加速血管的修复,也可能是围手术期心肌保护的机制之一[11]。已有研究证实择期PCI术前的他汀类药物治疗对围手术期的心脏有保护作用[12-13]。但他汀的理想剂量和用药时机尚需进一步研究。本研究发现围术期使用较高剂量他汀,在心肌保护、抗炎作用方面均优于常规剂量组(P <0.05)。
诸多研究认为他汀药物导致的肝损害发生率较低。接受低剂量和中等剂量他汀类药物治疗,肝酶ALT或谷氨酸草酰乙酸转移酶升高超过3 ULN发生率在1%以下,但使用高剂量(80 mg·d-1)时发生率则达2% ~3%[14]。本研究发现无论常规剂量组还是较高剂量组,均未观察到不良反应的增加,两组间比较差异无统计学意义,较高剂量组2例患者服用他汀后出现ALT>3 ULN,并没有发现血清胆红素的升高,因此可以考虑在严密观察下继续用药,且其中1人为慢性乙肝患者,不排除乙肝活动可能。本研究中未观察到明显的肾功能的损害,提示他汀对肾功能的影响较小。较高剂量组1例患者出现肌痛、无力,但无显著肌酸激酶升高。本研究仅观察了短期效果,随着服药时间的延长,其副作用发生的比例可能会进一步增加。
本研究提示择期PCI术前应用较大剂量(40 mg·d-1)的他汀药物在术后1周即可显示出心肌保护作用,并优于常规剂量组,他汀不良反应的发生率较低,与常规剂量组无明显差异,同时需要说明的是,本研究入选样本相对少,观察时间较短,因此他汀类药物在PCI术前最佳给药时间、最佳负荷剂量和最佳疗程尚需对中国人群进行多中心、大样本、长时间的随机前瞻对照研究。
[1]LaROSA J C,GRUNTY S M,WATERS D D,et al.Intensive lipid lowering with atorvastatin in patients with stable coronary disease[J].N Engl J Med,2005,352:1425-1435.
[2]WATKINS P B,SEEFF L B.Drug-induced liver injury:summary of a single topic clinical research conference[J].Hepatology,2006,43(3):618-631.
[3]BRENER S J,ELLIS S G,SCHNEIDER J,et al.Frequency and long-teml impact of myonocrosis after coronary stenting[J].Eur Heart J,2002,23:869-876.
[4] GRAVNING J,UELAND T,MORKRID L,et al.Different prognostic importance of elevated troponin I after percutaneous coronary intervention in acute coronary syndrome and stable anginapectoris [J].Scand CardiovascJ,2008,42(3):214-221.
[5]PRASAD A,SINGH M,LERMAN A,et al.Isolated elevation in troponin T after percutaneous coronary intervention is associated with higher long-term mortality[J].J Am Coll Cardiol,2006,48(9):1765-1770.
[6]SAADEDDIN S M,HABBAB M A,SOBKI S H,et al.Minor myocardial injury afterelective uncomplicated successful PTCA with or without stenting:detection by cardiac troponins[J].Catheter Cardiovasc Interv,2001,53:188-192.
[7]钱琦,陈忠,马根山,等.血浆超敏C反应蛋白和补体因子H浓度与冠心病的关系研究[J].东南大学学报:医学版,2008,27(5):336-339.
[8]RIDKER P M,RIFAI N,ROSE L,et al.Comparison of C-reactive protein and low-density lipoprotein cholesterol levels in the prediction of first cardiovascular events[J].N Engl J Med,2002,347:1557-1565.
[9]KOSTIS J B,TURKEVICH D,SHARP J.Association between leukocyte count and the presence and extent of coronary atherosclerosis as determined by coronary arteriography[J].Am J Cardiol,1984,53:997-999.
[10]CANNON C P,McCABE C H,BELDER R,et al.Design of the Pravastatin or Atorvastatin Evaluation and Infection Therapy(PROVEIT-TIMI22)[J].Am J Cardiol,2002,89:860-861.
[11]HOSHIDA S,NISHINO M,TAKEDA T,et al.A persistent increase in C-reactive protein is a risk factor for restenosis in patients with stable angina who are not receiving statins[J].Atherosclerosis,2004,173(2):285-290.
[12]PATTI G,PASCERI V,COLONNA G,et al.Atorvastatin pretreatmemimproves outcomes in patients with ACS undergoing early pereutaneous coronary intervention:results of the ABMYDA--ACS irandomized trial[J].J Am Coli Cardiol,2007,49:1272-1278.
[13]PASCERI V,PATTI G,NUSCA A,et al.Randomized trial of atorvaatatin for reduction of myocardial damage during coronary intervention results from the ARMYDA study[J].Circulation,2004,110:674-678.
[14]COHEN D E,ANANIA F A,CHALASANI N.An assessment of statin safety by hepatologists[J].Am J Cardiol,2006,97(8A):77C-81C.
