高效液相色谱法测定小儿清化丸中的绿原酸和芍药苷的含量*
2011-06-21薛士荣李玉仿孙燕燕
薛士荣,李玉仿,孙燕燕
(1.天津市大港区药品检验所,天津 300270; 2.天津市儿童医院,天津 300070)
小儿清降丸是天津市儿童医院传统成方制剂,是由生地黄、青黛、金银花、薄荷、赤芍等14味中药组成的传统蜜丸,具有清热解毒、养阴利咽的功效,用于急性咽炎,喉炎,急性扁桃体炎,内热外感发烧,伴有大便秘结者。绿原酸和芍药苷分别为该制剂中主要药物金银花和赤芍的有效成分,本实验采用高效液相色谱法测定绿原酸和芍药苷的含量,为该制剂的质量控制提供了可行的方法。
1 仪器和试药
岛津高效液相色谱仪 LC-2010C,岛津高效液相色谱仪工作站LC-Solution(日本岛津公司)。对照品均来自中国药品生物制品检定所,绿原酸批号为110753-200413,芍药苷批号为110736-200934(含量95.7%)。甲醇、磷酸均为色谱纯,水为纯化水。小儿清降丸(天津市儿童医院,批号为20101102、20110301、20110302)。
2 方法与结果
2.1色谱条件 色谱柱:Diamond C18柱(250 mm×4.6 mm,5 μm);柱温:35 ℃;流动相:乙腈-0.4%磷酸液(15∶85);流速:1.0 ml/min;检测波长:绿原酸327 nm,芍药苷230 nm;进样量:绿原酸10 μl,芍药苷20 μl。
2.2绿原酸含量测定
2.2.1溶液制备
2.2.1.1对照品溶液的制备 取绿原酸对照品置五氧化二磷减压干燥器中干燥12 h后,精密称取4.95 mg置250 ml量瓶中,加50%甲醇溶解并稀释至刻度,摇匀,制成每1 ml含0.019 8 mg/ml绿原酸对照品溶液。
2.2.1.2供试品溶液的制备 取“重量差异”项下的本品,剪碎,混匀,取约0.5 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇50 ml,密塞,称定重量,超声处理(功率250W,频率40 kHz)30 min,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液即得。
2.2.1.3阴性对照溶液的制备 按处方比例及制法,制备不含金银花的阴性样品,取相当于供试品的量,按照供试品溶液制备项下的方法制备阴性样品溶液。分别吸取对照品溶液、供试品溶液和阴性样品溶液,按上述色谱条件测定,结果阴性样品溶液在绿原酸峰的位置上没有干扰,见图1。
2.2.2线性关系考查 分别精密吸取含有0.019 8 mg/ ml绿原酸对照品溶液2、5、10、15、20、25和30 μl,按“2.1”项下的色谱条件,注入高效液相色谱仪,记录峰面积。以进样量(μg)为横坐标,峰面积为纵坐标,求得绿原酸回归方程为:Y=3 286 358.7X-317.9(r=0.999 9)。结果表明:绿原酸在0.039 6~0.594 0 μg范围内线性关系良好。

1.绿原酸
2.2.3精密度试验 取“2.2.1.1”项下对照品溶液,按“2.1”项下色谱条件分析,连续进样6次,测得峰面积值的RSD为0.05%。
2.2.4重复性试验 取同一批样品(批号20101102)6份,按“2.2.1.2”项下配制,采用“2.1”项下色谱条件测定绿原酸的含量,结果测得绿原酸的平均含量为1.647 7 mg/g ,RSD为0.96%。
2.2.5稳定性试验 取样品(批号20101102),按“2.2.1.2”项下配制,每隔4 h进样1次,共5次,结果样品在16 h内无明显变化,RSD中0.10%。
2.2.6回收率试验 精密称取已知含量同一批样品(批号20101102)约0.25 g,共6份,分别精密加入含有0.007 92 mg/ml绿原酸对照品溶液50 ml,按“2.2.1.2”项下配制,按“2.1”项下色谱条件测定绿原酸的含量,绿原酸的平均回收率为99.50% ,RSD为0.68%。结果见表1。
2.2.7样品测定 取小儿清降丸3批,按“2.2.1.2”项下供试品溶液制备方法制成供试品溶液,按“2.1”项下色谱条件测定绿原酸的含量,测定结果见表2。
2.3芍药苷含量测定
2.3.1溶液制备

表1 绿原酸加样回收试验结果

表2 绿原酸含量测定结果
2.3.1.1对照品溶液的制备 精密称取芍药苷对照品4.30 mg,置50 ml量瓶中,加稀乙醇溶解并稀释至刻度,摇匀,制成每1 ml含0.082 3 mg芍药苷对照品溶液。
2.3.1.2供试品溶液的制备 取“重量差异”项下的本品,剪碎,混匀,取约1 g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25 ml,密塞,称定重量,超声处理(功率250W,频率40 kHz)30 min,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液即得。
2.3.1.3阴性对照溶液的制备 按处方比例及制法,制备不含赤芍与丹皮酚的阴性样品,取相当于供试品的量,按照供试品溶液制备项下的方法制备阴性样品溶液。
分别吸取对照品溶液、供试品溶液和阴性样品溶液,按上述色谱条件测定,结果阴性样品溶液在芍药苷峰的位置上没有干扰,见图2。
2.3.2线性关系考查 分别精密吸取含有0.082 3 mg/ml芍药苷对照品溶液2、5、10、15、20和30 μl,按“2.1”项下的色谱条件,注入高效液相色谱仪,记录峰面积。以进样量(μg)为横坐标,峰面积为纵坐标,求得芍药苷回归方程为:Y=659 305.6X-4 815.5(r=0.999 9)。结果表明:芍药苷在0.164 6~2.469 0 μg范围内线性关系良好。
2.3.3精密度试验 取“2.3.1.1”项下的溶液,按“2.1”项下色谱条件分析,连续进样6次,测得峰面积RSD为1.09%。
2.3.4重复性试验 取同一批样品(批号20101102)6份,按“2.3.1.2”项下方法配制,采用“2.1”项下色谱条件测定芍药苷的含量,结果测得芍药苷的平均含量为1.906 8 mg/g,RSD为1.13%。

1. 芍药苷
2.3.5稳定性试验 取样品(批号20101102),按“2.3.1.2”项下配制,每隔4 h进样一次,共5次,结果样品在16 h内无明显变化,结果RSD为1.11%。
2.3.6回收率试验 精密称取已知含量同一批样品(批号20101102)约0.5 g,共6份,分别精密加入含有0.041 34 mg/ml芍药苷对照品溶液25 ml,按“2.3.1.2”项下配制,按“2.1”项下色谱条件测定芍药苷的含量,芍药苷的平均回收率为99.32%,RSD为0.72%。结果见表3。

表3 芍药苷加样回收试验结果
2.3.7样品测定 取小儿清降丸3批,按“2.3.1.2”项下供试品溶液制备方法制成供试品溶液,按“2.1”项下色谱条件测定芍药苷的含量,测定结果见表4。
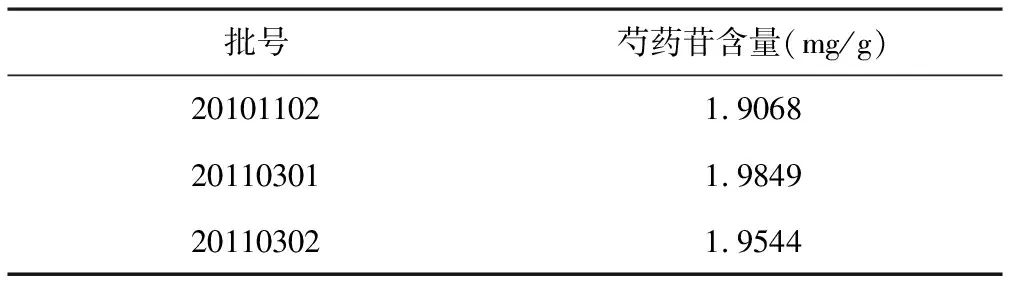
表4 芍药苷含量测定结果
3 讨论
3.1检测波长的选择 绿原酸、芍药苷经紫外扫描可知,绿原酸最大吸收波长为327 nm,芍药苷的最大吸收波长为230 nm,故选择以最大吸收波长作为检测波长。
3.2样品提取方法的选择[1]用50%甲醇同时提取样品中绿原酸、芍药苷,选择双波长同时测定,绿原酸峰形、峰面积都很好,但芍药苷峰面积太小,结果易出现偏差,故选择分别提取。提取芍药苷时分别用纯甲醇和稀乙醇两种溶剂,相同取样量、超声提取时间,稀乙醇溶解比纯甲醇溶解完全,故提取芍药苷选择稀乙醇。
本品为中药复方制剂,成分极为复杂,采用HPLC法来分别测定制剂中绿原酸和芍药苷的含量。结果表明,方法简单、灵敏度高、重现性好,所测的结果准确,可用于该制剂的质量控制。
1 中国药典.一部.2010:96,147,205
