清气凉营注射液中15个成分的HPLC/ESI/MS分析研究
2011-05-26任爱农顾学红王大为
任爱农, 顾学红, 王大为
(1.江苏省中医药研究院,江苏南京 210028;2.江苏大学药学院,江苏镇江 212013)
清气凉营注射液是由大青叶,大黄,金银花,知母,野菊花,淡竹叶经提取加工制成的静脉注射液,具有清气泄热、凉营化瘀等功效。临床上治疗流行性出血热早期发热(气分证及气营两燔证)效果显著。中医学理论认为,“气”、“营”是指温热病的病理发展阶段,由于气分及气营两燔阶段时,病邪已到气,并多波及营分,故应用清气凉营注射液治疗。对于清气凉营注射液中结合型大黄酸的HPLC研究之前已有报道[1],而随着液质联用仪的广泛应用,尤其是电喷雾(ESI)等软电离技术的快速发展,HPLC/MS直接用于中药复杂体系中化合物的定性分析已逐渐成为中药研究的热点技术[2-6]。本实验对清气凉营注射液中极性类成分和苷元类成分进行分析,采用HPLC/ESI/MS方法,对清气凉营注射液HPLC图谱上所显示的特征谱峰进行分析,旨在弄清清气凉营注射液中特征谱峰的结构及其归属,为进一步丰富清气凉营注射液全方的内涵奠定一定的基础。
1 材料与方法
1.1 药品和药材
清气凉营注射液由泰州苏中药业集团股份有限公司生产提供。大青叶来自十字花科植物菘蓝Isatis indigoticaFort.的干燥叶;金银花来自忍冬科植物忍冬Lonicera japonicaThunb.的干燥花蕾或带初开的花;大黄来自蓼科植物掌叶大黄Rheum palmatumL.、唐古特大黄Rheum tanguticumMaxim.ex Balf.或药用大黄Rheum officinaleBaill.的干燥根及根茎;野菊花来自菊科植物野菊Chrysanthemum indicumL.的干燥头状花序;知母来自百合科植物知母Anemarrhena asphodeloidesBge.的干燥根茎;淡竹叶来自禾本科植物淡竹叶Lophatherum gracile Brongn.的干燥茎叶。以上药材均由任爱农教授鉴定。
1.2 试剂与仪器
Waters2695型液相色谱仪(四元泵、在线脱气及自动进样系统、2996型二极管阵列检测器);Micromass Quattro micro质谱仪,串联四极杆质谱检测器,ESI接口,Masslynx 4.0数据处理系统;Milli-Q纯水器(美国)。除甲醇为色谱纯外,其余试剂均为分析纯。绿原酸(S1,批号:110821-200413)和大黄酸(S2,批号:0757-200206)对照品购自于中国药品生物制品检定所。
1.3 色谱条件
1.3.1 极性类成分色谱条件 色谱柱是Promosil C18柱(4.5 mm × 250 mm,5 μm);流动相:甲醇-0.2%醋酸水溶液,梯度洗脱见表1;进样量:10 μL;洗脱时间:90 min;检测波长:325 nm;柱温:30℃;流速:0.8 mL/min。
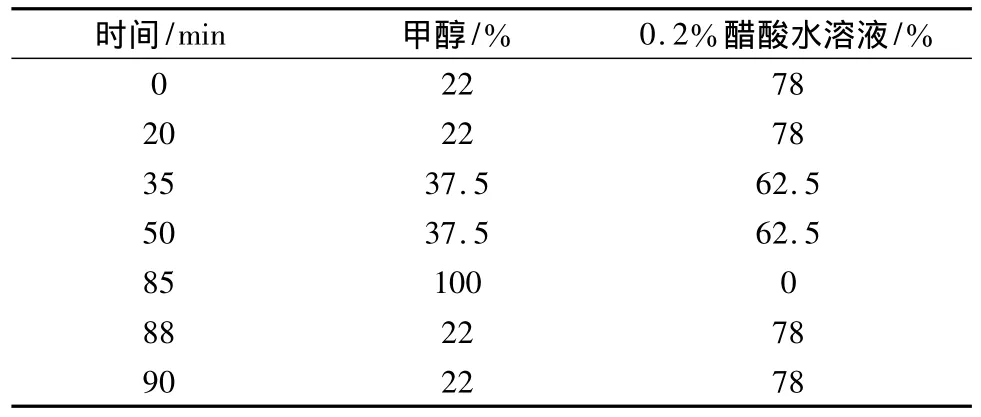
表1 梯度洗脱情况Tab.1 Gradient elution
1.3.2 苷元类成分色谱条件 色谱柱是Promosil C18柱(4.5 mm × 250 mm,5 μm);流动相:甲醇-0.2%醋酸水溶液,梯度洗脱见表2;进样量:10 μL;洗脱时间:60 min;检测波长:440 nm;柱温:30℃;流速:0.8 mL/min。

表2 梯度洗脱情况Tab.2 Gradient elution
1.4 质谱条件
电喷雾离子化(ESI)源;离子源温度:120℃;正负离子同时检测;脱溶剂气(N2)流速:500 L/h;锥孔气(N2)流速:50 L/h;毛细管电压:3.0 kV;扫描范围m/z:150~650;锥孔电压:30 V;碰撞气体为氩气(Ar);碰撞室能量:40 V。
1.5 供试品的制备
1.5.1 极性类成分的制备 取清气凉营注射液2 mL,过 0.45 μm 微孔滤膜,备用。
1.5.2 苷元类成分的制备 取清气凉营注射液10 mL,加过氧化氢1 mL,盐酸2 mL,加热回流1 h,冷却至分液漏斗中,乙醚提取3次,每次20 mL,合并提取液,并水洗至中性,挥尽乙醚,加甲醇定容至2 mL作为供试品溶液,过0.45 μm微孔滤膜,备用。
1.5.3 对照品的制备 取绿原酸对照品,加甲醇制成每1 mL含0.1 mg的溶液作为对照品溶液。取大黄酸对照品,加甲醇制成每1 mL含0.2 mg的溶液作为蒽醌类成分检测的对照品溶液。
2 结果与讨论
2.1 HPLC/UV检测
实验中对清气凉营注射液中极性类成分和苷元类成分进行分析,仅用单组分流动相很难达到很好的效果,因此选用以上含两种不同组分的流动相进行分析。通过比较,酸性条件下指纹图谱中的峰形较好,出峰时间稳定,所以选择甲醇-0.2%醋酸水溶液作为流动相。在极性类成分分析中,因为结果中多含有酸性成分如绿原酸及其异构体等,所以在325 nm处出现的谱峰信息较多,并且峰形较好;而在苷元类成分分析中,因为多以方中大黄中含有的蒽醌类为主,所以选择在440 nm处观测,该波长下峰形较好,出峰时间稳定。结果见图1。
2.2 图谱中各峰药材归属
按照注射液制备工艺分别提取制备了只含有单味药材的注射液,而含苷元类药材按照注射液提取工艺提取后再进行水解并分析,以考察药材与注射液之间的相关性,金银花,野菊花,知母,淡竹叶按照1.3.1项下条件进样,大黄按照1.3.2项下条件进样,结果见图2。由图2A 可以看出峰1,2,3,4,6,7,9在金银花与野菊花中均有出现,而峰10,11在野菊花中出现,其相对应的紫外吸收也相同,峰5未在任何药材中出现,可能是在注射液制备过程中产生的新的化合物。由图2B可以看出12,13,14,15均在大黄药材中出现,推测这4个峰是大黄蒽醌类化合物。
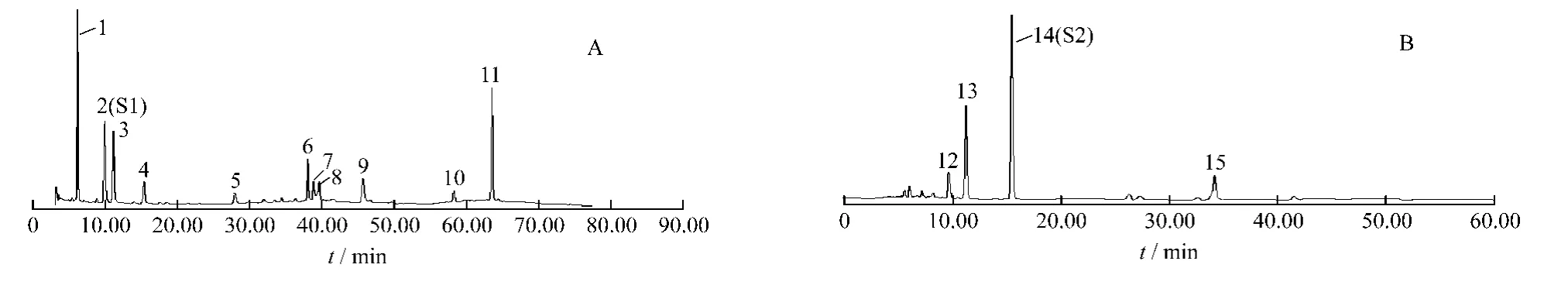
图1 清气凉营注射液HPLC/UV指纹谱图Fig.1 The HPLC/UV fingerprint of Qingqi Liangying Injection

图2 清气凉营注射液与药材指纹图谱相关性比较Fig.2 The relativity between the fingerprints of Qingqi Liangying Injection and medical material
2.3 HPLC/MS检测
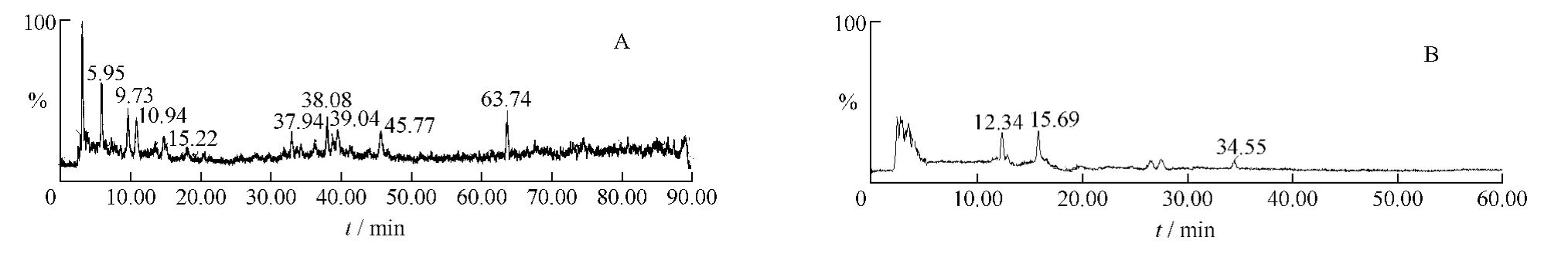
图3 清气凉营注射液HPLC/MS谱图ESI(-)Fig.3 The HPLC/MS spectra of Qingqi Liangying Injection ESI(-)
分别以正、负离子模式全面检测清气凉营注射液中各类化合物。经条件优化,最终确定了1.4和1.3项下的色谱和质谱条件。结果显示大部分峰的负离子吸收比正离子吸收明显。清气凉营注射液的HPLC/MS指纹图谱见图3。通过所得到的一级质谱碎片离子数据并参考相关文献,对注射液HPLC图谱中的部分共有峰进行了初步定性分析。
2.3.1 极性类成分的质谱分析 根据绿原酸对照品峰的保留时间和紫外光谱数据,推出峰2为绿原酸,而质谱数据(在负离子模式下有响应较高的253峰[M-H]-离子,而在正离子模式下有277峰[M+Na]+离子)也进一步确定了峰2是绿原酸;峰1和峰3具有与绿原酸相同的响应峰,即在负离子模式下有响应较高的253峰[M-H]-离子,和正离子模式下有277峰[M+Na]+离子,推测峰1和峰3为绿原酸的同分异构体新绿原酸和隐绿原酸,根据文献[7-8]可以推断出峰1为新绿原酸,峰3为隐绿原酸。
峰4的[M-H]-离子的m/z为179,而其正离子吸收不明显,但其紫外吸收与绿原酸相近,都在193,218,323 nm出有最大吸收,并且药材归属到金银花与野菊花中,因此推测为咖啡酸。
峰6,峰7和峰9负离子模式下具有相同的515峰[M-H]-离子并且在正离子模式下同样具有540峰[M+Na]-离子,推测为异绿原酸异构体,通过文献[8-9],异绿原酸B和异绿原酸A的保留时间相近,且异绿原酸B先于异绿原酸A出峰,从而可以推出峰6为异绿原酸B,峰7为异绿原酸A,而峰9为异绿原酸C。
峰8的负离子模式下有较高的447峰[M-H]-离子,且在正离子模式下有较高的449峰[M+H]+离子和287峰[M-glu+H]+离子,而金银花及其野菊花中都含有丰富的木犀草苷[10-11],因此我们推测峰8为木犀草苷。
峰11负离子模式下有较高的591峰[M-H]-离子,正离子模式下具有较高的593峰[M+H]+离子,因此推测为蒙花苷。
峰5和峰10在正负离子模式下均无明显吸收。
2.3.2 苷元类成分的质谱分析 根据大黄酸对照品峰的保留时间和紫外光谱数据,推出峰14为大黄酸,而质谱数据(在负离子模式下有响应较高的283峰[M-H]-离子和 239[M-CO2-H]-离子,而在正离子模式下有285峰[M+Na]+离子)也进一步确定了峰14是大黄酸。
峰12在正负离子模式下均无明显吸收。
峰13和峰15的负离子模式下有都较高的269峰[M-H]-离子,且在正离子模式下都有较高的271峰[M+H]+离子,猜测这两个化合物为大黄蒽醌类中的同分异构体芦荟大黄素和大黄素,根据文献[12-13],可以看出芦荟大黄素先于大黄素出峰,因此峰13为芦荟大黄素,而峰15为大黄素。总结果见表3。
3 结论
本实验通过HPLC/ESI/MS联用的方法对清气凉营注射液中极性类成分和苷元类成分进行定性检测,结果显示该方法将检测到的15个峰中的12个峰的化学结构初步推断出来,极性类成分中大部分为绿原酸及其异构体和异绿原酸及其异构体,而苷元类成分全部是大黄蒽醌类化合物,这一结果为清气凉营注射液的质量控制提供了依据。同时由于该方法能够同时实现有效组分的良好分离并提供各峰的组成和结构信息,在中药复杂体系研究及其质量控制方面具有非常广阔的应用前景。
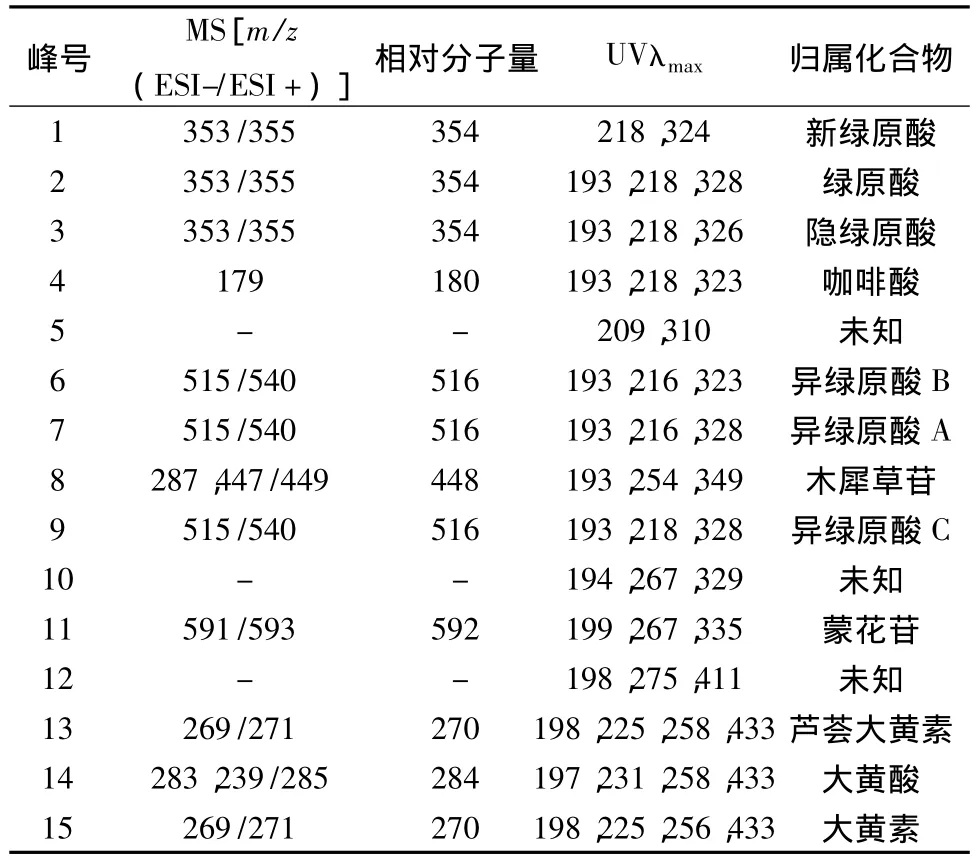
表3 峰1-15的质谱数据和紫外数据Tab.3 The MS and UV date of the peaks 1-15
[1]任爱农,鞠建明,陈 廉.反相高效液相色谱法测定清气凉营注射液中结合型大黄酸的含量[J].时珍国医国药,1998,9(6):528-529.
[2]邵清松,胡润淮.HPLC-MS联用技术在中药指纹图谱研究中的应用[J].中国药房,2007,18(12):938-940.
[3]许海棠,徐远金.HPLC/MS测定蒲公英颗粒中绿原酸、咖啡酸和阿魏酸的含量[J].化学通报,2008(6):415-419.
[4]董 静,王 弘,万乐人,等.高效液相色谱-电喷雾-离子阱-飞行时间质谱分析鉴定中药虎杖中的主要化学成分[J].色谱,2009,27(4):425-430.
[5]张 炜,盛彧欣,张金兰,等.应用HPLC-DAD/MS技术评价中药天麻的质量[J].药学学报,2007,42(4):418-423.
[6]周 慧,宋凤瑞,刘志强,等.ESI-MS和HPLC-UV法研究大黄、黄柏、赤芍炮制前后化学成分变化[J].药物分析杂志2009,29(6):883-888.
[7]田晨煦,徐小平,廖丽云,等.高效液相色谱-串联质谱法分离鉴定绿原酸及其相关杂质[J].色谱,2007,25(4):496-500.
[8]Aezet T,Puigmaia M.High-performance liquid chromatography of caffeoylquinic acid derivatives of Cynara scolymus L.leaves[J].J Chromatogra,1985,348:447-453.
[9]刘永刚,卢建秋,高晓燕,等.高效液相色谱-电喷雾电离质谱法分析不同时期金银花中酸性成分及含量变化[J].中国药房,2006,17(22):1756-1757.
[10]张 雪,何丙辉,杨 宪,等.HPLC法测定金银花中常春藤皂苷元、齐墩果酸、槲皮素、木犀草苷和绿原酸[J].中草药,2008,39(10):1576-1577.
[11]谭晓杰,贾 英,李 清,等.RP-HPLC法同时测定野菊花中木犀草素-7-O-葡萄糖苷和蒙花苷[J].中草药,2006,37(8):1261-1262.
[12]薛小平,鹿燕敏,王 倩,等.HPLC法测定清热解毒方芦荟大黄素、大黄酸、大黄素、大黄酚及大黄素甲醚的含量[J].中国实验方剂学杂志,2009,15(7):6-8.
[13]许风国,刘 颖,宋 瑞,等.LC-MS/MS法研究大承气汤与其君药大黄物质基础间的相关性[J].中国药科大学学报,2008,39(2):136-141.
