高效液相二极管阵列检测法同时测定丹参粉针剂中4种水溶性成分的含量
2011-05-26褚文静杜秀芳黄喜茹
王 伟, 张 雪, 褚文静, 杜秀芳, 许 祺, 黄喜茹
(河北医科大学药学院,河北石家庄 050017)
丹参粉针剂是由中药丹参加工制成,具有扩张血管、增加血流量、通脉养心、活血化瘀的功效,临床用于心绞痛、冠心病等疾病的治疗[1]。丹参中的活性成分为脂溶性二萜醌类化合物和水溶性酚酸类化合物,而该制剂中的药效成分是水溶性酚酸类化合物,包括丹参素、原儿茶酸、原儿茶醛、迷迭香酸、迷迭香酸甲酯、咖啡酸、异阿魏酸、紫草酸、鼠尾草列醇和丹酚酸 A、B、C、D、E、F、G 等[2]。前4 种成分含量较高,是该制剂的主要药效成分。用反相高效液相色谱法测定其中原儿茶醛和丹参素的含量已见报道[3-4],此法只用 2 种药效成分作为质量控制的指标,不能综合评价药品的内在质量。用比色法测定此制剂或测定丹参有关制剂中水溶性酚酸总量的质量分析方法已有多篇报道[5-7],这些方法虽操作简单,但专属性差。本试验建立高效液相二极管阵列检测法同时测定丹参粉针剂中4种主要水溶性成分丹参素、原儿茶酸、原儿茶醛和迷迭香酸的含量,为综合评价该制剂的内在质量提供一种分析方法[8-10]。
1 仪器、样品与试剂
Agilent 1200高效液相色谱仪(二极管阵列检测器、柱温箱、四元泵、自动控温进样器)。Agilent化学工作站。JA1203A型电子天平(上海精密科学仪器有限公司)。TCQ-250超声波清洗器(北京医疗设备二厂)。
丹参素钠(批号110855-200405)、原儿茶酸(批号 110809-200503)、原 儿 茶 醛 (批 号 110810-200506)对照品,均由中国药品生物制品检定所提供,迷迭香酸对照品,购自四川成都曼思特生物科技有限公司,纯度98%以上。丹参粉针剂为市售品(批号 080410、06042201、07030202)。冰醋酸为分析纯,甲醇为进口色谱纯,水为重蒸水。
2 方法与结果
2.1 色谱条件 色谱柱:DiamonsilTM(钻石)C18(250 mm ×4.6 mm,5 μm);流动相:甲醇(A)-5%冰醋酸(B),梯度洗脱。洗脱程序 A:0~7 min,30%;7~10 min,线性改变至 50%,10~25 min,50%(A+B=100%)。停止时间25 min,后运行10 min。柱温为30℃,流速:1.0 mL/min,检测波长:298 nm,进样量为20 μL。在此色谱条件下,理论塔板数按丹参素、原儿茶酸、原儿茶醛和迷迭香酸计算均大于6 000。4组分均达到基线分离(R>1.5),其色谱图见图1。
2.2 供试品溶液的制备 精密称取丹参粉针剂62.22 mg置50 mL量瓶中,用20%甲醇溶解稀释至刻度,摇匀,用0.45 μm微孔滤膜过滤,取得续滤液,即为供试品溶液。
2.3 对照品溶液的制备 分别精密称取丹参素、原儿茶酸、原儿茶醛、迷迭香酸对照品适量,置于25 mL量瓶中,用20%甲醇稀释至刻度,配制成浓度分别为 109.6,148.4,35.08 μg/mL 和 129.6 μg/mL的对照品贮备液。

图1 对照品(A)和样品(B)的HPLC色谱图1.丹参素 2.原儿茶酸 3.原儿茶醛 4.迷迭香酸Fig.1 Chromatogram of reference substances(A)and sample(B)1.danshensu 2.protocatechuic aicd 3.protocatechuic aldehyde 4.rosmarinic acid
分别精密吸取上述丹参素、原儿茶酸、原儿茶醛、迷迭香酸贮备液3、0.1、0.5和0.3 mL置于10 mL量瓶中,用20%甲醇溶解稀释至刻度,摇匀,配制成浓度分别为 32.88、1.484、1.754、3.888 μg/mL的混合对照品溶液。
2.4 标准曲线测定 取混合对照品溶液用0.45 μm微孔滤膜过滤后,按以上色谱条件分别进样5、10、20、30、40、50、60、70、80 μL,记录色谱峰面积,以峰面积A对进样量C(μg)进行线性回归,结果:丹参素的线性方程为A=42.499C-0.437 8,r=0.999 9,线性范围为 0.164 4 ~2.630 μg;原儿茶酸的线性方程为A=1 836.8C-0.843 8,r=1.000,线性范围为0.007 420~0.118 7 μg;原儿茶醛的线性方程为A=2 512.5C-0.461 9,r=1.000,线性范围为0.008 770~0.140 3 μg;迷迭香酸的线性方程为A=577.19C+0.043 8,r=1.000,线性范围0.019 44 ~0.311 0 μg。
2.5 精密度和稳定性试验 按照上述色谱条件,取线性关系项下对照品溶液,各取20 μL注入高效液相色谱仪,连续进样5次,丹参素、原儿茶酸、原儿茶醛和迷迭香酸的峰面积RSD分别为0.45%、0.16%、0.074%和0.094%。取同一供试品溶液,分别在 2、4、6、8、10、12、14 h 进样 20 μL,记录峰面积,结果丹参素、原儿茶酸、原儿茶醛和迷迭香酸的峰面积 RSD分别为0.16%、0.50%、0.051%和0.16%。
2.6 最低检测限 取混合对照品溶液逐步稀释后,注入高效液相色谱仪,以峰高为基线噪音3倍计,丹参素、原儿茶酸、原儿茶醛和迷迭香酸的最低检测浓度分别为 38、0.80、0.63、1.8 μg/mL。
2.7 重复性试验 取批号为080410的丹参粉针剂,按照2.2项下方法制备5份供试品溶液,分别进样20 μL,测得丹参素、原儿茶酸、原儿茶醛和迷迭香酸的平均含量分别为213.5 mg/g(RSD=0.13%),1.278 mg/g(RSD 为 0.67%),8.451 mg/g(RSD为0.32%)和10.49 mg/g(RSD为0.15%)。
2.8 加样回收率试验 精密量取已知含量的供试品溶液(080410)3份,分别加入一定量的混合对照品溶液,按照上述色谱条件测定,计算加样回收率。结果见表1。
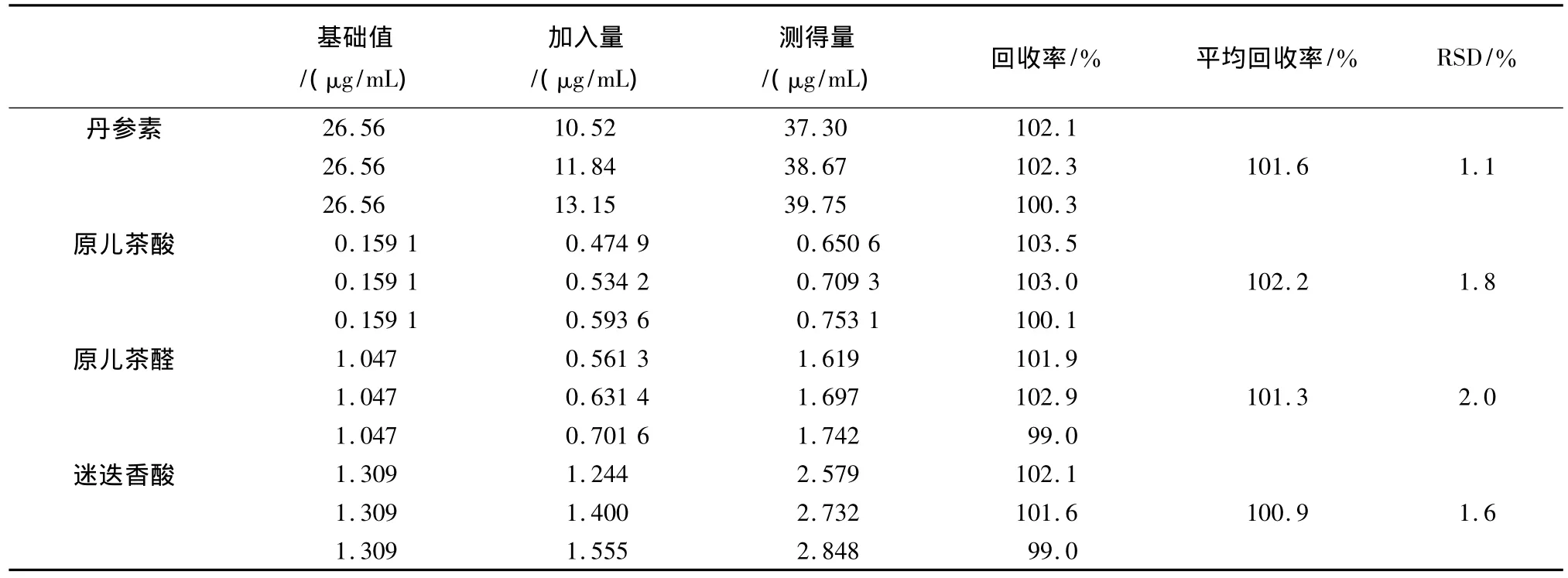
表1回收率测定结果Tab.1 Determination results of recovery(n=3)
2.9 样品测定 取3个批号丹参粉针剂,按照2.2项下方法制备供试品溶液,按上述色谱条件分别进样测定,用外标法计算含量。结果见表2。
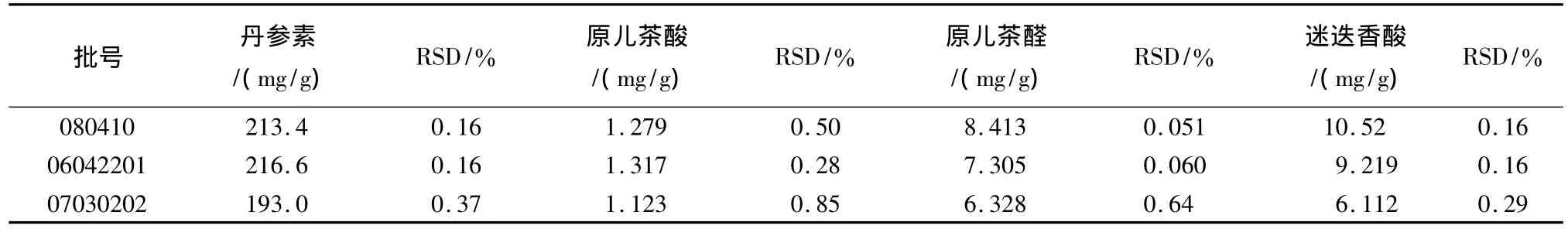
表2样品测定结果Tab.2 Determination results of samples(n=5)
3 讨论
经二极管阵列检测器对4种成分进行全波长扫描,丹参素和原儿茶醛的最大吸收波长为281 nm,原儿茶酸的最大吸收峰波长为260 nm,次强吸收峰波长为298 nm,迷迭香酸的最大吸收波长为330 nm。为兼顾4种成分的检测灵敏度,本试验考察了采用不同检测波长时检出的信号强度,结果在298 nm各组分信号较强,且基线稳定,因此采用298 nm为检测波长。
从样品测定结果看,不同厂家,不同批号的丹参粉针剂中4种水溶性酚酸类成分的含量有一定差异,其主要原因是原料丹参的品质受产地、生长期、加工、提取条件等因素的影响。本试验建立高效液相二极管阵列检测法同时测定丹参粉针剂中丹参素、原儿茶酸、原儿茶醛和迷迭香酸4种有效成分的含量,此法可更全面评价该药品的质量。
[1]郑虎占.中药现代研究与应用[M].第二卷.北京:学苑出版社,1997:1099.
[2]张英锋,王燕革,马子川,等.丹参活性化学成分的研究[J].化学世界,2009,10:638-640.
[3]戴 忠,钱忠直.HPLC法测定丹参粉针剂中丹参素及原儿茶醛含量[J].中成药,1996,18(6):10-11.
[4]关大卫.HPLC法测定注射用丹参粉针中丹参素的含量[J].药物分析杂志,1994,14(3):36-37.
[5]黄喜茹,曹 冬,樊淑彦,等.NaNO2-Al(NO3)3显色测定丹参及其制剂中水溶性酚酸总量[J].化学试剂,2005,27(12):745-746.
[6]李广胜,王光新,赵牛和.丹参口服液中总酚酸性成分的含量测定[J].时珍国医国药,2001,12(8):683.
[7]王胜春,蒋永培,迂苏宁,等.五灵丸中丹参总酚性成分的测定[J].第四军医大学学报,1993,14(5):386.
[8]张 烨,郑 颖,王一涛.应用改进的质量评价方法考察复方丹参制剂[J].中成药,2009,31(12):1855-1860.
[9]吕文海,王 姣,张力中,等.山东丹参饮片产地加工方法与质量分析[J].中成药,2004,26(8):637.
[10]褚文静,张 雪,黄喜茹,等.RP-HPLC法测定湿毒清片中7种活性成分[J].中草药,2010,41(11):1809-1811.
