BD方案与VAD方案治疗多发性骨髓瘤的疗效比较
2011-05-25肖萌何娟李艳苏楠徐赢东王玉婷王庆玲李树国
肖萌,何娟,李艳,苏楠,徐赢东,王玉婷,王庆玲,李树国
(中国医科大学附属第一医院1.血液科;2.输血科;3.泌尿外科,沈阳 110001)
多发性骨髓瘤(multiple myeloma,MM)是浆细胞恶性克隆增生性疾病[1],多发生于中老年人,其发病率分别占全部恶性肿瘤和血液系统肿瘤的1%和10%,并呈逐年升高趋势[2]。目前,联合化疗是治疗MM的主要手段,尽管化疗方案不断改进,且化疗强度不断提高,却仍未取得满意效果。硼替佐米(bortezomib)是一种26S蛋白酶体抑制剂,通过多种机制杀伤骨髓瘤细胞。本研究比较了硼替佐米联合地塞米松方案(BD方案)与传统的VAD方案治疗MM的临床疗效及副作用,为今后MM的治疗提供新的临床依据。
1 材料与方法
1.1 一般资料
收集2005年5月至2009年6月在中国医科大学附属第一医院血液内科住院的MM患者120例,均符合MM的诊断标准[3]。根据治疗方案分为:(1)BD组(n=37):其中初治16例,复发/难治21例;(2)VAD 组(n=83):其中初治 39例,复发/难治 44例。2组患者性别、年龄、免疫分型和临床分期比较差异均无统计学意义(P>0.05)。见表1。
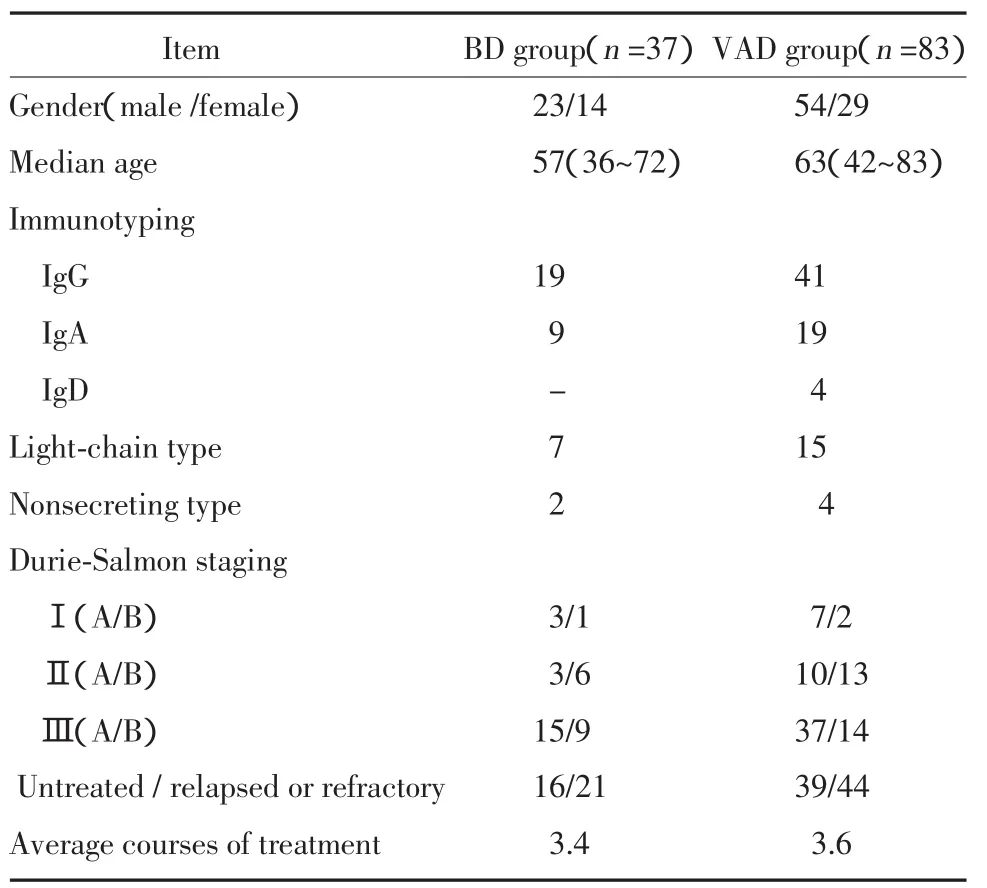
表1 2组MM患者基线资料比较(n)Tab.1 Comparison of baseline informations of two groups(n)
1.2 治疗方案
BD 方案:硼替佐米 1.3 mg/m2第 1、4、8、11 天静推;地塞米松20 mg/d第1~4、8~11、17~20天静滴,21 d为1个疗程;VAD方案:长春新碱0.4 mg/d,表阿霉素10 mg/d,地塞米松20 mg/d,第1~4天静脉滴注,28 d为1个疗程。
1.3 观察指标
治疗前后监测血常规、肝功能、肾功能、电解质、免疫固定电泳、血浆蛋白电泳、免疫球蛋白定量、β2微球蛋白(β2-microglobulin,β2-MG)、血及尿轻链定量、尿本-周氏蛋白、尿常规、骨髓细胞形态学检查、骨骼X线检查等。治疗期间观察两组的不良反应。
1.4 随访
累积生存时间由2005年5月使用硼替佐米或VAD方案治疗开始,以死亡时间为终止时间,随访至2010年6月30日。
1.5 疗效判定
治疗至少4个疗程后,根据EBMT/ABMT标准[4]进行疗效评价,同时按世界卫生组织(WHO)标准判断不良反应。
1.6 统计学分析
应用SPSS17.0统计软件包。2组之间率及构成比的比较采用χ2检验,采用Kaplan-Meier生存曲线进行生存分析,采用Log-rank检验比较2种方案的的生存率。全部统计方法均采用双侧检验,P<0.05为差异有统计学意义。
2 结果
2.1 疗效观察
37例接受BD方案治疗的患者中,34例病情得到不同程度的缓解,骨痛、贫血、肾功能不全、高钙血症等均得以改善;83例接受VAD方案治疗的患者中,55例病情得到缓解。如表2所示,BD组总有效率为91.9%,平均起效疗程数为2.06;VAD组总有效率为66.3%,平均起效疗程数为3.09。2组总有效率之间比较差异有统计学意义(χ2=8.772,P<0.05)。
BD组16例初治患者中,6例完全缓解或接近完全缓解(complete response or near complete response,CR/nCR),8 例部分缓解 (partial response,PR),1例微小反应(minimal response,MR),1例无反应(non-response,NR),有效率为 93.8%;VAD 组39例初治患者中,6例CR/nCR,15例PR,5例MR,8例NR,5例PD,有效率为66.7%。2组方案与初治患者的有效率比较差异有统计学意义(χ2=4.386,P<0.05)。见表 3。
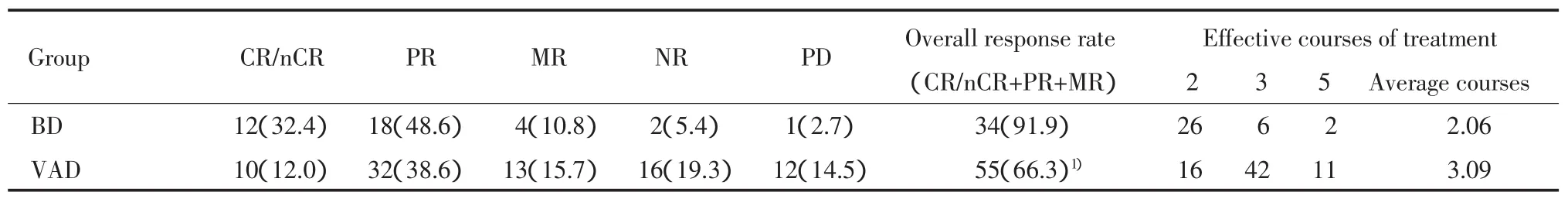
表2 两组患者总疗效比较(n/%)Tab.2 Comparison of overall response rates of two groups(n/%)

表3 两组初治患者疗效比较(n/%)Tab.3 Efficacy comparison of newly diagnosed patients in the two groups(n/%)
BD组21例复发/难治患者中,6例CR/nCR,10例PR,3例MR,1例NC,1例PD,有效率为90.5%;VAD组44例复发/难治患者中,4例CR/nCR,17例PR,8例MR,8例NC,7例PD,有效率为65.9%。2组方案与复发/难治患者的有效率比较差异有统计学意义(χ2=4.442,P<0.05)。见表 4。

表4 两组复发/难治患者疗效比较(n/%)Tab.4 Efficacy comparison of relapsed/refractory patients in the two groups(n/%)
2.2 各项主要指标的比较
如表5所示,BD组血肌酐及β2-MG下降程度明显优于VAD组,差异有统计学意义(P<0.05);而BD组血红蛋白改变、M蛋白及骨髓瘤细胞下降程度虽优于VAD组,但由于BD组例数较少,与VAD组相比,差异无统计学意义(P>0.05)。
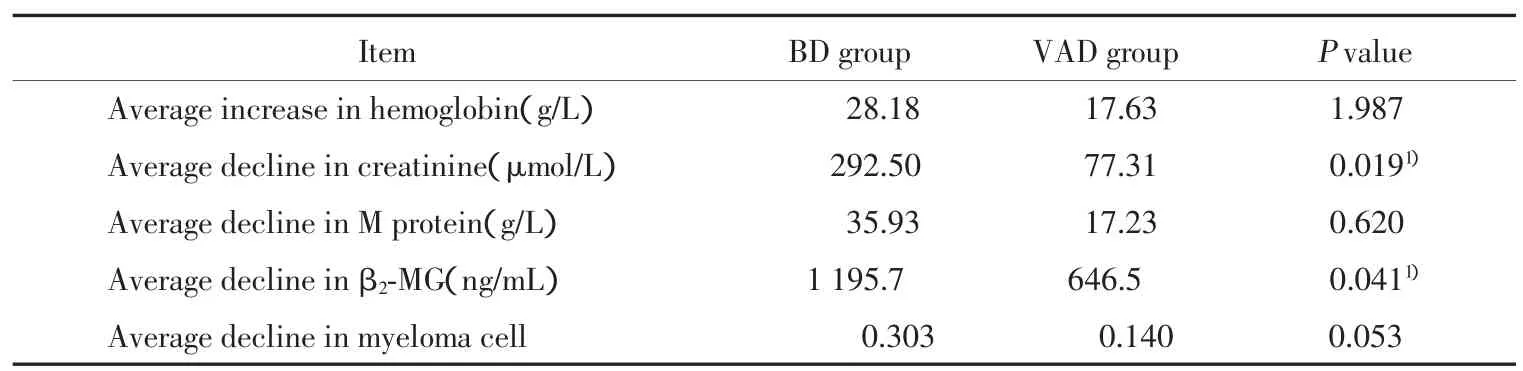
表5 两组主要疗效指标比较Tab.5 Comparison of primary endpoint of two groups
2.3 患者的生存期
自2005年5月患者开始使用硼替佐米或VAD方案治疗即纳入随访,截止至2010年6月30日,随访中位时间36个月(4~64个月),120例MM患者共存活35例,失访6例。
BD组中位生存期为43.5个月,2年和4年生存率分别为86.4%和47.3%,共死亡23例(初治9例,复治/难治14例)。6例获得CR/nCR的初治患者中仍有3例保持CR/nCR状态,6例获得CR/nCR的复发/难治患者中仍有2例保持CR/nCR状态。1例患者在完成7个疗程治疗后出现病情恶化。目前存活的14例患者正在接受后续的BD方案或其他方案进一步治疗,病情稳定。VAD组中位生存期为29.1个月,2年和4年生存率分别为64.3%和33.5%。共死亡62例(初治25例,复治/难治37例)。目前无1例CR/nCR,存活的21例患者中,1例发生严重的肺部感染,4例存在肾功能不全,均正在接受进一步治疗。
采用Kaplan-Meier生存曲线进行生存分析,经Log-rank检验发现,2组生存率比较差异有统计学意义(χ2=3.933,P<0.05),BD 组生存期长于 VAD组。见图1。

图1 两组的生存曲线Fig.1 Survival curves of two groups
2.4 不良反应
(1)血液毒性:BD组中7例(18.9%)患者发生骨髓抑制,表现为1~2级的外周血白细胞减少或血小板减少,血象在下一周期治疗前恢复正常,3例(8.1%)出现轻度感染;VAD组中19例(22.9%)患者出现2~3级骨髓抑制,16例(19.3%)出现不同程度的感染;(2)非血液毒性:BD组未出现心肝肾损害、恶心、呕吐等其他化疗药物常见的毒性反应,仅有轻度乏力、腹泻、便秘、外周神经病、带状疱疹,多≤2级,可自行消失或在延长用药间歇期后明显消失;VAD组20例(24.1%)患者出现不同程度的心肝肾毒性、恶心、呕吐、脱发、浮肿、指端麻木等不良反应,多为2~3级,绝大多数患者经积极治疗后好转。2组方案相比,BD组不良反应轻微,且患者均可耐受。
3 讨论
MM至今仍然是一种不可治愈的疾病,主要治疗手段是联合化疗,常用的方案有MP、VAD、M2,其中VAD方案是治疗MM的较佳方案。Barlogie等[5]于1984年首先报道,VAD方案治疗MM总反应率为70%,但很少CR。既往研究已明确疾病完全缓解率是长期生存的重要预后因素,为提高缓解率,各种新的治疗方案正在探索和不断改进中。
硼替佐米是26S属可逆性蛋白酶体抑制剂,为新型靶向MM及骨髓微环境的治疗药物,其作用机制基础为“泛素-蛋白酶体通道理论”,研究表明,它主要是通过以下途径对骨髓瘤细胞直接或间接产生抑制作用,最终使肿瘤细胞发生凋亡:(1)选择性地与蛋白酶体活性位点的苏氨酸结合,抑制蛋白媒体的20S亚单位的糜蛋白酶/胰蛋白酶活性,阻断其降解途径[6,7];(2)抑制核因子 κB(nuclear factor-kappa B,NFκB)的活性,从而使白细胞介素6等骨髓瘤细胞生长因子及黏附分子表达减少[8],同时降低破骨细胞活性,促进骨形成和骨质修复[9];(3)抑制内皮细胞生长,同时抑制新生血管形成,从而阻断对瘤细胞的血液供应,促使其凋亡[10];(4)抑制 DNA 的修复,逆转骨髓瘤细胞对激素和传统化疗的耐药[11,12]。2009年NCCN指南[13]已推荐硼替佐米联合地塞米松方案(BD方案)为难治复发MM的Ⅰ类治疗方案。Jean等[14]应用硼替佐米+口服地塞米松治疗18例初治MM患者,4个疗程后总反应率(CR+PR)为83%。另有研究发现,对初治MM应用硼替佐米与其他传统化疗药物联合有效率也高达84%~95%,优于单用硼替佐米[15]。早期获得完全缓解对患者的长期生存至关重要,尤其对于多药耐药以及心肝肾功能较差的老年患者应考虑尽早应用。苏楠等[16]报道,硼替佐米联合地塞米松治疗11例Ⅲ期多发性骨髓瘤患者的总有效率为90.9%,其中初治患者有效率为80.8%,复发/难治患者有效率为100%,其中2例患有严重肾功能不全和冠心病的患者经4个疗程的治疗后,贫血及肾功能不全得到较好的纠正。因此,硼替佐米为初发和复发难治MM患者提供了有效的治疗途径。
本研究比较了BD方案和VAD方案治疗MM的疗效和安全性,结果显示,2种方案均有明显疗效,但BD组总有效率为91.9%,其中初治患者有效率为93.8%,复发/难治患者有效率为90.5%,中位生存期为43.5个月,平均起效疗程数为2.06,起效较快,且能明显改善患者的肾功能,毒副作用小,患者耐受性良好,明显优于VAD组(P<0.05)。故BD方案是治疗MM更有效的方法。本临床研究结果也与国外的临床试验结果及观察报道接近[17]。此外,120例MM患者中有部分患者使用了沙利度胺。沙利度胺具有免疫调节和抗血管生成的作用,国内外多个临床中心对如何使用沙利度胺治疗MM进行了多次探讨,目前国内已有相关临床研究结果证实沙利度胺联合化疗可显著提高MM患者的总体生存期[18]。
已知明确影响MM的预后因素有:年龄>60岁,血红蛋白<60 g/L,血肌酐>180μmol/L,β2-MG>5.5 mg/L,Durie-Salmon分期Ⅲ期,骨髓中浆细胞>33%或有原始浆细胞出现或外周血出现浆细胞。本研究BD组中治疗效果不理想的患者存在严重肾功能损害或发生浆细胞白血病的情况。即使患者在使用硼替佐米治疗后能获得较好的疗效,但由于这些不良预后因素的存在,良好的疗效维持时间亦不能长久。
综上所述,与经典VAD方案相比,硼替佐米联合地塞米松治疗MM疗效明显,起效快,作用强,反应率和完全缓解率高,且不良反应少,安全性及耐受性好。硼替佐米开拓了MM治疗的新途径,值得临床推广使用。
[1]Greer JP,Foerster J,Lukens JN,et al.Wintrobe'sclinical hematology[M].11th ed,Philadelphia:Lippincott Williams&Wilkins,2004:2583-2636.
[2]Jayasundar R,Shah T,Vaishya S,et al.In vivoand in vitro MRspectroscopic profileof central neurocytomas[J].JMagn Reson Imaging,2003,17(2):256-260.
[3]张之南.血液病诊断及疗效标准[M].3版,北京:科学出版社,2007:232-234.
[4]Durie BL,Harousseau JH,Miguel JS,et al.International uniform response criteria for multiple myeloma [J].Leukemia,2006,20(9):1467-1473.
[5]Barlogie B,Johnston DA,Keating M,et al.Effectivetreatment of advanced multiplemyelomarefractory toalkylatingagents [J].NEngl JMed,1984,310(21):1353-1356.
[6]Adams J.The development of proteasome inhibitors as anticancer drugs[J].Cancer Cell,2004,5(5):417-421.
[7]Meister S,Schubert U,Neubert K,et al.Extensive immunoglobulin production sensitizes myeloma cells for proteasome inhibition[J].Center Res,2007,67(4):1783-1792.
[8]Boccadoro M,Morgan G,Cavenagh J.Preclinical evaluation of the proteasome inhibitor bortezomibin cancer therapy [J].Cancer Cell Int,2005,5(18):1-9.
[9]Van Cutsem E,Nowack IM,Lang I,et al.Randomized phaseⅢ study of irinotecan and 5-Fu/FA with or without cetuximab in the first-line treatment of patients with metastatic colorectal cancer(mCRC),the crystal trial[J].JClin Onco,2007,25(Suppl):164s.
[10]Roccaro AM,Hideshima T,Raje N,et al.Bortezomib targets multiple myelomaendothelial cells [J].Blood,2004,104(11):4903-4910.
[11]Mitsiades N,Mitsiades CS,Richardson PG,et al.The proteasome inhibitor PS-341 potentiates sensitivity of multiple myeloma cells to conventional chemotherapeutic agents:therapeuticapplications[J].Blood,2003,101(6):2377-2380.
[12]Ma MH,Yang HH,Parker K,et al.Theproteasomeinhibitor PS-341 markedly enhances sensitivity of multiple myeloma tumor cells to chemotherapeutic agents[J].Clin Cancer Res,2003,9(3):1136-1144.
[13]NCCN clinical practice guideline in oncology:multiple myeloma[S].National Comprehensive Cancer Network,2009.
[14]Harousseau JL,Attal M,Leleu X,et al.Bortezomib (Velcade)plus decamethasone as induction treatment prior to autologous stem cell transplantation in patientswith newly diagnosed multiplemyeloma:preliminary results of an IFM phase Ⅱ study[J].Blood,2004,104(11):1490[abstract].
[15]Richardson PG,Chanan-Khan A,Schlossman R,et al.A multicenterphaseⅡtrial of bortezomib in patients with previously untreated multiplemyeloma:efficacy with manageabletoxicity in patientswith unexpectedly high rates of baseline peripheral neuropathy[J].Blood,2005,106(11):2548[abstract].
[16]苏楠,于锦香,李艳,等.硼替佐米联合地塞米松治疗Ⅲ期多发性骨髓瘤临床观察[J].中国肿瘤临床与康复,2009,16(2):146-150.
[17]Manochakian R,Miller K,Chanan-Khan A.Clinical impact of bortezomib in frontline regimensfor patients with multiple myeloma[J].The Oncologist,2007,12(8):978-990.
[18]漆佩静,王亚非,李业楠,等.沙利度胺治疗102例多发性骨髓瘤患者的临床研究[J].中华血液学杂志,2008,29(4):226-229.
