静脉推注药物微粒污染的实验观察及干预
2011-05-23唐美玲钱云娟刘经纬黄海燕
唐美玲,钱云娟,刘经纬,黄海燕
(江苏省南通大学第二附属医院,1.肿瘤科;2.供应室;3.护理部,江苏南通,226001;4.江苏省南通市药检所,江苏南通,226006)
随着医院医疗质量管理的发展和患者对于治疗手段纯净度要求的提高,加强对静脉注射液中不溶性微粒控制及减少不溶性微粒对静脉注射患者的危害,愈来愈被医院和患者所重视,静脉注射途径给药是很常见的治疗方法。国外医疗单位规定[1],静脉注射的药物必须由安装微型滤器的注射器加注,并在洁净间或层流洁净台上操作。而目前国内静脉推注药物时缺乏过滤装置,病区静脉加药在普通治疗室进行,能成立配置中心使用层流设施的医疗单位为数不多,微粒污染可能无时不在。有不少文献报道,静脉注射药物不溶性微粒污染相当严重[2]。有实验表明[3],静脉加药操作使微粒增加数倍,加入粉剂的针剂比加入注射针剂的微粒更多,而且50 μ m以上的微粒也大大增加。为了提高用药安全性,作者对静脉推注用的复配液中不溶性微粒污染情况进行了实验观察,并设计一次性单独包装的微粒截留器供静脉注射用药时使用。
1 材料与方法
1.1 实验材料
试验器械:GWJ-5微粒检测仪(天大天发科技有限公司)、一次性静脉注射微粒截留器(专利产品,临床试用,批号 20100228,江苏康进医疗器材有限公司提供)、一次性注射器(批号20081030,上海康德莱企业发展集团有限公司)、一次性头皮针(批号20081105G03,江苏康进医疗器材有限公司)、药用电子震荡器(南通海纳医学科技有限公司)。
试验药品:选用临床常见药物,抽取临床上按规范配制好的、实际用于患者的静脉注射药液(表1)。
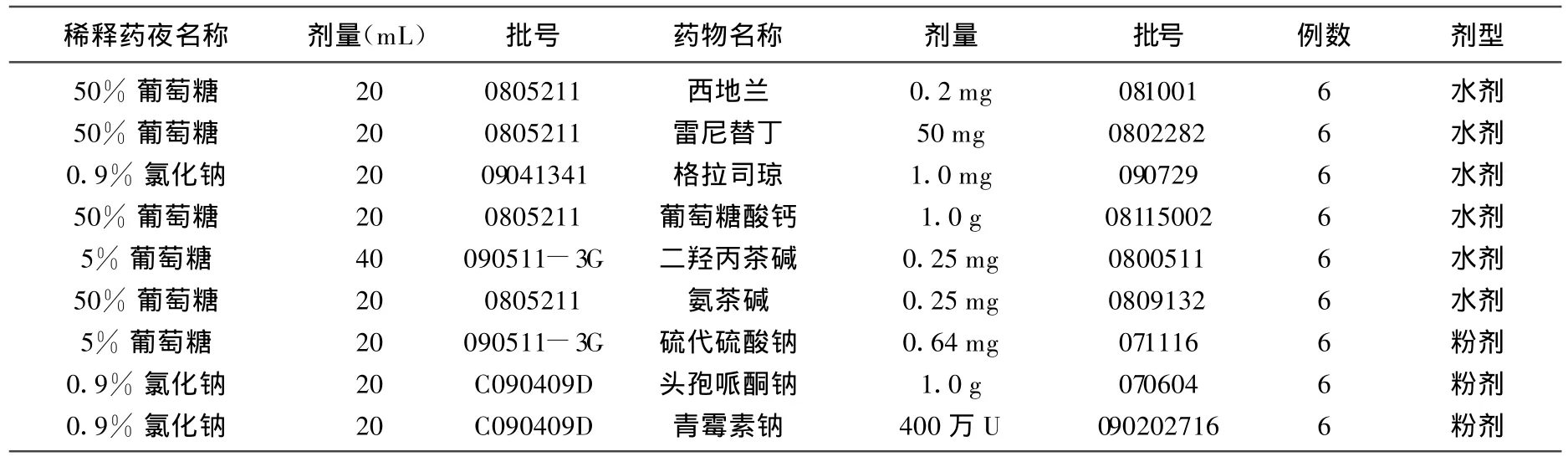
表1 测定微粒含量的静脉推注药物种类及分组
1.2 方法
实验环境 :净化条件下配液 ,室温22~25℃[4],避免人为因素,由同一人操作,严格遵守无菌技术操作原则,遵从药品使用说明书,针剂的吸取严格执行弹-消-锯-消-掰程序,粉剂彻底溶解至澄清时吸取,橡胶塞均穿刺2次。
实验方法:抽取用于静脉推注的药液,包括标本装量25 mL以上与25 mL以下的水针剂和注射用无菌粉末,应用光阻法按照文献[5]方法,使用GWJ-5微粒检测仪进行微粒测定,先测定静脉推注药液在截留前不同微粒的含量及大小,然后将同一标本药液通过一次性微粒截留器截留后再测定其不同微粒含量及大小。取样本54份,截留前后的样本均静置2 min后进行微粒测定,每个样本各检测3次,取其平均值。
2 结 果
静脉推注药物截留前后微粒含量变化见表2。截留后微粒数显著减少,与截留前比较,差异有统计学意义(P<0.01)。
表2 静脉推注药物截留前后微粒数量变化(粒/mL,±s)

表2 静脉推注药物截留前后微粒数量变化(粒/mL,±s)
?
3 讨 论
微粒是指注射液中流动的不溶性物质,微粒进入人体后,由于其不能在体内代谢,较大的微粒或微粒集合体能造成局部血管堵塞或供血不足、组织缺氧、产生静脉炎和水肿、肉芽肿,甚至引起肿瘤,超出患者个体耐受的超量微粒还可引起过敏反应和热原样反应等,也是引起临床输液反应的重要原因[6-7]。《中国药典》2010年版对小容量注射剂的质量作了 ≥10 μ m 及 ≥25 μ m 微粒检验规定[5],即标准装量为100 mL以下的静脉用注射液、静脉注射用无菌粉末、注射用浓溶液及供注射用无菌原料药,每个供试品容器(份)中含10 μ m 及 10 μ m 以上的微粒不得过 6 000 粒,含25 μ m 及25 μ m 以上的微粒不得过600粒。本组试验药品配伍后复配液的质量滤前及滤后均符合药典规定,但复配液截留前后≥10 μ m 及≥25 μ m微粒数目及大小有显著差异,加入水针剂(包括标本装量25mL以上及25mL以下)截留后≥10μ m减少3.9倍;≥25 μ m减少9.8倍。加入粉剂截留后 ≥10 μ m 减少 6.8 倍 ,截留后无 ≥25 μ m 微粒出现。以上结果表明静脉推注药物时使用微粒截留器,可明显减少不溶性微粒数目及大小。
静脉注射液的生产过程、输液器具、操作不当、房间不洁净及加入静脉注射液中的药物是静脉用药微粒污染的来源[8]。本实验的微粒测定值是在排除操作不当、房间不洁净的情况下取得,为无法避免的状况。表2显示,截留前后的微粒数差异具有统计学意义。而目前大多数医疗单位配液室都在普通的治疗室进行,有的甚至与处置室相通,静脉配制药液时缺乏层流工作柜;护理人员的工作衣、帽、鞋、口罩又未消毒,且人员流动大,虽然治疗室每天消毒,但开放使用后很快被污染,造成治疗室不洁净;再加上护理人员缺编,治疗任务大,紧急状态下抢救患者时分秒必争,很难做到操作规范。以上种种情况表明,实际临床上配制的液体在截留前微粒污染的现象比实验组更严重。实验表明,普通条件下配液,微粒、细菌、内毒素污染较重,而净化条件下的配液几乎无污染,可确保临床用药安全[9]。为此,目前状况下临床上进行任何途径静脉给药,都必须使用微粒截留器,以减少不溶性微粒对人体的危害。本组实验使用的一次性静脉注射微粒截留器符合国家质量检测标准和国家药检检测标准,能有效截留10 μ m 以上的微粒,标准接口,连接简单而不繁琐,便于临床操作,任何情况均可使用,包括单独静脉推注,输液过程中,抢救时及麻醉用药时,且价格低廉,实用性强。
[1]居晓伟.输液中不溶性微粒的危害、来源及预防[J].武警医学,2001,12(4):212.
[2]何曙云,刘宇英,温冬梅.静脉注射溶液过滤前后不溶性微粒的观察[J].中华护理杂志,2004,39(3):220.
[3]姚蕴伍,郭常平.现代护理学新编[M].杭州:浙江大学出版社,2005:7.
[4]张琴辉,杨丽丽,涂文婷,等.静脉注射给药中有效过滤器的使用效果探讨[J].温州医学院学报,2005,35(6):484.
[5]国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社,2010:附录71.
[6]王 燕.输液中不溶性微粒和异物及其预防措施[J].黑龙江医药,2009,22(4):542.
[7]刘艳玲.引起临床输液反应的原因及预防措施[J].中国医药导报,2008,5(7):143.
[8]韩红芳.临床输液不溶性微粒危害及其预防[J].护理研究,2003,17(7):812.
[9]李帮兰,袁俊华.引起静脉输液反应常见因素的探讨[J].临床和实验医学杂志,2007,6(4):78.
