HPLC法测定炎立消片中原儿茶酸的含量
2011-04-25,,
,,
(吉林省食品药品检验所,吉林 长春130033)
炎立消片为由单味丁香叶水煎煮和粉末入药制成的片剂。原儿茶酸为其主要成分之一,也是其有效成分,因此原质量标准采用反相高效液相色谱法测定样品中原儿茶酸的含量。在复核过程中发现原操作方法看上去色谱峰为单峰,但是通过多年的经验发现色谱峰实为有效成分与杂质峰的复合峰,使含量测定不能真实的控制有效成分的含量[1-4]。因此,对原标准中原儿茶酸的含量测定方法进行了修订。修改后方法易于操作,结果准确,重现性良好。
1 仪器与试药
岛津LC-2010A高效液相色谱仪,CLASS-VP色谱工作站;原儿茶酸对照品(批号:0844-9802,规格:供含量测定用)由中国药品生物制品检定所提供;乙腈为色谱纯;磷酸为分析纯;水为超纯水。
2 方法与结果
2.1 色谱条件 色谱柱:Alltima HP C18(Φ 4.6×250 mm)(奥泰公司);流动相:乙腈-0.1%磷酸溶液(3∶97);流速:0.8 mL/min;柱温:40 ℃;检测波长:260 nm;理论板数按原儿茶酸峰计算应不低于5 000。
2.2 对照品溶液的制备 取原儿茶酸对照品适量,精密称定,加甲醇制成每1 mL含0.02 mg的溶液,即得
2.3 供试品溶液的制备 取本品20片,精密称定,研细,取约1.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,密塞,称定重量,超声处理30 min,放冷,称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液25 mL,蒸干,残渣加水30 mL使溶解,加稀盐酸约1.5 mL,摇匀,用醋酸乙酯提取5次,每次20 mL,合并醋酸乙酯液,蒸干,残渣用甲醇溶解并转移至10 mL量瓶中,用甲醇稀释至刻度,摇匀,即得。
2.4 方法学考察
2.4.1 阴性对照试验 为进一步考察实验设计的合理性,取不含丁香叶的阴性对照样品,依上述方法测定,结果阴性样品色谱图在原儿茶酸峰相应的保留时间附近无干扰峰检出,从而证明本法是合理可行的。
2.4.2 线性关系考察 精密称取原儿茶酸对照品适量,加甲醇制成每1 mL含0.023 64 mg的溶液。分别精密吸取1、3、5、8、10、12 μL,测定,以对照品进样量为横坐标,以峰面积积分值为纵坐标绘制标准曲线。
求得回归方程:Y=4 812 772.83X-1 024.51(r=1.000 0)
结果表明原儿茶酸进样量在0.023 64~0.283 68 μg范围内,标准曲线线性关系良好,符合外标法定量测定的要求。
2.4.3 精密度试验 精密吸取同一供试品溶液5 μL,注入液相色谱仪,重复6次,测定原儿茶酸色谱峰面积的平均值为486 219,RSD为0.35%,结果表明仪器精密度良好。
2.4.4 稳定性试验 取本品供试品溶液,按上述色谱条件测定,结果见表1。结果表明,在24 h内,供试品溶液中原儿茶酸的含量基本稳定。

表1 稳定性试验结果
2.4.5 重复性试验 取同一供试品6分,依“2.3”项下的方法制成供试品溶液,在上述条件下测定,原儿茶酸含量的平均值为85.0 μg/片,RSD为1.26%。结果表明,方法重复性良好。
2.4.6 加样回收率试验 精密称取同法测定已知含量的供试品(批号070601,含量:274.64 μg/g)6分,分别精密加入对照品甲醇溶液(4.5 μg/mL)50 mL,按“2.3”项下的方法制成所需溶液,并按上述色谱条件测定,计算回收率,结果见表2。

表2 回收率试验结果
2.5 样品测定 取本品,按“2.3”项下的方法制备供试品溶液,分别精密吸取供试品溶液与对照品溶液各5 μL,注入液相色谱仪,按上述色谱条件测定,以外标法计算样品中原儿茶酸的含量,结果见表3。
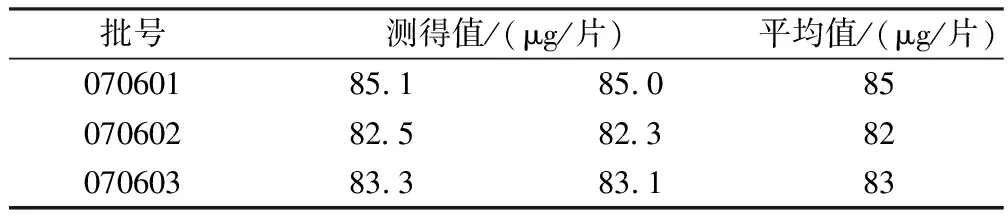
表3 3批样品含量测定结果
2.6 原料药材的测定 上述方法测定3批投料药材,3批丁香叶中原儿茶酸的含量结果见表4。
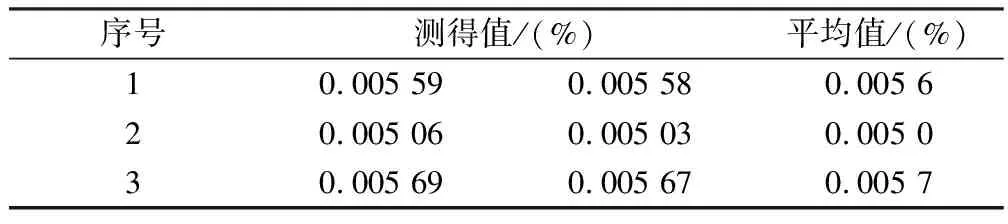
表4 3批药材含量测定结果
如表4所示,3批样品含原儿茶酸的量在0.005 0%~0.005 7%之间,故暂定本品的含量限度为每1片含原儿茶酸不得少于50 μg。
3 讨论
本次实验考察了供试品提取纯化条件的选择:1)将样品用70%甲醇超声,滤过,即得;2)将样品用盐酸溶液超声,乙醚振摇提取;3)“2.2”项下的方法。3种提取方法测得的原儿茶酸含量分别为86 mg/片,74 mg/片,85 mg/片,对方法1)、2)、3)进行比较,结果表明方法2)提取易乳化,杂质较多,含量较低;方法1)、3)得到的供试品含量较高,但是方法1)得到的供试品杂质较多,难于分离,故未采用;方法3)得到的供试品杂质较少,分离效果佳,含量较高,故选此方法。
取原儿茶酸对照品,用甲醇配制成溶液,经UV-2550紫外分光光度计在波长200~350 nm范围内进行光谱扫描,测得原儿茶酸在258.7 nm波长处有最大吸收,因此确定260 nm为本法的测定波长。
本文建立的方法简单准确、灵敏度高、方便可行,为控制炎立消片的质量提供了科学依据。
[1]杜之平.沉香口服液中广枣的原儿茶酸含量测定[J].北方药学,2010(2):13-14.
[2]王勤,孙芸.HPLC法测定锁阳中没食子酸和原儿茶酸的含量[J].西北药学杂志,2010(3):190-192.
[3]刘兴超,杨丽,徐海燕,等.HPLC法同时测定茵山莲颗粒中绿原酸和原儿茶酸的含量[J].沈阳药科大学学报,2008(2):122-125.
[4]邓科君,张艺,王平,等.反相高效液相色谱法同时测定藏药广枣中没食子酸和原儿茶酸的含量[J].色谱,2006(6):652-653.
