沉淀/电解集成处理高盐冶金废水实验研究
2011-04-11袁根勤朱芳芳马扬光
袁根勤,朱芳芳,马扬光
(1.江苏省泰州市环境保护局,江苏 泰州225300;2.江苏省姜堰市环境保护局,江苏姜堰225500;3.江苏省中国医药城,江苏 泰州225300)
1 引言
江苏某新材料有限公司,主要产品为高端锂离子电池,在萃取/反萃生产过程中产生含有萃取剂和铜、镍和铬等重金属的大量硫酸盐废水,根据一类污染物排放要求和标准,经石灰和烧碱沉淀处理后,金属镍和铬在生产车间排放口已达排放标准,但出水中硫酸盐为103.0g/L,对后续生化处理影响较大,无法达标排放。本研究以CaCl2为沉淀剂,在pH值较宽的范围内获得纯度95%~98%的CaSO4。CaSO4是重要的化工、建筑原料,有广阔的市场前景。沉淀尾水通过电解法处理,制取低浓度碱液,回用产品生产中的萃取/反萃取工艺中,实现废水的零排放和资源化利用。
2 材料与方法
2.1 废水水质
试验用水来源于南通市经济开发区某新材料有限公司,为萃取/反萃取制镍生产废水,经石灰和烧碱沉淀处理后,该水质颜色微黄、无味,有少量悬浮物,具体水质最大值见表1。

表1 废水水质
2.2 仪器与药剂
仪器选用HH-S数显恒温水浴锅、DHG-9123A电热恒温鼓风干燥箱、79-2磁力加热搅拌器、电解槽等等。器皿为容量瓶、烧杯、吸附柱、量筒、滴定管等。药剂选用铬酸钾、氯化钡、氧化钙、氯化钙、硝酸银等。
2.3 测定方法
硫酸根浓度与氯离子浓度均采用GB11899-89法测定,氢氧根浓度采用滴定法测定。
2.4 试验设计
根据废水中的硫酸根离子浓度,确定CaCl2的投加量和电解工艺中最佳温度、pH值、极板间距和电解时间,获得最佳硫酸根去除效果和最佳制碱工艺条件。
3 实验结果分析
CaSO4微溶于水,溶解后的硫酸钙一部分以未电离硫酸钙存在,一部分电离成硫酸根离子和钙离子,由于废水中其他盐浓度也较高,CaSO4沉淀的生成必须考虑盐效应和同离子效应的影响,化学式为:

3.1 试验影响因素分析
3.1.1 pH对沉淀效果的影响
取废水50mL分别置于5个锥形瓶中,调节pH值分别6、7、8、10和12。各加入10mLCaCl2溶液,搅拌5min,静置2h,取上清液过滤测定硫酸根浓度,各pH值硫酸根去除率如图1所示。
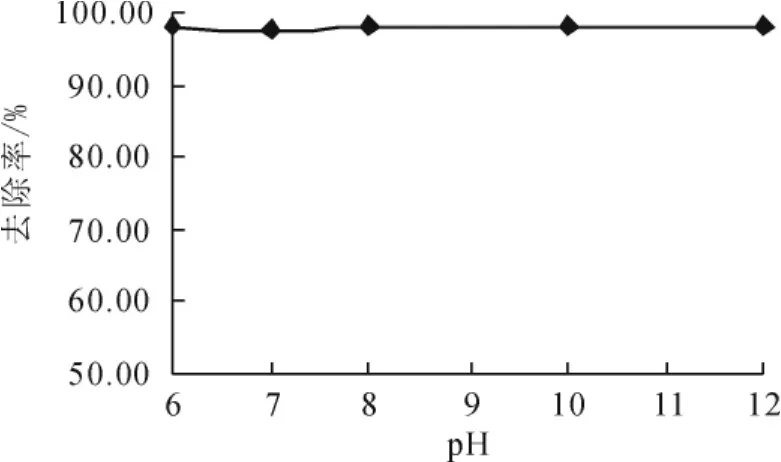
图1 pH对沉淀效果的影响
由图1可知,随pH值的增加,SO2-4去除率均在98%~99%之间,说明pH值在6~12范围内,对CaSO4的沉淀去除效果影响不显著,原水无需调整pH值。
3.1.2 氯化钙投加量
试验在室温25℃进行,称取41.09gCaCl2(CaCl2在25℃的溶解度为70g)溶解于水中,定容至 100mL。取 2mL、3mL、5mL、9mL、10mL 和11mL分别加入50mL废水中,搅拌5min后测定硫酸根去除率,去除效果见图2。
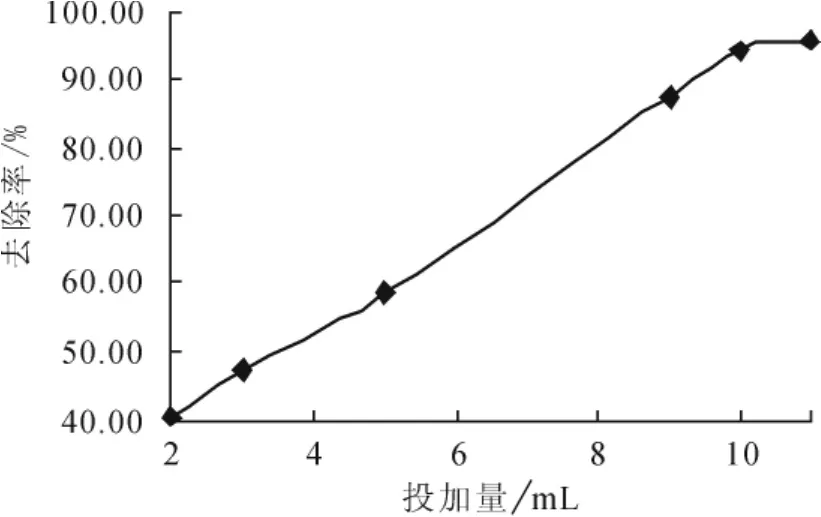
图2 氯化钙溶液投加量对硫酸根去除效果
由图2可知,当CaCl2的投加量为10mL,即4 109mg时,硫酸根的去除率在99.15%,尾水中硫酸根浓度降至880mg/L,CaCl2溶液对硫酸根的去除效果比较好,产生的CaSO4纯度在95%~98%,达到工业级应用标准。
CaSO4微溶于水,溶解度与温度有关,10℃溶解度为1.928g/L,40℃溶解度为2.097g/L,100℃溶解度为1.619g/L,而实验值却为880mg/L,远小于硫酸钙的溶解度,根据本实验测定,硫酸钙的容度积常数在5.1×10-6-1.96×10-4,之所以没有确定值,是由于试验用水非自配纯水,而且原水中含有大量的其它物质,同离子效应和盐效应对本沉淀反应影响比较大,实际上硫酸钙溶解后,一部分以未电离硫酸钙存在,一部分电离成硫酸根离子和钙离子存在,故SO24-离子实际去除率高于理论计算值。
3.2 电解制碱试验
原水经沉淀剂CaCl2处理后,SO24-离子浓度从原来的103 000mg/L降为880mg/L,原水pH 值略有下降,为11.2,Cl-离子浓度为50 672.5mg/L,如果此处理水直接排放,必须回调pH<8,为实现处理水的回用,满足生产需求,Cl-离子浓度必须低于3 500mg/L,通过电解可达到此要求。
3.2.1 电解试验机理
沉淀试验后尾水中氯化钠浓度为50 672.5mg/L,依据电解法制碱工艺机理。
电解:2NaCl+2H2O=2NaOH+Cl2↑+H2↑,
阴极:2H++e=H2↑,
阳极:2Cl-2e=Cl2↑。
3.2.2 电极选择
通过前期实验研究,与电解法制碱工艺比较,Ti/PbO2电极具有电解效率高,电极使用寿命长等优点,一直被广泛应用于电解行业中,所以本试验电极选用Ti/PbO2电极,探索极板间距、pH等对去除Cl-离子的效果影响,确定最佳电解条件。
3.2.3 电极板间距选择
实验选择 Ti/PbO2为阴极,石墨为阳极,以Cl-离子去除率为指标,确定最优板电极间距。如图3知,最佳电极间距为7mm。
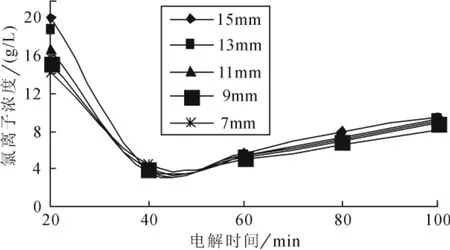
图3 极板间距对电解效率的影响
3.2.4 pH值对电解效果的影响
由图4知,在酸性条件下,电解效率优越于碱性条件,当pH=3,电解时间为40min时,Cl-离子去除率为90.8%,Cl-离子浓度为4 625.3mg/L。

图4 pH对电解效果的影响
3.2.5 最佳条件电解试验
原水经沉淀剂CaCl2处理后,上清液pH=11.2,如果在酸性条件下进行电解去除Cl-离子,势必重调pH值,增加电解负担,故实验确定最佳电解实验条件为:pH=11.2,极板间距为7mm,常温。电解实验结果见图5所示。

图5 电解时间对氯离子浓度的影响
由图5可知,起始时氯离子浓度下降很快,电解时间为60min时,氯离子浓度最低,为3200mg/L,氢氧根浓度为40g/L,完全满足回用要求。
4 结语
(1)用CaCl2作为沉淀剂,处理冶金萃取废水脱除SO24-离子,当原水SO24-离子浓度为103.0g/L,投加CaCl282.18g/L,出水SO24最低880mg/L,去除率在99.15%;回收CaSO4纯度95%~98%,由于同离子效应和盐效应的影响及实际CaSO4溶解特性,SO4-离子实际去除率高于理论计算值。
(2)原水经沉淀剂CaCl2处理后,上清液最佳电解实验条件为:pH=11.2,极板间距为7mm,电解时间60min,常温下,氯离子浓度最低为3 200mg/L,氢氧根浓度为40g/L,完全满足回用要求。
(3)在实验研究中发现,当水中氯离子浓度较高时,电解反应以Cl-为主反应,电解H+为副反应;当水中氯离子浓度低于3.2g/L时,电解H+逐渐成为主反应,电解Cl-则成为副反应;说明电解效率与氯离子浓度有着较大关系。
(4)与传统除盐工艺相比,针对本废水特性和生产工艺,实验探索了电解法处理冶金萃取废水回用、实现CaSO4资源化利用的可行性,有关Cl2的回收将在以后的研究中继续探索。
[1]曹志强.利用脱硫石膏生产纸面石膏板的工艺技术[J].粉煤灰,2009(4):41~42.
[2]张向前,丘自力.沉淀的溶解度及其影响因素[J].商丘职业技术学院学报,2008,38(5):100~103.
[3]陈 魁,向 兰.硫酸钙溶解行为初探[J].盐业与化工,2007,36(2):1~3.
[4]孙宝静.浅谈精盐水预热温度对电解直流电耗的影响 [J].中国氯碱,1999(6):39~40.
