葛渣总黄酮提取及葛根素含量测定
2011-04-06杨树平韩立军朱金卫许瑞波蒋迎道
杨树平,韩立军,朱金卫,许瑞波,蒋迎道
(1.淮海工学院化学工程学院,江苏 连云港 222005;2.淮海工学院理学院,江苏 连云港 222005)
葛渣总黄酮提取及葛根素含量测定
杨树平1,韩立军2,朱金卫1,许瑞波1,蒋迎道1
(1.淮海工学院化学工程学院,江苏 连云港 222005;2.淮海工学院理学院,江苏 连云港 222005)
目的:优化葛渣中总黄酮提取工艺条件,测定葛渣中葛根素含量。方法:以葛渣为原料、总黄酮得率为评价指标,采用L9(34)正交试验设计,考察乙醇体积分数、提取时间、固料比、提取温度对葛渣总黄酮提取效果的影响,同时采用高效液相色谱法(HPLC法)测定葛根素的含量。结果:葛渣中总黄酮的最佳提取工艺条件为以体积分数70%乙醇溶液为溶剂、提取150min、料液比1∶40(g/mL)、提取温度80℃,此条件下的总黄酮得率最高,为32.41mg/g。在该提取条件下,葛根、葛渣和葛粉中总黄酮的含量分别为46.11、32.41mg/g和11.23mg/g;葛根、葛渣和葛粉中葛根素的含量分别为40.63、21.24mg/g和4.71mg/g。结论:葛渣中含有丰富的总黄酮和葛根素,该方法可作为从葛渣中提取总黄酮和葛根素的方法。
葛渣;总黄酮;葛根素;高效液相色谱法;正交试验
葛根(Radiχ puerariae)为豆科植物野葛Pueraria lobata (wmd) Ohwi或甘葛藤P.thomsonii Benth的干燥根,具有解肌、退热、生津、透疹、升阳、止泻之功效,主要用于治疗外感发热、头痛、高血压等疾病[1]。作为常用的传统中药,葛根富含黄酮类化合物和淀粉,也是营养丰富的功能食品原料,已被国家卫生部列入药食同源的天然植物名单[2]。葛根中含有的异黄酮类物质具有降低心肌耗氧量、增加冠状动脉循环、缓解心绞痛、抗心律失调、增强肌体免疫力、生津止渴等多种药理作用。其中葛根素为主要的有效成分,作为治疗心脑血管的主要临床用药[3-7]。葛粉是葛根初级加工产品[8-11]。在鲜葛根制取葛粉的传统工艺中大部分有效成分仍残留在葛渣中,葛渣常常被丢弃不用或作为造纸原料,造成葛根资源的浪费。因此,从“废渣”中获得葛根总黄酮及葛根素,为葛根资源的综合利用提供理论依据。
1 材料与方法
1.1 材料、试剂与仪器
葛渣来自江苏省连云港市云台山区葛根制取葛粉后的残渣(自然晾干,粉碎),葛根采自江苏省连云港市云台山,葛粉购自当地超市。
葛根素对照品 中国药品生物制品检定所;乙醇、石油醚等均为分析纯,甲醇为光谱纯。
DF-1型集热式磁力搅拌器 江苏省金坛市荣华仪器制造有限公司;电热鼓风干燥器浙江舟山市定海区海源仪器厂;BS210S型电子天平 北京赛多利斯天平有限公司;UV-2550型紫外分光光度计、LC-10AVP高效液相色谱仪 日本岛津公司;XA-1固体样品粉碎机 金坛市科兴仪器厂。
1.2 方法
1.2.1 对照品溶液及供试品溶液的制备
对照品溶液的制备:精密称取105℃干燥至质量恒定的葛根素对照品10.1mg于100mL容量瓶中,用体积分数95%乙醇溶解并定容,制备成0.1mg/mL的对照品溶液。
供试品溶液的制备:取葛渣粉末(60目)1g,置于100mL圆底烧瓶中,加入石油醚20mL,加热回流1h进行脱色,过滤弃去滤液,如此重复1次,残渣挥干溶剂后,按照正交试验设计表(表2)中设定的提取条件进行总黄酮的提取,过滤,合并滤液,减压浓缩至原体积的1/4,用95%乙醇定容于100mL容量瓶中,作为供试品溶液待测。
1.2.2 总黄酮的测定
1.2.2.1 检测波长的选择
精密移取对照品溶液和供试品溶液各1.0mL分别置10mL的容量瓶中,加95%乙醇至刻度,摇匀,以95%乙醇作为空白对照,在200~400nm波长范围分别进行紫外吸收扫描,最大吸收均出现在250nm附近(图1),故选250nm为检测波长。
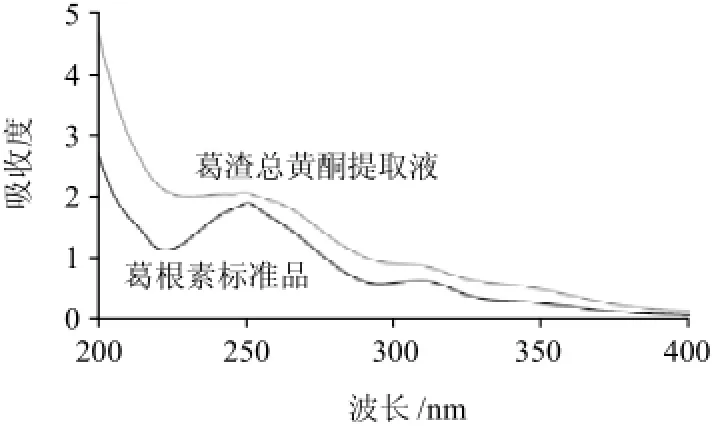
图1 葛根素对照品和葛渣供试品吸收光谱Fig.1 UV absorption spectra of puerarin standard and Radix Puerariae residue extract
1.2.2.2 标准曲线的绘制
精密量取葛根素对照品溶液0.0、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0mL,分别置于10mL容量瓶中,用95%乙醇溶液定容,摇匀静置10min后,以95%乙醇溶液作为空白对照,于波长250nm处测定吸光度,以吸光度Y为纵坐标、葛根素质量浓度X/(mg/mL)为横坐标,绘制标准曲线,得回归方程为Y=84.5180X-0.1334,R2=0.9996。结果显示,葛根素对照品质量浓度在0.01~0.05mg/mL范围内线性关系良好。方法精密度RSD为0.85%,方法重复性RSD为0.34%,稳定性实验RSD为0.99%,样品液在8h内稳定,方法回收率为98.25%,RSD为1.73%。
1.2.2.3 精密度实验
精密吸取同一浓度的葛根素对照品溶液,重复测定5次,吸光度平均值为0.6952,RSD为0.85%,结果表明仪器精密度良好。
1.2.2.4 稳定性实验
精密吸取同一供试品溶液,在0、2、4、6、8h测定,吸光度平均值为1.2442,RSD为0.99%,结果表明本品8h内具有良好的稳定性。
1.2.2.5 重复性实验
精密称取葛渣样品5份,每份1g,按1.2.1节供试品溶液制备方法制成供试品液(6号提取条件)测定吸光度,吸光度平均值为2.6061,RSD为0.34%,结果表明本法具有良好的重复性。
1.2.2.6 准确度实验
精密称取已知总黄酮含量的葛渣样品5份,每份0.1g,每份加入质量浓度为0.101mg/mL的对照品溶液3mL,按1.2.1节操作制成供试品溶液,直接测定吸收度,计算回收率,平均回收率为98.25%,RSD为1.73%,结果表明总黄酮回收率良好,该方法准确度较好,可行性强。
1.2.2.7 样品总黄酮含量的测定
精密移取供试品溶液1mL置于10mL容量瓶中,用95%乙醇溶液定容,以95%的乙醇作空白参比,于波长250nm处测定吸光度,按1.2.2.2节标准曲线的绘制项下的回归方程计算供试品液中总黄酮质量浓度,并计算样品总黄酮得率。

1.2.3 正交试验设计
以葛渣总黄酮得率为评价指标,乙醇体积分数(A)、提取时间(B)、料液比(C)、提取温度(D)为试验因素进行正交设计,因素水平见表1,选用L9(34)正交试验设计表进行正交试验,优化葛渣中总黄酮的提取工艺,正交试验设计及试验结果见表2。
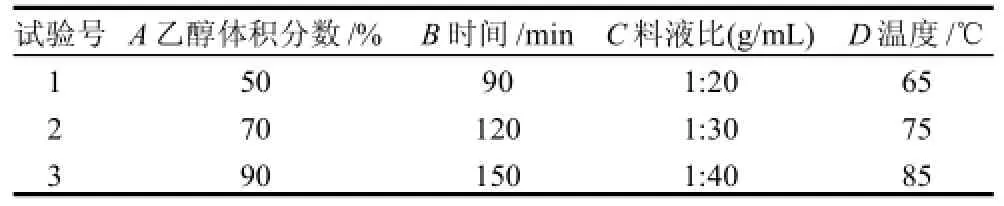
表1 正交试验因素水平表Table 1 Factors and levels in orthogonal array design
1.2.4 高效液相法测定葛根素含量[12-13]
1.2.4.1 色谱条件
色谱柱:C18ODS柱(4.6mm×250mm,5μm);流动相梯度洗脱:其中0~10min为50%甲醇,10~15min为75%甲醇溶液,15~20min为50%甲醇溶液,之后运行5min;检测波长:250nm;流速:1.0mL/min;进样量:20μL;柱温:室温。
1.2.4.2 标准曲线的绘制
精密量取葛根素对照品溶液0.0、1.0、2.0、3.0、4.0、5.0mL分别置于10mL容量瓶中,用甲醇稀释至刻度,摇匀静置10min后,分别进样20μL,于波长250nm处测定吸收峰面积,以吸收峰面积Y为纵坐标、葛根素质量浓度X/(μg/mL)为横坐标,绘制标准曲线,得回归方程为Y=1702.9X+4668.2,R2=0.9997。结果显示,葛根素质量浓度在10.1~50.5μg/mL范围内线性关系良好。
1.2.4.3 精密度实验
精密吸取同一浓度对照品溶液20μL,在上述色谱条件下测定,重复进样5次,峰面积RSD为1.12%,结果表明仪器精密度良好。
1.2.4.4 稳定性实验
精密吸取同一供试品溶液20μL,按上述色谱条件,分别于0、2、4、6、8h进样测定,峰面积RSD为1.23%,结果表明供试品溶液在8h内稳定性良好。
1.2.4.5 重现性实验
精密称取葛渣样品5份,按1.2.1节供试品溶液制备方法制成供试品溶液,在上述色谱条件下测定,峰面积RSD为0.69%,结果表明方法重现性良好。
1.2.4.6 回收率实验
精密称取已知葛根素含量的葛渣样品5份,每份0.1g,每份加入质量浓度为0.101mg/mL的对照品溶液3mL,按1.2.1节供试品溶液制备方法制成供试品溶液,精密吸取20μL进样,在上述色谱条件下测定峰面积,计算回收率,平均回收率为98.44%,RSD为1.64%,表明葛根素回收率良好,该方法准确度较好,可行性强。
1.2.4.7 样品葛根素含量的测定
精密移取供试品溶液1mL置于10mL容量瓶中,用甲醇稀释并定容,在上述色谱条件下,进样20μL,测定峰面积,按1.2.4.2节标准曲线的绘制项下回归方程计算供试品液中葛根素质量浓度,并计算样品中葛根素含量。

1.2.5 葛根、葛渣、葛粉样品中总黄酮和葛根素含量比较
在最佳提取工艺条件下,即乙醇体积分数70%、提取时间150min、料液比1∶40(g/mL),提取温度80℃,将葛根、葛渣、葛粉按1.2.1节供试品溶液制备方法分别制成供试品溶液,按1.2.2.7节样品总黄酮含量测定方法测定并计算总黄酮含量,按1.2.4.7节样品葛根素含量测定方法测定并计算葛根素含量。
2 结果与分析
2.1 总黄酮提取工艺正交试验
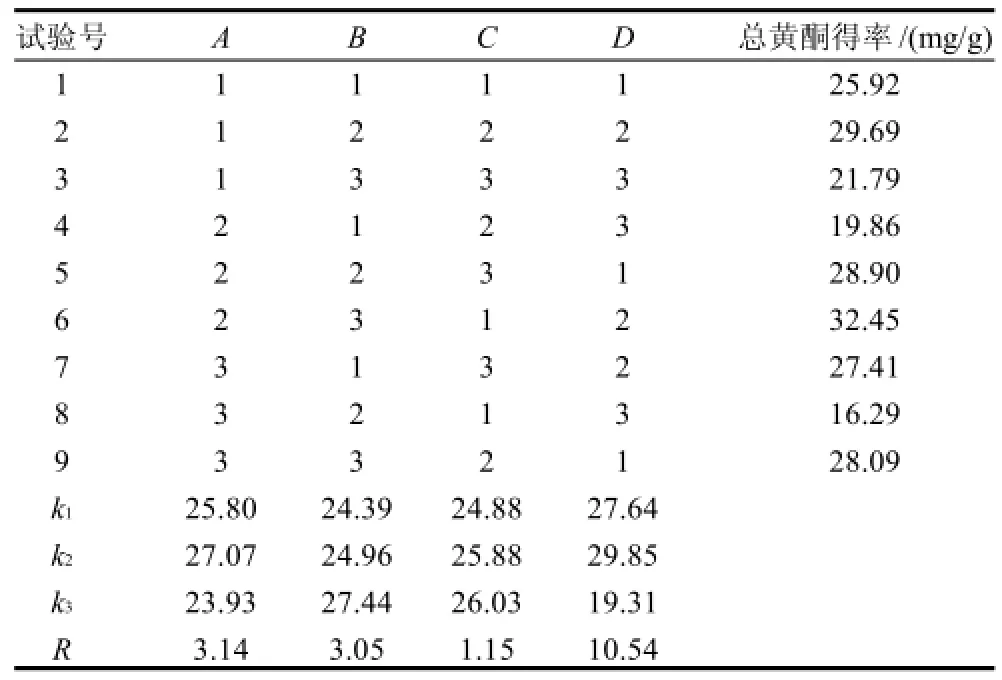
表2 总黄酮提取L9(34)正交试验设计及结果Table 2 Orthogonal array design and corresponding experimental results
表2表明,各因素对提取效果的影响程度为提取温度>乙醇体积分数>提取时间>液固比,其中提取温度对葛渣总黄酮的提取效果影响最大,而料液比对提取效果无显著影响。葛渣总黄酮的最佳提取工艺为A2B3C3D2,即70%乙醇溶液、提取150min、料液比1∶40、提取温度80℃。
在最佳优化工艺条件进行3次平行验证实验,葛渣总黄酮分别为32.32、32.52、32.40mg/g,RSD为0.31%,总黄酮的平均含量为32.41mg/g,重现性较好,可见该工艺稳定可行。
2.2 葛根、葛渣、葛粉中总黄酮及葛根素含量比较

表3 葛根、葛渣和葛粉总黄酮及葛根素含量对比Table 3 Contents of total flavonoids and puerarin in Radix Puerariae, Radix Puerariae residue and pueraria root powder
黄酮是葛根的主要活性成分,其含量是衡量葛根质量的重要指标,传统方法制备的葛粉中总黄酮含量较少,一部分总黄酮在葛粉加工过程中流失。通过含量比较实验,由表3可知,连云港市云台山地区葛根中总黄酮的含量较高为46.11mg/g,葛渣中总黄酮含量达32.41mg/g,而葛粉中总黄酮含量仅为11.23mg/g,即在制取葛粉过程中,葛根中黄酮成分的70.29%残留在葛渣中,仅有24.36%黄酮成分留在葛粉中,有近5.35%的黄酮成分在葛粉的制备过程中流失。
葛根素为葛根总黄酮中主要成分,是葛根总黄酮产品的一个重要指标,通过比较,由表3可知,连云港云台山地区葛根中葛根素的含量较高,为40.63mg/g,而葛渣中葛根素含量为21.24mg/g,葛粉中葛根素含量近4.71mg/g。也就是说,在制取葛粉中过程中,葛根中葛根素成分的52.29%残留在葛渣中,仅有11.60%葛根素成分存在于葛粉中,还有近36.11%的葛根素成分在葛粉的制备过程中流失掉落。
如果葛渣被直接丢弃而不被利用,葛根中约75.6%黄酮成分或者约52.29%葛根素成分被白白扔掉而未被利用,造成葛根资源的极大浪费。同时,葛粉中功能性成分含量较少,葛粉传统制备方法值得商榷,以避免资源的过度浪费。
3 结 论
葛渣总黄酮最佳提取工艺为乙醇体积分数70%、提取时间150min、料液比1∶40(g/mL)、提取温度80℃。葛渣总黄酮得率为32.41mg/g。
连云港云台山地区葛根、葛渣、葛粉中总黄酮的含量分别为46.11、32.41mg/g和11.23mg/g,葛根素的含量分别为40.63、21.24mg/g和4.71mg/g,即在制取葛粉中,葛根中大约70.29%的黄酮成分或52.295%葛根素留在葛渣中,可从生产葛粉的“废渣”中获得葛根黄酮及葛根素。
[1]国家药典委员会. 中华人民共和国药典∶ 一部[M]. 8版. 北京∶ 化学工业出版社, 2005∶ 233-234.
[2]徐怀德. 药食同源新食品加工[M]. 北京∶ 中国农业出版社, 2002∶ 126-130.
[3]苗慧, 肖文彬, 秦伯益. 异黄酮化合物的药理作用[J]. 国外医学∶ 药学分册, 1989, 16(6)∶ 355-358.
[4]陶忠华. 新药葛根素的研究[J]. 中国新药杂志, 1993, 2(6)∶ 1-3.
[5]孙泽铃, 李以菊, 闰玉芹. 葛根素的临床应用[J]. 实用医技杂志, 2006, 13(16)∶ 2830-2832.
[6]廖洪波, 贺稚非, 王光慈, 等. 葛根的研究进展及展望[J]. 食品工业科技, 2003, 24(2)∶ 81-83.
[7]郑皓. 葛根的研究与开发现状[J]. 氨基酸和生物资源, 2006, 28(2)∶24-26.
[8]孙林超. 效液相色谱法测定葛粉保健品中葛根素的含量[J]. 理化检验∶ 化学分册, 2008, 44(10)∶ 945-949.
[9]张尊听. 野葛根中葛根素的提取及HPTLC测定[J].中国医药工业杂志, 2001, 32(7)∶ 291-293.
[10]张雁, 张孝棋. 葛根的营养保健功能及开发利用[J]. 食品研究与开发, 2000, 21(2)∶ 37-39.
[11]李悦, 李艳菊. 国内外葛根功能食品研究进展[J]. 食品研究与开发, 2007, 28(12)∶ 174 -177.
[12]张梦军, 吴世容, 李志良. 几种提取葛根异黄酮的方法比较及实验优化[J]. 中成药, 2005, 27(10)∶ 1133-1135.
[13]彭菊艳, 王俊儒, 张义英, 等. 葛根有效成分的含量测定与提取工艺优化[J]. 陕西农业科学, 2005(3)∶ 52-54.
Optimization of Total Flavonoids Extraction from Radiχ Puerariae and HPLC Determination of Puerarin
YANG Shu-ping1,HAN Li-jun2,ZHU Jin-wei1,XU Rui-bo1,JIANG Ying-dao1
(1. School of Chemical Engineering, Huaihai Institute of Technology, Lianyungang 222005, China;2. School of Mathematics and Science, Huaihai Institute of Technology, Lianyungang 222005, China)
In this paper, orthogonal array design L9(34) was employed to optimize the extraction conditions of total flavonoids from Radiχ Puerariae residue left after pueraria root powder extraction. The effects of extraction temperature, ethanol concentration, extraction time and material-to-liquid ratio on extraction rate of total flavonoids were probed. Meanwhile, a HPLC method to determine puerarin content in Radix Puerariae was presented based on optimized extraction process. The optimal extraction conditions were determined as follows∶ ethanol concentration 70%, reflux time 150 min, reflux temperature 80 ℃, and material-to-liquid ratio 1∶40, under which, the contents of total flavonoids in Radiχ Puerariae, Radiχ Puerariae residue and pueraria root powder were 46.11, 32.41 mg/g and 11.23 mg/g, and of puerarin 40.63, 21.24 mg/g and 4.71 mg/g, respectively. From these results, we drew the conclusion that Radix Puerariae residue is rich in total flavonoids and puerarin and that the optimized extraction process can be used for the extraction of total flavonoids and puerarin from Radiχ Puerariae residue.
Radiχ Puerariae residue;total flavonoids;puerarin;high performance liquid chromatography;orthogonal array design
R284.2
A
1002-6630(2011)14-0303-04
2010-10-03
江苏省海洋资源开发研究院科技开放基金课题(JSIMR09D02);淮海工学院自然科学基金项目(KX10019);淮海工学院引进人才启动基金项目(KK01064)
杨树平(1960—),女,副教授,学士,主要从事药物化学研究。E-mail:spyang69320@yahoo.cn
