柠檬酸化壳聚糖的合成及其水溶性研究
2011-03-14孙晓君刘晓慧冯玉杰
孙晓君,刘晓慧,秦 智,冯玉杰
(1.哈尔滨理工大学化学与环境工程学院,150040哈尔滨,sunxjhit@yahoo.com.cn; 2.哈尔滨工业大学城市水资源与水环境国家重点实验室,150090哈尔滨)
壳聚糖(β-(1,4)-2-氨基-2-脱氧-D-葡聚糖)是甲壳素脱乙酰化反应生成的产物,它是一种含有氨基多糖的高分子化合物,无毒且具有独特的生物兼容性、显著的蛋白质亲和性及易与金属离子螯合等优点,在药物控制释放、细胞培养及微反应器、人体器官和基因运载工具以及分离介质等多个领域展现出广阔的应用前景[1-3].但因分子内和分子间氢键的作用,壳聚糖水溶性很差,限制了其进一步应用[4-5].对壳聚糖进行化学改性,引入功能性基团,进而增加其溶解性和功能性,是壳聚糖化学研究的热点领域之一.Li等[6]采用微波辐照法制备了可溶于水的低分子量壳聚糖.Avadi等[7]为了增加壳聚糖的溶解性能,通过改进两步法制备出了具有抗菌作用的N-二乙基-甲基壳聚糖.Park等[8]制备了壳聚糖与Carbopol的高分子聚合物IPC.该聚合物有望成为药物释放的基础材料,并且有良好pH依赖性.本文首次提出了将柠檬酸引入壳聚糖并成功制备出柠檬酸化壳聚糖.柠檬酸是一种含羟基的多元有机酸,将其引入壳聚糖中,会大大提高壳聚糖产物的溶解性能,对拓展壳聚糖的应用领域具有重要意义.
1 实验
1.1 试剂和仪器
壳聚糖(浙江玉环县化工厂,脱乙酰度99.56%,摩尔质量为 160.09 g/mol);柠檬酸(AR);无水乙醇(AR);PHS-3C型酸度计;乌式黏度计(D=0.5~0.6 cm);80-2型离心机;红外光谱仪(Nicolet Avator370型);GZX-9070MBE型电热恒温鼓风干燥箱.
1.2 柠檬酸化壳聚糖的反应原理
壳聚糖和柠檬酸进行羧基化反应,主要发生在氨基上,反应式如下:

1.3 柠檬酸化壳聚糖的制备
称取一定量的壳聚糖,按一定摩尔配比加入柠檬酸,在乙醇介质中,于一定温度下搅拌进行反应,反应结束后将产物离心提纯,再用蒸馏水溶解、无水乙醇洗涤3次,于55℃恒温干燥至恒重.
1.4 取代度测定
准确称取0.200 g已干燥的反应产物于锥形瓶中,用移液管量取25 mL 0.1 mol/L NaOH标准溶液,摇匀.以酚酞为指示剂,用0.1 mol/L HCl标准溶液滴定过量的NaOH,至微红色消失30 s内不再现,即为终点.柠檬酸化壳聚糖产物的取代度[9]
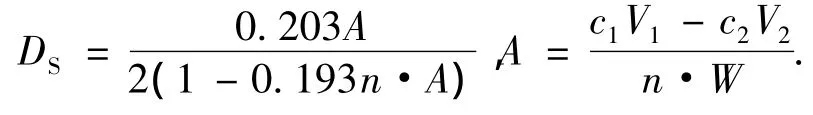
式中:0.203为与1 mol NaOH反应后的每个乙酰氨基葡萄糖残基的毫克数;0.193为与1 mol NaOH反应的毫克数;A为取代基的质量分数(%);n为取代因子;c1为NaOH标准溶液的摩尔浓度(mol/L);V1为消耗NaOH标准溶液的体积(mL);c2为HCl标准溶液的摩尔浓度(mol/ L);V2为消耗HCl标准溶液的体积(mL);W为试样的质量(g).
1.5 溶解性的测定
用移液管取100 mL蒸馏水注入锥形瓶中,准确称取定量的柠檬酸化壳聚糖,逐渐加入锥形瓶中,加热至完全溶解,记下产品的溶解温度[10].
1.6 粘均分子量的测定
称量已干燥的柠檬酸化壳聚糖样品溶于0.1 mol/L氯化钠水溶液中,用乌氏黏度计在(30±0.5)℃下测得其特性粘数[η],平行测定3次,用方程[η]=6.58×10-3M0.88计算得到粘均分子量[11].
1.7 柠檬酸化壳聚糖的红外表征
将壳聚糖和最佳工艺条件下制备的柠檬酸化壳聚糖研细,KBr压片,在4 000~400 cm-1进行红外波谱扫描.
2 结果与讨论
2.1 最佳工艺参数的确定
选取柠檬酸和壳聚糖的投料摩尔比、反应时间、反应温度为主要影响因素,分别考察各种因素对产物取代度的影响,实验结果如图1~3所示.
图1是在20℃下反应16 h,柠檬酸和壳聚糖投料摩尔比对产品取代度的影响.可以看出,随着柠檬酸和壳聚糖投料摩尔比的增加,柠檬酸化壳聚糖的取代度逐步增大.这是因为壳聚糖分子中的活性中心一定,而随着柠檬酸用量增加,此活性中心与柠檬酸碰撞发生反应的几率增加,这说明适量增加柠檬酸的量有利于壳聚糖进行羧基化反应.实验中发现当柠檬酸和壳聚糖投料摩尔比小于0.5时,反应不彻底,产品不能全部溶解于水;当柠檬酸和壳聚糖投料摩尔比大于0.5以后,随着柠檬酸用量的增大,取代度最初增加较快而后增加趋势变缓并逐渐趋于平衡.
图2是在柠檬酸和壳聚糖投料摩尔比为1.5∶1、反应温度为20℃条件下反应时间对取代度的影响.可以看出,在反应的前4 h,产物的取代度提高较快,之后产物的取代度有所下降.这是因为开始时反应进行得不完全,故取代度较低;随着反应时间的延长,取代度逐渐增加;但当产物的取代度达到一定值后,取代基之间会产生位阻效应,阻碍柠檬酸的进一步取代;同时,随着取代度的增加,取代基自身的水解等副反应也会发生,故在反应4 h后,取代度又有所下降.
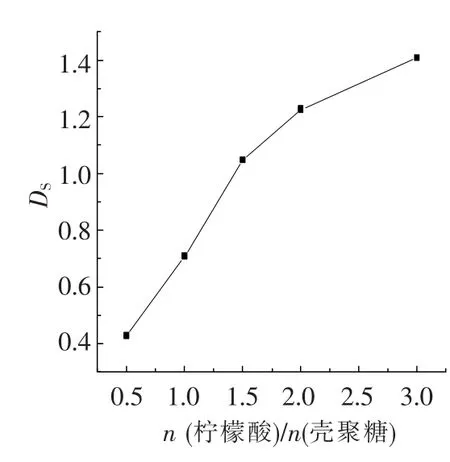
图1 柠檬酸和壳聚糖投料摩尔比对取代度的影响
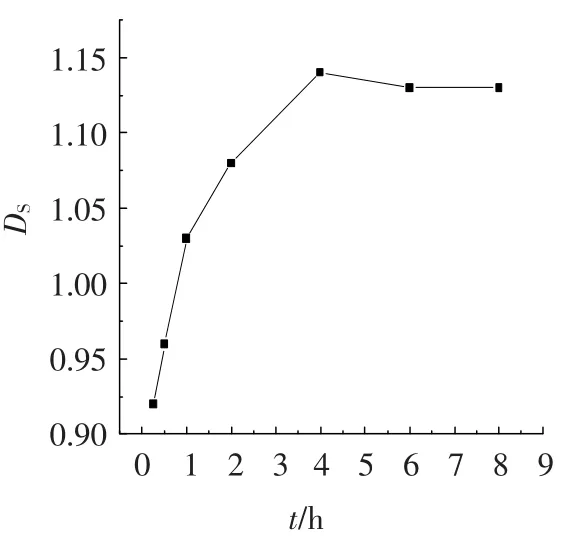
图2 反应时间对取代度的影响
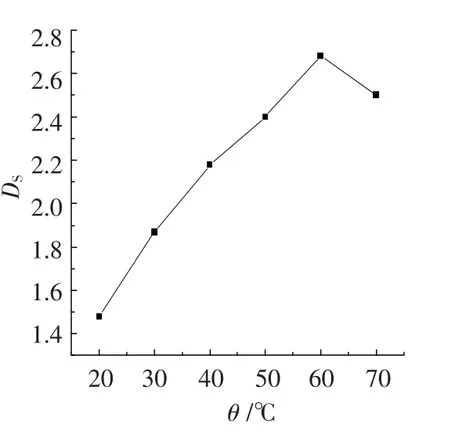
图3 反应温度对取代度的影响
图3是反应温度对产品取代度的影响.可以看出,随着反应温度的升高,柠檬酸化壳聚糖的取代度逐步增大,但当温度高于60℃时,取代度开始下降.这是因为柠檬酸基取代反应为亲电取代反应,温度的升高促进正碳离子的进攻,使活性中心发生反应的几率提高,故使取代度随温度升高而增加;但温度过高会加剧壳聚糖在弱碱性介质中的降解作用,增加副反应和物料的黏附,使产物的取代度下降.综合以上因素并结合后续改性壳聚糖水溶性实验(表1)确定制备柠檬酸化壳聚糖的最佳工艺参数为:反应温度为20℃,柠檬酸和壳聚糖摩尔比为2∶1,反应时间为0.5 h.
2.2 产品性能测定
2.2.1 取代度和粘均分子量的测定
按照最佳工艺参数:θ=20℃,柠檬酸和壳聚糖投料摩尔比为2.0,t=0.5 h,制备柠檬酸化壳聚糖.按照1.4的方法测其取代度,平行测3次取平均值,测得柠檬酸化壳聚糖取代基的质量分数A=3.78,代入计算,)取代度DS=1.45.按照1.6的方法测产品的粘均分子量,平行测3次取平均值,测得柠檬酸化壳聚糖的特性粘数[η]=451.7 mL/g,代入[η]= 6.58×10-3M0.88计算,产品的粘均分子量为28.5万.
2.2.2 溶解性的测定
准确称取壳聚糖和不同取代度的柠檬酸化壳聚糖各0.030 g,分别溶于10 mL蒸馏水中,加热并随时记录溶液的温度,记下柠檬酸化壳聚糖完全溶解时的温度,考察不同的取代度对柠檬酸化壳聚糖溶解性的影响,并平行做壳聚糖的溶解性对照实验,结果见表1.
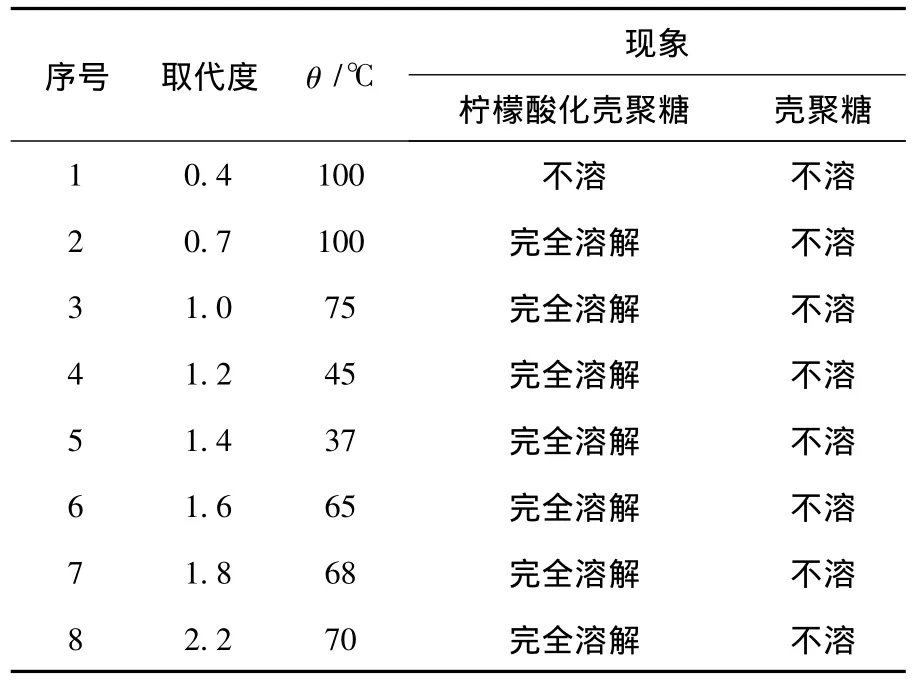
表1 柠檬酸化壳聚糖和壳聚糖溶解性对照
从表1可以看出,柠檬酸化壳聚糖打破了壳聚糖不溶于水的限制,柠檬酸化壳聚糖完全溶解时所需的温度随取代度变化.这是由于当取代度较低时,取代度的增加会使壳聚糖产物分子中的亲水基团—COOH增多,进而会使柠檬酸化壳聚糖的溶解性能也随之增大.但当取代度大于1.4时,随着柠檬酸化壳聚糖取代度的逐步增大,接到壳聚糖上的亲水基团—COOH会发生聚合,形成二聚体,使其溶解性能又开始下降,进而导致其溶解于水的温度又逐渐升高.本实验结果表明,取代度在1.4左右的柠檬酸化壳聚糖是溶解性较好的壳聚糖改性产品.
2.2.3 红外表征
图4为柠檬酸化壳聚糖与壳聚糖的FTIR谱图,可以看出,柠檬酸化壳聚糖在3 400 cm-1处出现的强吸收是产物形成氢键后的—OH和—NH的伸缩振动吸收峰;在3 200~2 500 cm-1区出现的宽而散的吸收峰是形成氢键后羧基中O—H的伸缩振动峰,1 723 cm-1的较强吸收峰为羧基中伸缩振动吸收峰,这两组峰表明柠檬酸已接枝到壳聚糖上;1 577 cm-1附近较强、较宽的吸收峰是酰胺Ⅰ峰、II峰,1 394 cm-1处为酰胺III吸收峰,这3组峰的出现说明是N上取代,即壳聚糖中氨基与柠檬酸的羧基反应生成了酰胺.
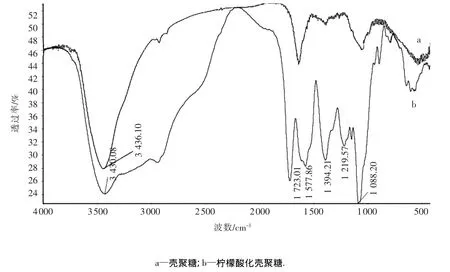
图4 柠檬酸化壳聚糖与壳聚糖的红外谱图
3 结论
1)以壳聚糖和柠檬酸为原料首次在温和的条件下合成了水溶性较好的改性壳聚糖产物.
2)红外光谱测试结果证明所合成的产物为柠檬酸化壳聚糖.
3)制备柠檬酸化壳聚糖的适宜工艺参数为:柠檬酸/壳聚糖投料摩尔比为2∶1,反应温度为20℃,反应时间为0.5 h.
4)在壳聚糖分子上引入柠檬酸,其水溶性得到很大程度的改善,有助于扩大壳聚糖产品的应用范围.
[1]WANG C,SUN S L,XIAO H N,et al.Release model of water-soluble chitosan nanoparticles for protein delivery[J].Agricultural Science and Technology,2009,10(3):144-147.
[2]HUANG G L,YANG C,ZHANG K,et al.Adsorptive removal of copper ions from aqueous solution using cross-linked magnetic chitosan beads[J].Separation Science and Engineering,2009,17(6):960-966.
[3]ZHANG M,REN H X.Structural modification and application of chitosan[J].Journal of Clinical Rehabilitative Tissue Engineering Research,2007,11(48):9817-9820.
[4]蒋挺大.壳聚糖[M].2版.北京:化学工业出版社,2007.
[5]车小琼,孙庆申,赵凯.甲壳素和壳聚糖作为天然生物高分子材料的研究进展[J].高分子通报,2008 (2):45-49.
[6]LI P C,XING R,LIU S,et al.Low molecular weight chitosan oligosaccharides and it separation method[J].Poultry Science Association,2007(86):1107-1114.
[7]AVADI R M,MAHDAVINIA G,SADEGHI A M,et al. Synthesis and characterization of N-diethyl methyl chitosan[J].Iranian Polymer Journal,2004,13(5):431-436.
[8]PARK S H,CHUN M K,CHOI H K.Preparation of an extended-release matrix tablet using chitosan/carbopol interpolymer complex[J].International Journal of Pharmaceutics,2008(1):39-44.
[9]吴友吉,宋庆平,李庆海.高取代度羧甲基壳聚糖的制备[J].合成化学,2006,14(5):506-509.
[10]SHAW M T.Studies of polymer-polymer solubility using a two-dimensional solubility parameter approach[J].Journal of Applied Polymer Science,2003,18 (2):449-472.
[11]陈鲁生,周武,姜云生.壳聚糖粘均分子量的测定[J].化学通报,1996(4):57-58.
