荷移-同步荧光光谱法直接测定血清中阿米卡星的含量
2011-03-06
(江苏省南通卫生高等职业技术学校,江苏 南通 226007)
阿米卡星是一种抗菌谱广的半合成氨基苷类抗生素,临床上用于革兰阴性杆菌主要为耐庆大霉素菌株所致较重的感染,属浓度依赖性杀菌剂,临床疗效与血药浓度有一定关系,但药物浓度过高会产生一定的耳、肾毒副作用,且对神经肌肉接头有阻滞作用[1]。为了科学合理、安全有效地使用该药,应建立准确、快速的方法监测血液中药物浓度。目前阿米卡星的含量测定方法为微生物法[2],但该法繁冗费时、费用高,不适于快速检测;镍毛细管电泳法[3]、电化学方法[4]、分光光度法[5]、旋光法[6]、荧光法[7]、共振瑞利散射法[8]等也曾用于阿米卡星的测定,其中应用最多的是分光光度法,该法所用仪器价廉、操作简易,但灵敏度欠佳;高效液相色谱法准确,但所需仪器昂贵,样品预处理复杂。为此,笔者建立了荷移-同步荧光光谱法直接测定血清中阿米卡星的含量,现报道如下。
1 仪器与试药
RF-5301 PC型荧光光度计(日本岛津公司);电子天平(德国Sartorius公司);HH-S型数显恒温水浴锅(江苏省金坛市医疗仪器厂);80-2型离心沉淀器(江苏省金坛市医疗仪器厂)。阿米卡星标准品(中国药品生物制品检定所);2,3-二氯-5,6-二氰基-1,4-苯醌(DDQ,美国Sigma公司);血清(镇江中心血站);甲醇、乙腈(国药集团化学试剂有限公司)为分析纯,水为双蒸水。
2 方法与结果
2.1 溶液制备
准确称取0.058 5 g阿米卡星标准品,用双蒸水溶解后转移至100 mL容量瓶中,定容制成1.00×10-3mol/L的阿米卡星标准品溶液,置4℃冰箱中保存,使用时用水逐级稀释至所需浓度。准确称取0.045 4 g DDQ,用甲醇溶解后转移至100 mL容量瓶中,定容制成2×10-3mol/L的DDQ标准液,置4℃冰箱中保存,使用时用甲醇逐级稀释至所需浓度。吸取适量阿米卡星溶液,置10 mL容量瓶中,加1 mL DDQ甲醇溶液,用甲醇定容至刻度,摇匀,置30℃水浴中恒温30 min,取出冷却至室温,以364 nm为激发波长,在452 nm波长处测定荷移反应产物的荧光强度,同时做空白试验。
2.2 测定条件选择
2.2.1 激发波长与发射波长
按2.1项下方法配制溶液,分别对所得荷移反应产物、阿米卡星和空白试剂进行荧光激发和发射扫描,结果见图1。在水溶液中阿米卡星能发射微弱荧光,其最大激发波长和最大发射波长分别为323 nm和366 nm。与DDQ发生荷移反应后,荷移反应产物的荧光激发峰和发射峰分别红移至361 nm和452 nm波长处,与阿米卡星相比,其激发光谱和发射光谱分别红移38 nm和86 nm,且荧光强度显著增强(激发光谱和发射光谱通带为5 nm)。
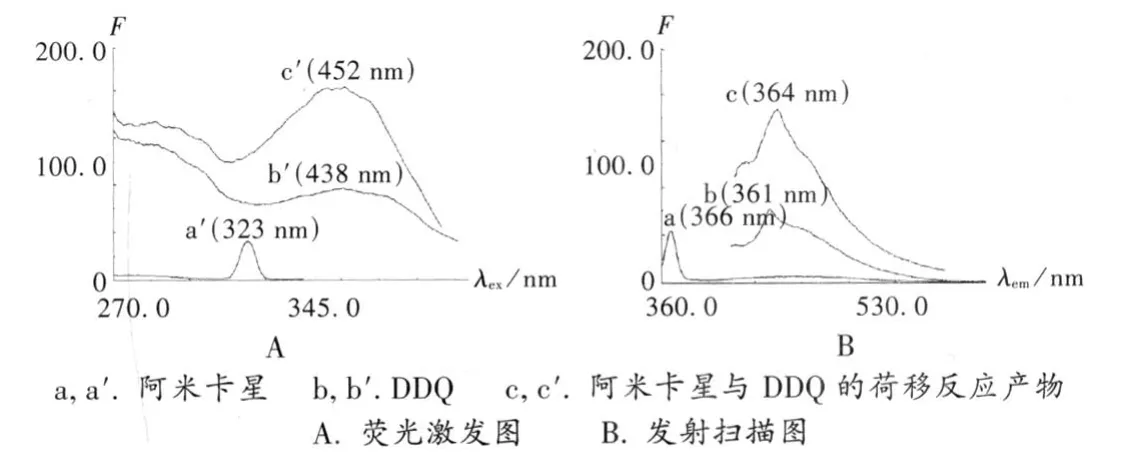
图1 荧光激发和发射扫描图谱
2.2.2 反应温度
分别依法测定20~60℃水浴中阿米卡星与DDQ电荷转移反应的荧光强度。结果从20℃起,荧光强度随温度的升高逐渐增强,30℃后受温度的影响不大,故选择30℃为反应温度。
2.2.3 反应时间
在选定的温度下,考察5~60 min内不同时间段的荧光光谱。结果表明,阿米卡星与DDQ在30 min后即可反应完全,故选择反应时间为30 min。荷移反应产物在室温下放置24 h荧光值无明显变化,说明荷移反应产物具有较好的稳定性。
2.2.4 溶剂
在选定的反应温度和反应时间下,分别用甲醇、乙醇、丙酮、正丁醇、异丙醇、四氢呋喃进行试验,发现阿米卡星与DDQ的荷移反应在甲醇中进行的灵敏度高,在乙醇中的荧光强度较在甲醇中低,在丙酮、正丁醇、异丙醇、四氢呋喃中无荷移反应产物生成,因此选择反应在甲醇中进行。
2.2.5 受体及用量
为选择合适的电子受体,分别用茜素、甲酚红、四氯苯醌、DDQ与阿米卡星进行试验,结果DDQ能与阿米卡星生成络合物。DDQ用量为0.7~1.2 mL时,荧光强度最大且稳定,浓度过低则反应完全,而浓度高可导致荧光强度下降。故选择2×10-5mol/L的DDQ 1.0 mL。
2.3 干扰试验
在最佳试验条件下,考察了体内常见金属离子对阿米卡星测定的干扰情况。结果在相对误差不大于±5%时,250倍量的K+,200倍量的 Ca2+,100倍量的 Na+,5倍量的 Al3+,2倍量的 Mg2+,0.5 倍量的 Fe3+,20 倍量的 Zn2+,0.05 倍量的 Cu2+等不干扰测定。
2.4 阿米卡星回收率测定
2.4.1 血清处理
取血清30 mL,加乙腈30 mL,混合,在3 000 r/min转速下离心处理10 min,待蛋白质沉淀后取上清液,置冰箱中保存。
2.4.2 测定方法
准确移取1 mL血清,加适量阿米卡星标准品溶液,置100 mL容量瓶中,用双蒸水稀释至刻度,备用。准确取1 mL备用溶液,置10 mL容量瓶中,加1 mL DDQ甲醇溶液(2×10-5mol/L),用甲醇定容至刻度,摇匀,于30℃水浴中恒温30 min,取出冷却至室温,在 Δλ=30 nm,狭缝宽度为5 nm时测荧光强度,同时做试剂空白试验。
分别对阿米卡星与DDQ的荷移反应产物和空白血清做荧光光谱扫描(图2),由图2可见,测定血清中阿米卡星时,由于血清中内源性荧光物质的背景干扰,常规荧光分析方法难以测定。而同步荧光光谱法能很好地解决这个问题,在同步荧光光谱测定中,Δλ是最重要的参数,直接影响方法的灵敏度和选择性。分别在 Δλ为20,30,40,50,60,70,80 nm 时,对含有阿米卡星的血清做同步荧光光谱扫描。结果表明,Δλ=30 nm时,阿米卡星荷移反应产物与血清中的内源性荧光物质分辨率最好,灵敏度最高(图3)。
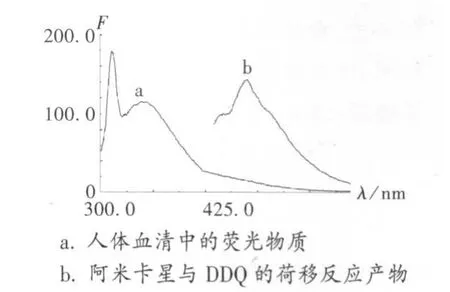
图2 荧光发射波长图谱
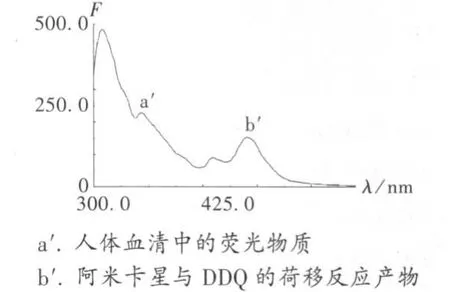
图3 同步荧光发射光谱
按测定方法操作,设定 Δλ=30 nm,对不同浓度的荷移反应体系分别在310~600 nm波长范围内进行同步荧光光谱扫描。结果表明,阿米卡星浓度在 0.3×10-6~1.5 ×10-6mol/L(即 175.65 ~878.25 μg/L)范围内与荧光强度线性关系良好,回归方程 F=19.692 C+132.459 3(C 为 10-6mol/L),r=0.998 3,检出限为33.387 μg/L。
取 1 mL 空白血清和 4 ×10-5mol/L(相当于 23.42 μg/mL)的阿米卡星标准品1mL,置100mL容量瓶中,用双蒸水定容,摇匀。取1mL试样溶液,置10 mL比色管中,依法做回收率试验,结果见表1。

表1 血清中阿米卡星回收率测定结果(n=3)
3 讨论
采用同步荧光技术很好地避免了血清中基体荧光与药物荧光光谱重叠而引起的干扰,血清不须预处理即可直接测定其中阿米卡星的含量,回收率测定结果令人满意,方法操作简单,灵敏度高,检出限低,体系稳定性好,损失小,对生物样品中药物含量的测定具有一定的理论意义和应用价值。
[1]周 芸.曲利本蓝、依文思蓝与氨基糖苷类抗生素的共振瑞利散射光谱研究及分析应用[D].济南:山东大学,2007.
[2]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2005:752.
[3]Fang XM,Ye JN,Fang YZ.Determination of polyhydroxy antibiotics by capillary zone electrophoresis with amperometric detection at a nickel electrode[J].Anal Chim Acta,1996,329(1-2):49-55.
[4]Yeh HH,Lin SJ,Ko JY,et al.Rapid and selective micellar electrokinetic chromatography for simultaneous determination of amikacin,kanamycin A,and tobramycin with UV detection and application in drug formulations[J].Electrophoresis,2005,26(4-5):947-953.
[5]张力增,陈 琪.分光光度法测定硫酸阿米卡星注射液的含量[J].海峡药学,2003,15(5):52-53.
[7]张 萍.荧光光谱法测定阿米卡星含量[J].化学工程师,2007(1):30-31.
[8]张远馥,王金中,郝巧艳.共振瑞利散射法测定阿米卡星[J].南阳师范学院学报,2008,7(3):49-52.
