吲哚美辛巴布剂小鼠离体皮肤透皮吸收实验研究
2011-02-28蔡丽娟杨金荣张庆伟
李 璐 蔡丽娟 杨金荣 张庆伟
吲哚美辛为非甾体抗感染药,能够抑制前列腺素合成,发挥较强的解热、镇痛及抗感染作用,但口服易带来明显的胃肠道刺激。有报道研究了一些新剂型如:肠溶微囊、缓释微囊及羟丙基-β-环糊精包合物滴眼液等来减轻这种不良反应[1-3]。本研究中,笔者研制了其外用型巴布剂,以期达到药剂量可控、载药量较大、透气性好及使用方便安全的特点[4],丰富临床应用剂型,并探讨自制的吲哚美辛巴布剂的体外透皮吸收情况。
1 材料与方法
1.1 材料 (1)试验用动物:普通级昆明种小鼠18只,雄性,50 d龄,平均体质量为(22±2)g,天津医科大学试验动物中心提供。(2)仪器与药品:日本岛津LC—6A高效液相色谱系统(LC-6A型恒流泵、SPD-6A紫外检测器、Anastar色谱工作站)、KromacilC18色谱柱(250 mm×4.6 mm,5 μm,天津市色谱科学技术公司)、GM-0.33隔膜真空泵(天津津腾)、BP211D型电子分析天平(Sartorius)、RYJ-6A型药物透皮扩散试验仪(上海黄海药检仪器厂);含氮酮的吲哚美辛巴布剂(自制,吲哚美辛含量1%,氮酮含量2%),无氮酮的吲哚美辛巴布剂(自制,吲哚美辛含量1%),吲哚美辛对照品(天津市药检所提供);市售吲哚美辛乳膏(规格为1%,锦州九泰药业有限公司);甲醇(色谱纯,天津市康科德科技有限公司);乙酸(分析纯,天津市化学试剂一厂),重蒸水(自制)、pH7.4磷酸盐缓冲液(自配)。
1.2 方法
1.2.1 建立吲哚美辛高效液相色谱(HPLC)测定方法 (1)色谱条件:色谱柱为KromacilC18,5 μm,250 mm×4.6 mm;流动相为甲醇∶水∶乙酸(75∶25∶0.1);流速为1.0 mL/min;柱温为室温;检测波长265 nm。(2)线性关系:精密称取吲哚美辛对照品16 mg,置100 mL容量瓶中,用流动相定容后,精密吸取0.2、0.4、0.6、0.8、1.0、1.2及1.5 mL,分别置于10 mL容量瓶中,用流动相定容,进样量为20 μL,265 nm波长处测定峰面积,以峰面积对吲哚美辛浓度(C)作线性回归。(3)连续进样精密度测定:取0.016 g/L的吲哚美辛对照品溶液20 μL连续6次进样,测定峰面积。(4)日间精密度测定:取0.016 g/L的吲哚美辛对照品溶液20 μL,在6 d内每天进样1次,测定峰面积。
1.2.2 鼠皮制备 小鼠驯养3 d后断颈处死,立刻用剃刀剃去腹毛,剪取完整腹部皮肤,去除皮下脂肪组织和结缔组织,露出真皮层,蒸馏水洗净,置于磷酸盐缓冲液中浸泡30 min后,取出用pH7.4的磷酸盐缓冲液漂洗至洗液澄明,用滤纸吸干,备用。
1.2.3 透皮吸收试验测定 改良Franz扩散装置,见图1。扩散池中暴露皮肤面积为2.8 cm2,接收室容积为6.5 mL。取处理好的鼠皮裁剪成合适大小,置于扩散池中,角质层向上。分别取自制巴布剂和市售乳膏剂适量(相当于吲哚美辛4 mg)均匀帖敷或涂布于皮肤表面,向接收室中加入pH7.4的磷酸盐缓冲液6.5 mL,置于(37±1)℃恒温水浴中,转速100 r/ min。分别于0.5、1、1.5、2、3、4、6及8 h精密吸取5 mL溶液,并向接收室中注入等量磷酸盐缓冲液,0.8 μm微孔滤膜过滤,精密吸取滤液2 mL定容于10 mL容量瓶中,取20 μm注入液相色谱仪并在265 nm波长下测定峰面积。计算不同时间单位面积时的累积渗透量Q(μg·cm-2)。

图1 改良Franz扩散装置示意图
累积渗透量Q按下式计算[5]:式中V为接收室容积,Vi为每次取样体积,Ci为第i次取样时接收液中的药物浓度,A为扩散池中暴露皮肤面积。以时间(h)为横坐标,累积渗透量Q(μg·cm-2)为纵坐标,对曲线进行直线回归,计算渗透速率(μg·cm-2·h-1),即单位时间内单位面积药物的渗透量。
1.2.4 分组及测定方法 以无氮酮吲哚美辛巴布剂和市售吲哚美辛乳膏剂作为对照组,以含2%氮酮吲哚美辛巴布剂为试验组,每组6例,采用改良Franz扩散池和小鼠离体皮肤进行体外渗透试验,利用HPLC法以接收液中吲哚美辛浓度为测定指标,计算制剂中吲哚美辛累积渗透量和渗透速率。
1.3 统计学方法 采用SPSS 12.0软件包进行统计学处理,计量资料以±s表示。组间均值比较采用方差分析,进一步两两比较用SNK-q检验法,P<0.05为差异有统计学意义。
2 结果
在本研究色谱条件下吲哚美辛的保留时间为12.5 min。主峰与改良Franz扩散装置接收液中杂质峰分离度良好。
2.1 线性关系 吲哚美辛浓度在3.2~24 mg/L范围内峰面积与浓度呈良好的线性关系,HPLC测定方法的回归方程为Y=7 709.2 X+1 048.5(X为吲哚美辛浓度,Y为峰面积),r=0.999 8(P<0.001)。连续进样精密度及日间精密度试验相对标准偏差(RSD)分别为0.60%和1.02%。
2.2 各组制剂中吲哚美辛的渗透速率比较 3种制剂中吲哚美辛累积渗透量与时间皆呈线性关系,体现出零级动力学特征;含2%氮酮的吲哚美辛巴布剂的渗透速率显著高于不加氮酮吲哚美辛巴布剂组及市售吲哚美辛乳膏剂组,差异有统计学意义(均P<0.01);不含氮酮的吲哚美辛巴布剂的渗透速率与市售吲哚美辛乳膏剂组的差异无统计学意义(P>0.05),见表1。
3 讨论
吲哚美辛为传统的解热镇痛抗感染药物,近年来又发现了其可预防抗生素性耳中毒、治疗慢性荨麻疹、防治节育器所致的子宫出血、治疗小儿神经性尿频、Banti综合征[6]、改善牙龈微循环[7]及抗肿瘤[8]等临床新用途。
药物透皮进入皮下组织后能迅速进入毛细血管入血循环,在皮肤两侧形成较大浓度梯度。本实验中吸取接收液5 mL并注入等量磷酸盐缓冲液,可提高浓度梯度,形成漏槽条件,有利于药物的透皮扩散。有研究显示吲哚美辛乳膏剂的透皮释药过程呈现零级动力学特征[9],此与本试验结果相符。本研究结果显示2种巴布剂和乳膏剂中吲哚美辛的累积渗透量Q与渗透时间t呈线性关系,表明3种制剂中吲哚美辛均以零级动力学恒速经皮渗透,吸收平稳,可以避免药物浓度的峰谷波动性,提高用药安全性。自制含氮酮巴布剂的吲哚美辛渗透速率明显高于不含氮酮的巴布剂,考虑与氮酮促进吲哚美辛渗透过皮肤有关。透皮吸收促进剂种类较多,主要有亚砜类、醇类、脂肪酸类、吡咯酮类、表面活性剂、萜类及精油等。氮酮是一种常用的非极性促透剂,能促进大多数疏水性和亲水性化合物的透皮吸收。其促透作用的机理是通过溶解角质细胞间和细胞内脂质,从而增加角质层的通透性,减小药物扩散阻力,同时增加角质层含水量,促进药物经水性通道渗透[10]。另外含氮酮巴布剂的吲哚美辛渗透速率也明显高于乳膏剂。
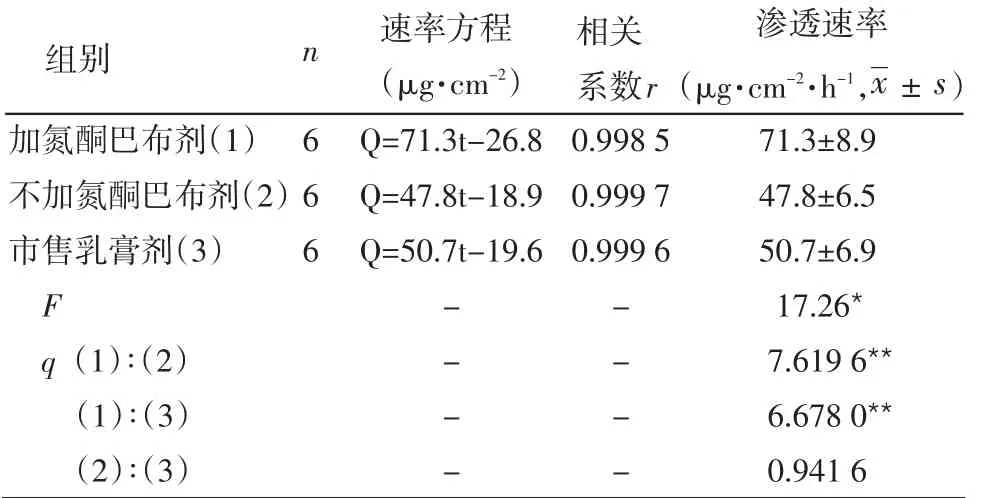
表1 3种制剂中吲哚美辛的渗透速率比较
因此,自制含氮酮巴布剂有利于药效的发挥,是具有开发价值的新型经皮控释制剂。
[1]谢茵,邢桂琴,张金.吲哚美辛肠溶微囊的制备及药物释放的研究[J].山西医科大学学报,2006,37(4):386-388.
[2]宋明侠,相晓东.复凝聚法制备吲哚美辛缓释微囊的研究[J].天津药学,2007,19(5):29-31.
[3]蔡永豪,张晓碧,刘小飞.吲哚美辛羟丙基-β-环糊精包合物滴眼液的制备[J].中国药业,2009,18(9):38-39.
[4]王艳艳,徐希明,余江南.中外巴布剂研究现状分析[J].中国药事,2009,23(6):603-606.
[5]唐人杰,尹东锋,丁雪鹰,等.星型硅微针阵列对化学药物的经皮促透作用[J].中国药学杂志,2008,43(12):914-917.
[6]田进军,李艳娜.吲哚美辛的临床新用途[J].中外医疗,2009,28(6):165.
[7]陈铁楼,刘景昌,刘国勤,等.吲哚美辛对人牙龈微循环的作用研究[J].口腔医学,2009,29(1):7-10.
[8] 董薇,肇丽梅,张彩霞,等.荷瘤与正常小鼠血浆及瘤体中吲哚美辛药动学研究[J].中国药学杂志,2008,43(1):48-50.
[9]邢桂琴,苗采烈,赵丽琴.透皮吸收促进剂对吲哚美辛乳膏透皮释放的影响[J].中国医院药学杂志,2000,20(11):662-664.
[10]侯雪梅,李国栋,李卫华.化学促渗剂及其机理的探讨[J].上海医药,2008,29(5):231-234.
