钼酸铵中钼含量不同分析方法的对比
2010-12-31侯新伟张志强张二召段松强彭光辉
侯新伟,张志强,张二召,段松强,彭光辉
(洛阳高科钼钨材料有限公司,河南 洛阳 471003)
0 引言
长期以来,钼酸铵中钼含量的分析没有相应的国家标准或行业标准做指导。业内主要使用乙酸铅重量法[1-2]和直接焙烧重量法两种方法。但两种方法之间结果的差异常常导致供需双方计算吨品位时的矛盾。因此,选择准确、方便、快捷的分析方法,具有重要的现实意义。
1 方法原理
1.1 乙酸铅重量法
试料经氨水溶解。溶液在乙酸-乙酸铵缓冲溶液中,用乙酸铅沉淀溶液中的钼酸根,钼酸铅沉淀经过滤,灼烧,称重。
1.2 直接焙烧重量法
试料经焙烧,称重,减去杂质含量,再乘以一定系数即为钼含量。
2 实验部分
2.1 主要仪器及试剂
主要仪器:箱式电阻炉(北京科伟永兴仪器有限公司),电子天平(德国梅特勒托列多分析仪器有限公司)。
试剂:盐酸(1.19g/mL);氨水(0.90g/mL);盐酸(1+1);乙酸-乙酸铵缓冲溶液(称取250g乙酸铵,溶于500mL水中,加入150mL乙酸,过滤后以水稀释至1 000mL);乙酸铵洗涤液(移取25mL乙酸-乙酸铵缓冲溶液,以水稀释至500mL);乙酸铅溶液(18g/L,称取18g乙酸铅,加入15mL冰乙酸和80mL水溶解,过滤后稀释至1 000mL);滤纸浆(将定量滤纸撕成碎片,放入500mL烧杯中,加水煮成糊状);甲基橙指示剂(1g/L);单宁溶液(10g/L,作外指示剂用)。
2.2 实验方法
2.2.1 乙酸铅重量法
称取0.200 0g试料,精确至0.000 1g。将试料置于400mL烧杯中,加入8mL氨水,盖上表面皿,低温加热溶解。溶液用水稀释至体积约300mL,加入两滴甲基橙指示剂,用盐酸(1+1)中和至橙红色,再过量10~12滴。加入50mL乙酸-乙酸铵缓冲溶液,加热至微沸,取下,在搅拌下用滴定管逐滴加入乙酸铅溶液至与单宁外指示剂不呈黄色反应后,再过量2~3mL。加入少许纸浆,加热微沸后,在温处静置30min。取下用中速定量滤纸过滤,黏附在烧杯壁和玻璃棒上的沉淀用一小片滤纸檫净,用热乙酸铵洗涤液洗涤沉淀10~12次。将沉淀和滤纸移入已知质量的瓷坩埚中,烘干,灰化,置于550~600℃高温炉中灼烧至恒重。在干燥器中冷却至恒温,称量。按下式计算钼的质量分数:

式中:m0为试料的质量,g;m1为灼烧后钼酸铅质量,g;0.261 3为钼酸铅换算成钼的系数。
独立地进行两次测定,所得结果应表示至2位小数。取其平均值。实验室之间分析结果的差值应不大于表1所列允许差。

表1 乙酸铅重量法测定结果允许差 %
2.2.2 直接焙烧重量法
取30mL瓷坩埚在箱式电阻炉(550~600℃)中焙烧至恒重,在干燥器中冷却至恒温,称取空坩埚质量。称取2g左右试料,将盛放试料的坩埚置于550~600℃箱式电阻炉中灼烧至恒重。在干燥器中冷却至恒温,称量焙烧后的试料加坩埚质量。按下式计算钼的质量分数:

式中:m0为试料质量,g;m1为焙烧后试料的质量,g;m2为焙烧后杂质的总质量,g;0.666 5为三氧化钼换算成钼的系数。
独立地进行两次测定,取其平均值。
3 结果与讨论
取两批钼酸铵,分别按照乙酸铅重量法和直接焙烧重量法进行分析,所得结果见表2、表3、表4。
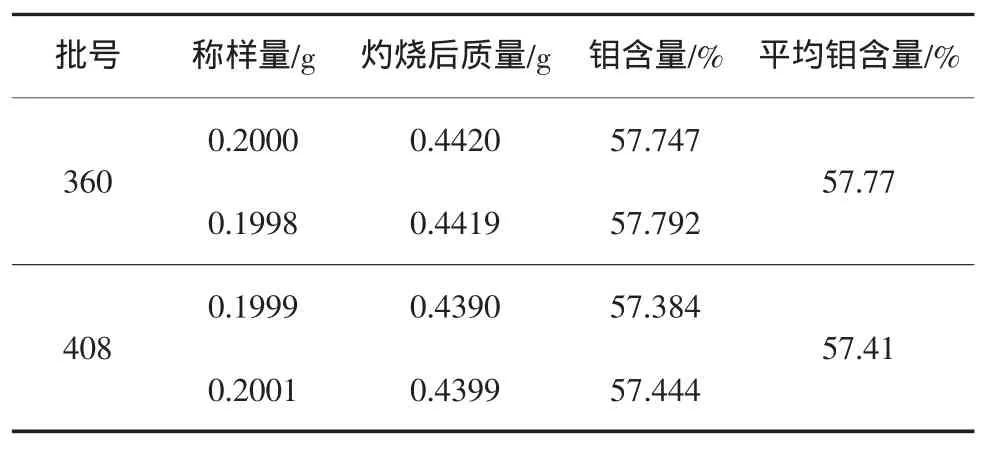
表2 乙酸铅重量法
由表4可知,钼酸铵中杂质含量很低,对最终分析结果基本没有影响,可以忽略不计。但当杂质总含量超过0.3%时,必须扣除杂质含量。当杂质含量超过1%时,直接焙烧重量法就不合适了,这时就要考虑使用乙酸铅重量法。
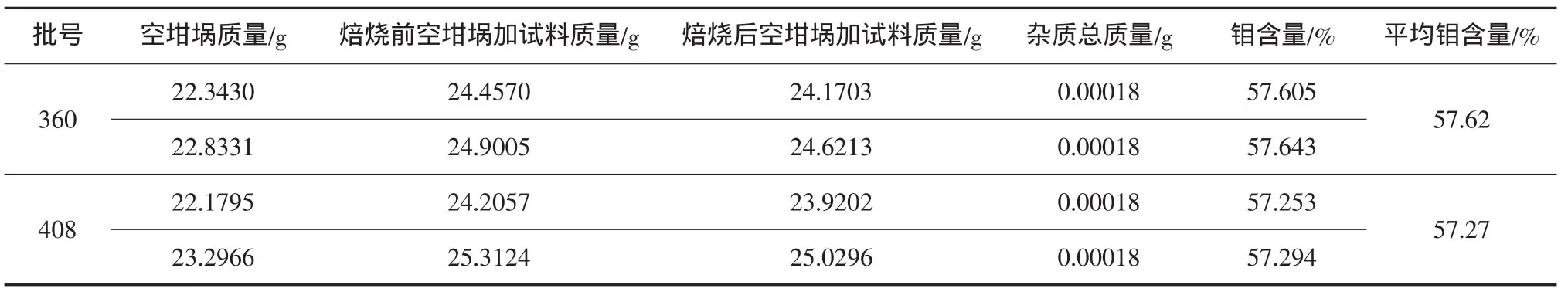
表3 直接焙烧重量法

表4 杂质含量(以三氧化钼为基体) %
4 结语
通过乙酸铅重量法和直接焙烧重量法测定钼酸铵中钼含量的对比可以看出,乙酸铅重量法称样量小,步骤烦琐,允许误差大,且中间添加试剂易引入杂质,导致分析结果偏高。而直接焙烧重量法称样量大,步骤简单方便,重复性和可操作性都很强。
[1]马永香.GB/T 15079.1-94钼精矿化学分析方法—钼量的测定[S].北京:中国国家标准化委员会.1994.
[2]北京矿冶研究总院分析室.矿石及有色金属分析手册[M].北京:冶金工业出版社,1990.
