气氛及添加剂对燃料热氧化作用的影响*
2010-12-12李丹
李 丹
(潍坊学院,山东 潍坊 261061)
气氛及添加剂对燃料热氧化作用的影响*
李 丹
(潍坊学院,山东 潍坊 261061)
采用碘量比色法跟踪测定了燃料a和b分别在饱和溶解氧和隔绝氧加热条件下氢过氧化物浓度随时间的变化,研究气氛环境对燃料热氧化过程中生成氢过氧化物的量的影响,结果表明,在不同温度下,溶解氧的量对燃料自氧化反应影响很大,饱和溶解氧时,燃料中氢过氧化物可以累积的量远远大于限氧条件下的。评价了主抗氧剂BHT与辅抗氧剂168(亚磷酸酯类)在燃料a中复配后的抗氧能力。
燃料;热氧化;氢过氧化物;抗氧剂
热氧化安定性是燃料的重要性质之一[1-2],研究燃料热氧化安定性的主要方法是考察燃料热氧化后所产生沉积物的量、颜色变化以及氢过氧化物量的变化等。燃料热氧化过程涉及一系列复杂的化学反应,生成氢过氧化物等中间产物,以及醇、酮、醛、酸等多种氧化产物。在相对较高的温度下,氢过氧化物分解产生的自由基可以加速碳氢燃料自氧化反应,成为沉积物前驱体,极少量的氢过氧化物分解可能极大地影响碳氢燃料的氧化速率[3-4],氢过氧化物是影响燃料系统不稳定的主要因素之一。
对于燃料的氧化过程,除温度,过氧化物外,这个过程受外界许多其它因素的影响,如溶解氧、接触材料和抗氧剂等。环境气氛显著影响燃料的氧化过程。从燃料自氧化机理中可以了解到,燃料中的溶解氧是燃料氧化变质的主要外来反应物,无论是烃自由基R·还是烃过氧化物自由基RO2·的生成都与之有着密切的关系[5-6]。研究环境气氛对燃料氢过氧化物生成的影响,对研究燃料的氧化安定性具有重要意义。
本文以采用碘量比色法定量分析燃料热氧化过程中氢过氧化物的浓度、燃料氧化诱导期的变化,用紫外-可见光谱分析氧化燃料颜色的变化,考察环境气氛对燃料自氧化反应的影响差异。此外,从抗氧剂的应用角度出发,将抗氧剂BHT与辅抗氧剂168(亚磷酸酯类)复配,研究其对燃料热氧化的抑制作用,考察并评价其复配效果。为深入了解碳氢燃料的热氧化安定性提供实验基础,研究结果对燃料的储存和应用具有重要意义。
1 实验部分
1.1 仪器与试剂
自制静态恒温热氧化装置;RD-100型压力溶弹(耐压4.6M Pa,北京石油化工研究院);DHG-9039A型电热恒温箱(上海精宏实验设备有限公司);UV 2550型紫外可见分光光度计(日本SH IMADZU公司)。
选用两种不同类型的航空煤油,编号a和b,其中燃料a为一种混合碳氢燃料,主要组成为链烃51.4 %、环烷烃47.4%、芳烃1.2%,密度(20℃)0.7933 g/cm3,燃料b是一种高密度环烷烃燃料,即挂式四氢双环戊二烯二聚体,密度(25℃)0.939 g/cm3。其他试剂:磷酸氢二钾 (AR,湖州湖试化学试剂有限公司),磷酸 (AR,浙江新安化工集团股份有限公司),碘酸钾 (AR,玉环生化试剂厂),碘化钾 (AR,广东汕头市西陇化工厂),冰醋酸 (AR,杭州化学试剂有限公司),三氯甲烷 (AR,国药集团化学试剂有限公司),可溶性淀粉 (AR,菱湖食品化工厂)。
1.2 实验步骤
采用静态法评价燃料的热氧化安定性,通过分别在通入氧气的敞开体系和隔绝空气的封闭体系两种条件下进行加速热氧化实验,考察气氛对燃料a和燃料b热氧化安定性的影响。
实验温度为120℃和160℃。通氧条件下是在加热燃料样品的同时以30 m L/min的流速向燃料样品中通入氧气,封闭条件下氧化实验则是将一定量燃料样品装入RD-100型压力溶弹内,于恒温箱中在设定温度下进行不同时间的热氧化。
通过碘量比色法[7]测定航煤氧化过程中氢过氧化物含量的变化。在酸性条件下,试样中的氢过氧化物与碘离子作用,生成游离碘,碘遇淀粉显蓝色,碘-淀粉显色物在过量碘离子存在下的磷酸-磷酸氢二钾缓冲体系中稳定,通过比色法可以得知含碘量,并换算出试样中氢过氧化物的质量摩尔浓度。
以未氧化的新鲜燃料作参比,用紫外扫描仪进行波长扫描,跟踪氧化燃料颜色变化。
2 结果与讨论
2.1 气氛对燃料热氧化作用的影响
通过观察燃料a和燃料b在通氧及隔绝氧条件下氢过氧化物含量的变化情况,了解溶解氧对燃料热氧化的影响。

图1 不同气氛中燃料a中氢过氧化物的含量(a 120℃;b 160℃)

图2 不同气氛中燃料b中氢过氧化物的含量(a 120℃;b 160℃)
从图1和图2可以看到,在a、b两种燃料中溶解氧的量对其自氧化反应影响是非常大的。如图1(a),在120℃温度条件下,燃料a在通氧条件下反应进行14 h燃料中氢过氧化物含量达到极大值0.18 mmol ·g-1,隔绝氧条件下反应进行6 h氢过氧化物含量达极大值0.032 mmol·g-1。160℃温度条件下,燃料a在封闭条件下,反应进行到2 h时,其氢过氧化物含量达到极大值,0.029 mmol·g-1,而在持续通氧条件下,反应到1 h时,氢过氧化物含量就达到了极大值,0.062 mmol·g-1。可见,160℃时在持续通氧条件下燃料氧化速度较快,且所生成的氢过氧化物的含量也大于隔绝氧条件下的反应(如图1(b)所示)。虽然通氧条件下燃料中生成氢过氧化物的含量大于封闭条件下的,但达到最大值所需的时间是封闭条件下的大于持续通氧条件下的。由于120℃时,燃料的氧化速度相对较慢,其所需的氧化诱导期相对较长,在封闭体系中,除燃料自身的溶解氧外,只有溶弹中剩余体积封存的空气中的氧气。所以在有限氧提供条件下,经6 h其中氢过氧化物含量即达到最大值,而在溶解氧充足的条件下,燃料在氧化过程中,氢过氧化物随着时间的延长不断累积至最大值,需要的时间相对较长。燃料b在160℃和120℃不同气氛下氧化时其中氢过氧化物含量的变化如图2所示。160℃温度条件下,燃料b在不同气氛下的氧化规律与燃料a的较相似,而燃料 b在120℃封闭条件下反应时相对较稳定,氧化速度较慢,20 h内其氢过氧化物含量增加幅度很小,持续通氧条件下氢过氧化物含量随时间延长持续增大。溶解氧浓度的增加,会使烃类自由基R·和烃过氧化物自由基RO2·的数量增加。而这两种活性基团正是燃料氧化反应的引发剂,它们的增加,使燃料自由基链氧化反应的循环周期加快,加速燃料氧化,致使燃料的氧化安定性降低[5-6]。
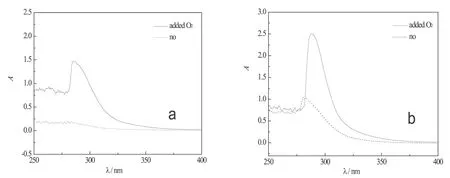
图3 不同气氛下氧化燃料a的吸收光谱(:a,120℃-4h;b,160℃-2h)
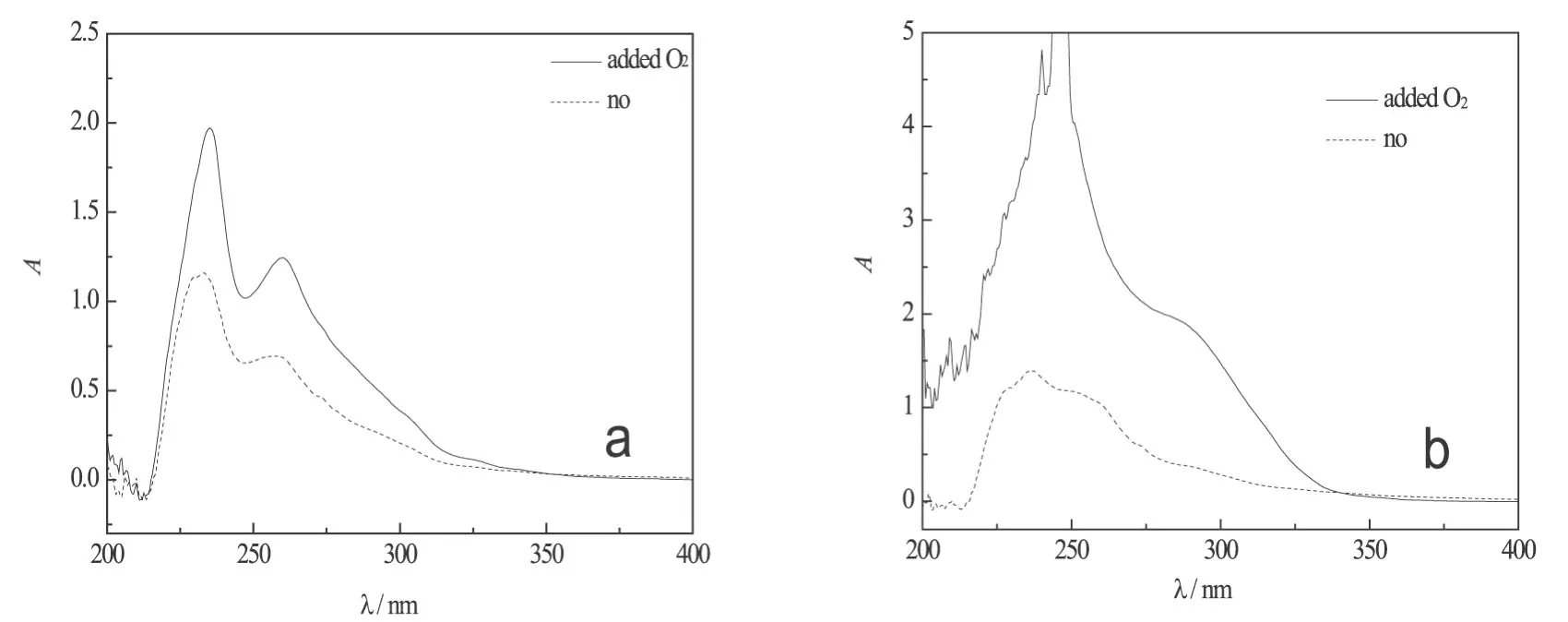
图4 不同气氛下氧化燃料b的吸收光谱(a,120℃-4h;b,160℃-2h)
图3显示了相同温度、通氧条件下和封闭条件下燃料a氧化后的紫外可见吸收光谱图,以未氧化燃料a为参比。其中燃料a在160℃氧化2 h后的紫外吸收是稀释10倍后的测试值。120℃封闭条件下,吸收峰非常不明显,而通氧条件下280~300 nm处吸收明显增强,且通氧条件下的吸收峰较封闭条件下的发生红移。图4显示了相同温度、通氧条件下和封闭条件下燃料b氧化后的紫外可见吸收光谱图,以燃料b为参比。通氧条件与封闭条件相比,吸收峰强度明显增大,且吸收峰红移。这是氧化程度加深的结果,通氧条件下,燃料中的溶解氧浓度一直处于饱和状态,燃料的氧化速度较封闭条件下快,燃料颜色变化也相对较快。
所以,溶氧量对燃料的安定性影响极大,在常温贮存时,要避免燃料中溶解氧含量的增加,隔绝空气或尽量减少燃料与空气的接触面积。
2.2 抗氧剂的复配作用
抗氧剂是延长燃料热氧化安定性的重要添加剂[7-8]。复合抗氧剂是由主、辅两种或两种以上抗氧剂复配而成,产生协同效应而发挥出优越性能。主要研究主抗氧剂BH T与辅抗氧剂168(亚磷酸酯类)在燃料a中复配,考察并评价其复配效果。
在140℃温度条件下,分别在将含有100 ppm主抗氧剂BH T、100 ppm辅抗氧剂168、100 ppm BH T +100 ppm 168和未添加抗氧剂的空白燃料试样的4支反应管,平行放入恒温油浴中,进行热氧化实验,观察燃料中氢过氧化物浓度随时间的变化情况。如图5所示,在燃料中添加100 ppm的168辅抗氧剂,其中对燃料中氢过氧化物的生成几乎没有抑制作用,氢过氧化物浓度从反应开始就迅速增大,与未添加抗氧剂的空白试样相差不大。而添加100 ppm BH T主抗氧剂的燃料样品,氢过氧化物浓度的变化明显呈两段式,第一个阶段,氧化抑制时间为12 h,12 h后BHT消耗完全,氢过氧化物迅速生成,浓度先增加后减小。在燃料中添加100 ppm BHT和100 ppm 168,抑制氧化时间较只添加100 ppmBH T有明显增长,由12 h增长至21 h。可见,168辅助抗氧剂本身并不能很好抑制氢过氧化物的生成,但将BHT和168复配在一起时,大大增强了抗氧化效果,延长了氧化抑制的时间。辅助抗氧剂可能是将热氧化链反应中生成的氢过氧化物分解,使之生成失去活性,从而终止或减缓热氧化。由于它与主抗氧剂常有协同效应,在与主抗氧剂并用时才能发挥最大的效果[9,10]。

图5 抗氧剂的复配对氢过氧化物的抑制
3 结论
采用碘量比色法跟踪测定了燃料a和b分别在饱和溶解氧和隔绝氧加热条件下氢过氧化物浓度随时间的变化,表明溶解氧的量对燃料a、b的自氧化反应影响非常大。通氧条件下燃料中生成氢过氧化物的含量大于封闭条件下的,但达到最大值所需的时间是封闭条件下的大于持续通氧条件下的,氧化诱导期大大延长,而且紫外吸收峰强度明显增大,且吸收峰红移。常温贮存燃料时要尽量减少燃料中溶解氧的含量。此外,辅助抗氧剂本身并不能很好抑制氢过氧化物的生成,但将BH T和168复配在一起时,主辅抗氧剂之间产生协同效应,大大增强了抗氧化效果,延长了氧化抑制的时间,使辅抗氧剂在与主抗氧剂并用时发挥最大的效果。
[1]Ervin J S,William s T F.Dissolved oxygen concentration and jet fuel deposition[J].Ind Eng Chem Res,1996,35(3):899-904.
[2]Pande S G,Hardy D R.Effectof copper,MDA,and accelerated aging on jet fuel thermal stability asmeasured by the gravimetric JFTOT[J].Energy&Fuels,1995,9(1):177-182.
[3]古玲,张香文,米镇涛.高密度燃料 HDF-1中过氧化物生成的研究[J].化学推进剂与高分子材料,2005,3(4):29-32.
[4]Zabarnick S.Pseudo-detailed chemical kinetic modeling of antioxidant chemistry for jet fuel[J].Energy&Fuels,1998, 12:547-553.
[5]Beaver B,Gao L,Burgess-Cliffo rd C,et a l.On themechanism sof fo rmation of thermaloxidative deposits in jet fuels.A re unified mechanism s possible fo r both sto rage and thermaloxidative deposit fo rmation fo rmiddle distillate fuels[J].Energy &Fuels,2005,19:1574-1579.
[6]Zabarnick S.Chemical kinetic modeling of jet fuel autoxidation and antioxidant chemistry[J].Ind Eng Chem Res,1993,32: 1012-1017.
[7]余金花,李丹,郭永胜,等.吸热型碳氢燃料的热氧化安定性研究[J].浙江大学学报:理学版,2007,34(2):185-188.
[8]孙海云,方文军,郭永胜,等.抗氧剂对燃料NNJ-150热氧化安定性的影响[J].高等化学工程学报,2006,20(3):455-459.
[9]蒋国柱,赵小艳.航空润滑油高温抗氧剂的研究进展[J].合成润滑材料,2005,32(1):32-35.
[10]王丽丽,潘炯玺,邱桂学,等.塑料用抗氧剂的应用技术和研究进展[J].塑料助剂,2005,(3):1-6.
(责任编辑:刘乃生)
2010-09-16
李丹(1983-),女,山东淄博人,潍坊学院化学化工学院讲师,博士。
TE624.81 文献标识码:A 文章编码:1671-4288(2010)06-0089-04
