高分散TiO2/SBA-15的制备及光催化性能
2010-12-05张书翠李君华
张书翠 姜 东 唐 涛 李君华 徐 耀
(1中国科学院山西煤炭化学研究所,煤转化国家重点实验室,太原 030001;2中国科学院研究生院,北京 100049)
高分散TiO2/SBA-15的制备及光催化性能
张书翠1,2姜 东1,*唐 涛1,2李君华1,2徐 耀1,*
(1中国科学院山西煤炭化学研究所,煤转化国家重点实验室,太原 030001;2中国科学院研究生院,北京 100049)
提出了一种制备高分散TiO2/SBA-15光催化剂的新方法.以钛酸四正丁酯(TB)和羧基改性的SBA-15 (COOH/SBA-15)为原料,利用COOH/SBA-15表面上高分散的羧基与TB的配合作用将TB锚定,经过溶剂热及焙烧处理制得TiO2/SBA-15光催化剂.采用粉末X射线衍射(XRD),N2吸脱附,傅里叶变换红外光谱(FT-IR),透射电镜(TEM)等对所得催化剂进行了表征.结果表明:所得TiO2/SBA-15光催化剂为高结晶度的锐钛矿晶型, TiO2均匀地分散在SBA-15表面,TiO2/SBA-15光催化剂保持较好的介孔特征结构,具有较大比表面积.以降解罗丹明B(RhB)为探针反应,考察了所得TiO2/SBA-15光催化剂的光催化性能.与后处理浸渍法制备的光催化剂相比,本文制备的TiO2/SBA-15光催化剂表现出了更加优越的光催化性能.
光催化;羧基改性;TiO2;SBA-15;溶剂热
TiO2作为一种重要的半导体光催化剂,由于其具有化学性质稳定、活性高、价廉无毒等优点,是目前研究最多的光催化材料,被认为是在环境治理领域最具开发前途的环保型光催化剂,在水处理、气体净化、自清洁及光解制氢材料制备等领域都有着广阔的应用前景[1-3].TiO2有三种晶型:锐钛矿、金红石和板钛矿,其中锐钛矿型在光催化方面表现出优越的性能.因此,锐钛矿TiO2的制备备受人们关注.目前,通过各种方法制备得到的锐钛矿TiO2,一般比表面积较小,对污染物的吸附能力较低,导致其光催化活性不佳,而且不易于回收,严重制约了其在工业上的应用.因此,将TiO2颗粒固定于介孔SiO2材料表面的研究受到了极大的关注.一方面,利用介孔SiO2材料高的比表面积增强TiO2对污染物的吸附能力,大大提高TiO2的光催化性能[4];另一方面,利用SiO2材料对紫外-可见光透明的性质[5],TiO2颗粒受光强度变化不大,光催化活性不会因负载而降低.而在众多的介孔SiO2材料中,SBA-15具有高度有序的六方介孔结构,均匀可调的孔径及大比表面积等优点,被认为是一种理想的光催化剂载体材料[6-7].这类将TiO2颗粒负载于SBA-15表面得到的TiO2/ SBA-15光催化剂显示出大的比表面积、好的水中分散性及高的氧化活性等特性,表现出优越的光催化性能[8-10].
目前制备TiO2/SBA-15光催化剂的方法主要有两种:后处理法(浸渍[11]、溶胶-凝胶[12]、嫁接[13])和直接合成法(原位反应法[14]).前者是先合成介孔SBA-15材料,然后在SBA-15的醇分散体系中引入少量水,使钛的前驱体发生水解-缩聚形成TiO2颗粒沉积在SBA-15表面,最后经高温处理制得TiO2/SBA-15光催化剂.但负载的TiO2颗粒在介孔上分散不均,且容易造成孔道堵塞,TiO2负载量也比较难控制;后者则是采用一步法直接合成TiO2/SBA-15光催化剂,在模板剂的作用下,硅源与钛源通过共水解-缩聚作用自组装形成TiO2/SBA-15光催化剂. TiO2颗粒与SBA-15是同时形成的,TiO2作为介孔骨架的成份,其负载量在一定程度上影响介孔结构的形成,而且所得的TiO2/SBA-15光催化剂的比表面积比较小,无法凸显介孔SBA-15材料的优势,影响其光催化性能的提高.
为了更好地克服上述方法存在的不足,本文基于本课题组早期的工作[15-16],提出了一种制备TiO2/ SBA-15光催化剂的新方法.利用COOH/SBA-15表面高度分散的羧基与钛酸四正丁酯(TB)的配合作用首先将TB分子锚定,经过溶剂热处理[15]得到TiO2/ SBA-15光催化剂,最后通过焙烧来提高TiO2颗粒的结晶度及除去残留的有机物.由于COOH/SBA-15表面羧基的均匀分散使得所形成的TiO2颗粒也均匀地分散于SBA-15表面.采用这种方法制备出了不同TiO2负载量的TiO2/SBA-15光催化剂,并采用XRD、FT-IR、TEM和N2吸脱附等手段对其进行了表征.在紫外光降解罗丹明B(RhB)的实验中,与后处理浸渍法制备的TiO2/SBA-15光催化剂相比,该TiO2/SBA-15光催化剂表现出了更加优越的光催化性能.
1 实验
1.1 试 剂
正硅酸乙酯(分析纯,简称TEOS,北京化学试剂公司),2-氰基乙基三乙氧基硅烷(纯度>97%(w),简称CETES,Alfa Aesar),钛酸四正丁酯(化学纯,简称TB,国药集团化学试剂有限公司),表面活性剂P123(EO20-PO70-EO20,分子量为5800,Aldrich),无水乙醇(分析纯,北京化学试剂公司),氯化钾(分析纯,天津市天力化学试剂有限公司),盐酸(分析纯,太原化肥厂化学试剂厂),浓硫酸(分析纯,太原化肥厂化学试剂厂),P25 TiO2(Degussa),去离子水(本所生产,经树脂交换).
1.2 催化剂的制备
COOH/SBA-15的合成方法参考本课题组的工作[16],以正硅酸乙酯(TEOS)、氰基乙基三乙氧基硅烷(CETES)为硅源(CETES与TEOS的摩尔比为1∶1), P123为模板剂,将4.0 g P123和4.0 g KCl加入到120 mL 2.0 mol·L-1的HCl溶液中,40℃恒温搅拌至P123完全溶解后缓慢加入CETES,继续搅拌30 min后加入TEOS,于40℃恒温搅拌24 h后移入特弗隆自压釜,在90℃烘箱中老化36 h,所得产物经过滤、水洗和醇洗(无水乙醇)后于60℃干燥得到氰基官能化SBA-15(CN/SBA-15).最后,将1.0 g CN/ SBA-15加入到150 mL H2SO4(48.0%,w)溶液中,95℃恒温搅拌24 h,过滤、水洗,80℃干燥即可得到COOH/SBA-15.
TiO2/SBA-15光催化剂的典型合成过程如下:以钛酸四正丁酯(TB)为钛源,室温下将0.002 mol TB和0.020 mol COOH/SBA-15分散于25 mL无水乙醇中,搅拌30 min后转移至聚四弗乙烯自压釜中,于220℃下溶剂热处理12 h,所得到的产物经无水乙醇洗涤三次后,60℃真空干燥.最后,在550℃下焙烧4 h得到TiO2/SBA-15光催化剂,样品被命名为TSEtx,其中x为羧基与TB的摩尔比,COOH/ SBA-15样品中羧基的相对含量的确定见文献[16].
作为对比,首先合成了纯硅SBA-15材料[6],然后以纯硅SBA-15为原料采用后处理浸渍法[11]制备TiO2/SBA-15光催化剂,其中 TiO2的负载量与TSEt5样品中TiO2的负载量相同,将该样品命名为post-synthesis.
1.3 催化剂的表征
样品的X射线粉末衍射(XRD)分析在D8 Advance型X射线衍射仪(德国Bruker AXS公司)上进行,扫描范围10°-80°,管电压40 kV,管电流100 mA,入射光为Cu Kα(λ=0.15406 nm).样品的傅里叶变换红外(FT-IR)光谱分析采用Nicolet-470型(美国热电公司)红外光谱仪测定,使用KBr压片技术制样,分辨率为4 cm-1.采用JEOL-2010型(日本电气公司)高分辨透射电子显微镜(HRTEM)观察样品颗粒形貌及晶格条纹.采用Tristar-3000型(美国麦克公司)Mi-cromeritics自动物理吸附仪测定样品孔结构,样品首先在100℃下真空处理12 h.样品的拉曼光谱分析采用LabRAM型显微激光拉曼光谱仪(法国J.Y.公司)进行测试,拉曼光谱检测范围100-800 cm-1,选用激光器波长为514.5 nm.采用PHI-5300型(美国Perkin-Elmer Physics Electronics公司)X射线光电子能谱(XPS)分析样品的表面化学组成及其结合能情况,电子结合能以污染炭的C 1s的结合能(284.6 eV)校准.29Si MAS NMR分析在Bruker MSL-400型(德国Bruker公司)超导核磁共振分析仪上进行,29Si MAS NMR共振频率为79.46 MHz,相对磁场强度为9.4 T,以高岭土为标样.
1.4 催化剂活性评价
紫外光催化实验在多功能光化学反应仪(SGY-1型,江苏省环境科学研究所研制)上进行,用300 W的高压汞灯为紫外光源,其波长集中分布在365 nm处,高压汞灯置于石英冷肼中.为了保持溶液温度稳定,石英冷肼通循环冷却水.催化剂悬浮于500 mL浓度为50.0 mg·L-1(C0)的RhB水溶液中,催化剂用量为1.0 g·L-1,反应在室温下进行.光照前,首先在避光条件下搅拌40 min,使RhB光催化剂表面达到吸附/脱附平衡(此时的RhB的浓度为Ce,光催化剂的吸附能力通过C0-Ce来表示),然后打开高压汞灯在紫外光照射下反应50 min,间隔10 min取样,每次取样5 mL,将所取样离心后,稀释5倍,采用普析通用TU-1901双光束紫外-可见分光光度计(波长554 nm)测定RhB溶液浓度.具体方法是:配制一系列已知浓度的RhB溶液(2.5、5.0、7.5、10.0, 12.5 mg·L-1),然后对其进行吸光度测定,最终可以得到浓度与吸光度的一条标准曲线,光催化反应过程中所得溶液只要测得其吸光度即可从标准曲线上得知其浓度.
2 结果与讨论
2.1 TiO2/SBA-15光催化剂的形成
TiO2/SBA-15光催化剂的制备过程如示意图1所示,整个制备过程可以分为三步.(1)合成COOH/ SBA-15.首先,硅源CETES和TEOS及表面活性剂P123在酸性条件下通过共水解-缩聚形成CN/SBA-15.由于在合成 CN/SBA-15的过程中,反应物CETES、TEOS、P123在酸性溶液中实现了分子水平上的组装,经过硫酸酸解处理去除模板剂和产生羧基后,得到的—COOH将均匀分散在SBA-15表面. (2)合成TiO2/SBA-15.将所合成的COOH/SBA-15和TB分散于乙醇溶剂中,COOH/SBA-15表面高分散的羧基通过与TB的配合作用首先将TB锚定,然后通过溶剂热处理将TB转化成TiO2颗粒,最后形成TiO2/SBA-15.⑶焙烧TiO2/SBA-15.通过焙烧来提高TiO2颗粒的结晶度及除去残留的有机物,最终得到TiO2颗粒均匀分散的TiO2/SBA-15光催化剂.
2.2 TiO2/SBA-15光催化剂的性质
2.2.1 TiO2/SBA-15光催化剂的表面性质
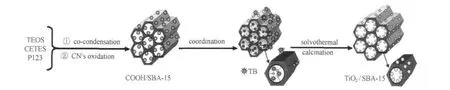
示意图1 TiO2/SBA-15光催化剂的制备过程Scheme 1 Preparation of TiO2/SBA-15 photocatalyst
相比于纯TiO2的红外谱图(图1)可以发现,所有TiO2/SBA-15光催化剂样品(TSEt3、TSEt5、TSEt7)的红外谱图在1086和800 cm-1处都出现了两个新的振动吸收峰,这两个吸收峰可分别归属为Si—O—Si键的不对称和对称伸缩振动峰[17].对纯TiO2, 400-600 cm-1之间的吸收峰是典型的Ti—O—Ti的振动吸收峰,而对纯硅SBA-15来说,459 cm-1处的吸收峰为Si—O—Si键的弯曲振动峰.从红外图中可以看出,TiO2/SBA-15光催化剂样品中的Si—O—Si键和Ti—O—Ti键在459 cm-1处出现了重叠.此外,与纯硅SBA-15相比较,COOH/SBA-15样品在1717 cm-1处出现强的吸收峰,而经过高温处理的COOH/SBA-15样品此峰消失,表明该处的吸收峰为羧基中C=O的特征振动峰[16].通常认为,910-960 cm-1之间的吸收峰可归属为Ti—O—Si键的伸缩振动[18],而对纯硅SBA-15,940-960 cm-1之间的吸收峰归属为Si—OH键[19],所以TiO2/SBA-15光催化剂样品红外谱图中952 cm-1处的吸收峰可能是Ti—O—Si键及Si—OH键吸收峰发生了交迭,表明样品中可能存在Ti—O—Si键及未发生聚合的Si—OH键.

为了进一步研究该光催化剂样品表面原子的结合情况,X射线光电子能谱(XPS)被用来对所得TiO2/SBA-15光催化剂进行表征,具体结果见表1.从表中可知,与纯TiO2相比,光催化剂样品的结合能有明显的增加.这种结合能的增加主要是由于电负性大的Si取代了Ti—O—Ti中电负性小的Ti形成Ti—O—Si键,从而使Ti—O键电子云密度增加导致结合能增加[20].XPS的结果也证实了TiO2/SBA-15光催化剂中存在Ti—O—Si键,这与红外光谱的结果相吻合.

表1 TiO2/SBA-15样品的O 1s、Ti 2p1/2、Ti 2p3/2的结合能Table 1 O 1s,Ti 2p1/2,and Ti 2p3/2binding energies of TiO2/SBA-15 samples
2.2.2 TiO2/SBA-15光催化剂的晶型
图2为TiO2/SBA-15光催化剂样品(TSEt3, TSEt5,TSEt7)的XRD(a)和拉曼(b)谱图.从图2(a)中可知,TiO2/SBA-15光催化剂样品在20°-60°之间出现五个衍射峰,分别对应于锐钛矿的(101)、(004)、(200)、(105)、(211)晶面的衍射峰,说明TiO2/SBA-15光催化剂表面的TiO2颗粒均为锐钛矿晶型.此外,从图2a中还可以发现所有的样品的(101)衍射峰均较强,呈现一个趋势,即随着TiO2含量的逐渐增加(n(—COOH)/n(TB)降低),(101)衍射峰的强度有所增强.当n(—COOH)/n(TB)=3时,TSEt3光催化剂样品的(101)衍射峰强度最强.一般认为在XRD谱图中,衍射峰的强度与结晶度和TiO2含量有关,样品结晶度越高,且TiO2含量越大,衍射峰强度就越强.从图2(b)可知,所有样品的拉曼图谱峰形一致,在拉曼光谱中的出峰位置相同,这些峰分别位于146.6、399.3、517.4、640.3 cm-1,与锐钛矿TiO2的四个特征拉曼模式(Eg,B1g,A1g和Eg)完全对应,说明催化剂为锐钛矿晶型[21-22],并且在拉曼谱图中没有发现其他晶型的散射峰,进一步说明催化剂样品为单一的锐钛矿TiO2,与XRD的结果相一致.

图2 TiO2/SBA-15样品的XRD(a)和拉曼(b)谱图Fig.2 XRD(a)and Raman(b)spectra of TiO2/SBA-15 samples

图3 TiO2/SBA-15样品的(a)N2吸脱附曲线和(b)孔径分布图Fig.3 N2adsorption isotherms(a)and pore size distributions patterns(b)of TiO2/SBA-15 samples
2.2.3 TiO2/SBA-15光催化剂的孔结构
图3所示为TiO2/SBA-15光催化剂(TSEt3、TSEt5、TSEt7、post-synthesis)和COOH/SBA-15样品的N2吸脱附曲线(a)和孔径分布图(b).从图3(a)中可以看出,COOH/SBA-15样品呈现出了介孔典型的IV型吸附等温线,说明对SBA-15进行羧基改性并没有破坏SBA-15材料的介孔结构.而且,从图3(a)中还可以发现,与COOH/SBA-15样品的吸附等温线不同,TiO2/SBA-15光催化剂样品的吸附等温线都发生了明显的变化,所有光催化剂样品吸附等温线的迟滞环均变为H3型 (狭缝状),迟滞环的改变表明在SBA-15表面形成了TiO2颗粒.另外,通过N2吸脱附曲线得出光催化剂样品TSEt3、TSEt5、TSEt7、post-synthesis的 BET比表面积分别为438.0、477.3、501.6、612.5 m2·g-1.
从图3(b)中可以看出,经过焙烧处理的COOH/ SBA-15样品的孔径为5.0 nm.而随着TiO2颗粒在COOH/SBA-15表面的形成,TiO2含量最低的TSEt7样品呈现出了独特的双孔分布,新的孔径出现在3.2 nm处.而且可以发现,随着TiO2含量的增加(n(—COOH)/n(TB)降低),3.2 nm处孔分布极大值的强度逐渐增加,而5.0 nm处的孔却逐渐降低.已知TSEt3样品的比表面积为438.0 m2·g-1,通过计算可得出每克SBA-15上的Ti原子数为3.3 Ti/nm2,这个值要小于锐钛矿TiO2的(010)晶面上Ti原子的密度5.5 Ti/nm2[23],说明当n(—COOH)/n(TB)=3时,所形成的TiO2颗粒还不足以完全覆盖整个SBA-15表面,随着n(—COOH)/n(TB)的增加,TiO2颗粒在SBA-15表面的覆盖度也随之降低.对制备的光催化剂样品来说,孔径的变化程度代表TiO2颗粒在SBA-15孔表面的覆盖程度,这是由—COOH与TB之间的精确相互作用引起的,而且由于COOH/ SBA-15表面的—COOH是均匀分散的,可知所形成的TiO2颗粒也是均匀分散在SBA-15表面.
图4所示为COOH/SBA-15及TSEt7光催化剂样品的HRTEM照片.从图4a中可以看出,合成的COOH/SBA-15样品具有介孔SBA-15材料规整的六方直孔道结构,说明对SBA-15进行羧基改性并没有破坏原有的介孔结构,对TSEt7催化剂样品来说,可以发现该样品也保持了比较规则的介孔结构(图4b),这说明TiO2颗粒的形成并没有破坏介孔材料的有序性,而且从图中还可以看出所形成的TiO2颗粒在SBA-15表面的分散也比较均匀.而且在图4c中显示了清晰的晶格条纹,通过测量得出其晶面间距大约为0.352 nm,这与锐钛矿TiO2的(101)晶面间距相一致,说明在SBA-15表面所形成的TiO2颗粒为锐钛矿晶型,这与XRD的结果相吻合.
2.2.4 TiO2/SBA-15光催化剂的紫外光催化性能
图5a是暗态情况下TiO2/SBA-15催化剂样品(TSEt3、TSEt5、TSEt7、post-synthesis、P25)对RhB的吸附能力曲线.由图5a可知,所有TiO2/SBA-15催化剂对RhB的吸附能力都高于P25,其中样品post-synthesis的吸附能力最强.通常认为,催化剂对目标降解物的吸附能力主要取决于催化剂的比表面积及其表面化学性质[24].毫无疑问,大的比表面积将有利于催化剂对RhB的吸附.由于本文所得催化剂均具有较大的比表面积,因此TSEt系列催化剂对RhB也显示出较强的吸附能力,从图中可以看出,以样品TSEt5对RhB的吸附能力为最强,其次是TSEt7、TSEt3.

图4 COOH/SBA-15样品(a)及TSEt7样品(b,c)的HRTEM照片Fig.4 HRTEM images of samples COOH/SBA-15(a)and TSEt7(b,c)
图 5b为 TiO2/SBA-15催化剂样品(TSEt3、TSEt5、TSEt7、post-synthesis、P25)在紫外光照射下对RhB的光催化降解曲线和无催化剂条件下紫外光照射RhB的光催化降解曲线.从图5b中可以看出,仅仅在紫外光照射下没有加催化剂,RhB也会被缓慢降解,但降解速度较慢,70 min仅有20%的RhB被降解.而本文所制备的光催化剂对RhB表现出显著的降解能力,样品TSEt3和TSEt7在50 min可以将RhB完全降解,其中样品TSEt5的降解能力最强,仅仅30 min就可以将RhB完全降解.因此,对于RhB溶液的降解主要归因于催化剂的光催化作用.为了突出本文所得催化剂的优越性,图5b中给出了被认为具有强降解能力的商业催化剂P25的光降解曲线,由图可知,P25表现出很好的光催化能力.与P25相比较,TSEt系列催化剂也具有同样优异的光催化性能,其中样品TSEt5更是表现出优于P25的降解能力.此外,图5b中还给出了采用后处理浸渍法所得催化剂post-synthesis的光降解曲线,从图中可以看出,与相同TiO2负载量的TSEt5样品相比,样品post-synthesis表现出较弱的光催化能力,70 min只有约80%被降解.一般认为,催化剂的紫外光催化性能主要与晶型,样品对目标降解物的吸附能力及TiO2颗粒在介孔材料表面的分散性等因素有关[25-26].对本文来说,所有样品均为高结晶度的锐钛矿TiO2,所以TSEt系列催化剂优越的光催化性能主要取决于其较高的吸附能力和TiO2颗粒在SBA-15表面较好的分散性.另外,由于该TiO2/SBA-15光催化剂中也存在少量的Ti—O—Si键,Ti—O—Si键的存在一方面使TiO2表面形成缺陷,不仅可以捕获光生电子或空穴以降低电子和空穴的复合几率[10],还增加了羟基的反应活性[27],另一方面也增强了表面酸性,这些都对光催化性能的提高有一定的作用.此外,由图5b可知,该TiO2/SBA-15光催化剂样品的光催化性能并非随着n(—COOH)/n(TB)比例的增大而提高,而是表现出了一定的差异,这应该是由光催化剂的比表面积和TiO2负载量共同作用引起的.随着n(—COOH)/ n(TB)的增加,样品的比表面积有所增加,但TiO2的负载量随之降低.当n(—COOH)/n(TB)=5时,表现出最佳的光催化性能应该是比表面积及TiO2负载量两种因素平衡作用的结果.

图5 TiO2/SBA-15样品对RhB的的吸附能力曲线(a)及其在紫外光照射下RhB的光催化降解曲线(b)Fig.5 Adsorption capacity(a)and photocatalytic degradation(b)for RhB under UV light of TiO2/SBA-15 samples
3 结论
利用COOH/SBA-15表面上高分散的羧基与TB的配合作用将TB锚定,然后通过溶剂热处理成功制备出TiO2颗粒均匀分散的负载型TiO2/SBA-15光催化剂.结果表明,该光催化剂具有较大的比表面积,保持了特征的介孔结构,所形成的高结晶度锐钛矿TiO2颗粒在SBA-15表面具有很好的分散性.在紫外光催化降解RhB的实验中,该TiO2/SBA-15光催化剂表现出了优越的光催化性能,其中,当n(—COOH)/n(TB)=5时,所得的TiO2/SBA-15光催化剂表现出最佳的紫外光催化能力.另外,此方法也为制备具有可见光催化活性的光催化剂提供了新的合成思路.
1 Zielinska,B.;Grzechulska,J.;Grzmil,B.;Antoni W,M.Appl. Catal.B-Environ.,2001,35:L1
2 Ohtani,B.;Ogawa,Y.;Nishimoto,S.J.Phys.Chem.B,1997,101 (19):3746
3 Hosseini,S.N.;Borghei,S.M.;Vossoughi,M.;Taghavinia,N. Appl.Catal.B-Environ.,2007,74:53
4 Stathatos,E.;Lianos,P.;Tsakiroglou,C.Microporous Mesoporous Mat.,2004,75:255
5 López-Muňoz,M.;van Grieken,R.;Aguado,J.;Marugán,J.Catal. Today,2005,101:307
6 Zhao,D.;Feng,J.;Huo,Q.;Melosh,N.;Fredrickson,G.H.; Chmelka,B.F.;Stucky,G.D.Science,1998,279:548
7 Perathoner,S.;Lanzafame,P.;Passalacqua,R.;Centi,G.;Schlögl, R.;Su,D.S.Microporous Mesoporous Mat.,2006,90:347
8 Chen,X.Q.;Gu,G.B.;Liu,H.B.Acta Chim.Sin.,2003,61:1714 [陈小泉,古国榜,刘焕彬.化学学报,2003,61:1714]
9 Li,Z.J.;Hou,B.;Xu,Y.;Wu,D.;Sun,Y.H.;Hu,W.;Deng,F. J.Solid State Chem.,2005,178:1395
10 Hoffmann,M.R.;Martin,S.T.;Choi,W.;Bahnemann,D.W. Chem.Rev.,1995,95:69
11 van Grieken,R.;Aguado,J.;López-Muňoz,M.J.;Marugán,J. J.Photoch.Photobiol.A,2002,148:315
12 Yang,J.;Zhang,J.;Zhu,L.W.;Chen,S.Y.;Zhang,Y.M.;Tang, Y.;Zhu,Y.L.;Li,Y.W.J.Hazard.Mater.,2006,137:952
13 Busuioc,A.M.;Meynen,V.;Beyers,E.;Cool,P.;Bilba,N.; Vansant,E.F.Catal.Commun.,2007,8:527
14 De Witte,K.;Busuioc,A.M.;Meynen,V.;Metens,M.;Bilba,N.; van Tendeloo,G.;Cool,P.;Vansant,E.F.Microporous Mesoporous Mat.,2008,110:100
15 Jiang,D.;Xu,Y.;Wu,D.;Sun,Y.H.Eur.J.Inorg.Chem.,2008, 1236
16 Xu,W.J.;Gao,Q.;Xu,Y.;Wu,D.;Sun,Y.H.;Shen,W.L.;Deng, F.J.Solid State Chem.,2008,181:2837
17 Jung,K.Y.;Park,S.B.Appl.Catal.B-Environ.,2000,25:249
18 Hu,Y.J.;Li,C.Z.;Cong,D.Z.;Jiang,H.B.;Zhao,Y.J.Inorg. Mater.,2007,22:205 [胡彦杰,李春忠,丛德滋,姜海波,赵 尹.无机材料学报,2007,22:205]
19 Llusar,M.;Monros,G.;Roux,C.;Pozzo,J.L.;Sanchez,C. J.Mater.Chem.,2003,13:2505
20 Li,Y.X.;Wang,T.H.;Peng,S.Q.;Lü,G.X.;Li,S.B.ActaPhys.-Chim.Sin.,2004,20:1434 [李越湘,王添辉,彭绍琴,吕功煊,李树本.物理化学学报,2004,20:1434]
21 Ohsaka,T.J.Phys.Soc.Jpn.,1980,48:1661
22 Ohsaka,T.;Izumi,F.;Fujiki,Y.J.Raman.Spectrosc.,1978,7: 321
23 Gao,X.T.;Bare,S.R.;Fierro,J.L.G.;Banares,M.A.;Wachs,I. E.J.Phys.Chem.B,1998,102:5653
24 Jiang,D.;Xu,Y.;Wu,D.;Sun,Y.H.J.Solid State Chem.,2008, 181:593
25 Minero,C.;Catozzo,F.;Pelizzetti,E.Langmuir,1992,8:481
26 Zhao,L.;Yu,J.G.J.Colloid Interface Sci.,2006,304:84
27 Liu,Y.Q.;Xu,Y.;Li,Z.J.;Zhang,X.P.;Wu,D.;Sun,Y.H.Acta Chim.Sin.,2006,64:453 [刘亚琴,徐 耀,李志杰,张秀萍,吴 东,孙予罕.化学学报,2006,64:453]
December 10,2009;Revised:January 13,2010;Published on Web:March 31,2010.
Synthesis and Photocatalytic Activity of Highly Dispersed TiO2/SBA-15
ZHANG Shu-Cui1,2JIANG Dong1,*TANG Tao1,2LI Jun-Hua1,2XU Yao1,*
(1State Key Laboratory of Coal Conversion,Institute of Coal Chemistry,Chinese Academy of Sciences, Taiyuan 030001,P.R.China;2Graduate University of Chinese Academy of Sciences,Beijing 100049,P.R.China)
Highly dispersed TiO2/SBA-15 photocatalysts were successfully synthesized by solvothermal treatment using titanium n-butoxide(TB)and carboxylate-modified SBA-15(COOH/SBA-15)as raw materials.The good dispersive carboxyl groups of COOH/SBA-15 coordinated with TB molecules to anchor them.After solvothermal treatment,the TB molecules were transformed into TiO2nanoparticles and finally formed the TiO2/SBA-15 products.The products were calcined to improve the crystallization of TiO2and to remove the organic compounds.As-obtained TiO2/SBA-15 photocatalysts were characterized by X-ray diffraction(XRD),nitrogen adsorption,Fourier transform infrared(FI-IR) spectroscopy,and transmission electron microscopy(TEM).Analytical results showed that the as-obtained TiO2/SBA-15 photocatalysts possessed a better mesoporous structure and a larger specific surface area.The highly crystalline anatase TiO2nanocrystals dispersed well on the surface of SBA-15.Rhodamine B(RhB),as a photodegradation target,was used to evaluate photocatalytic performance under UV light irradiation.The as-obtained TiO2/SBA-15 photocatalysts exhibited much better photocatalytic activity compared with the photocatalysts prepared by a post-synthesis impregnation method.
Photocatalysis;Carboxylate-modified;TiO2;SBA-15;Solvothermal
[Article] www.whxb.pku.edu.cn
*Corresponding authors.Email:xuyao@sxicc.ac.cn,jdred@sxicc.ac.cn;Tel:+86-351-4049859.
The project was supported by the State Key Laboratory of Coal Conversion(SKLCC)in-House Project,China(2008BWZ011).
煤转化国家重点实验室自主研究项目(2008BWZ011)资助
O643
