新型富勒烯膦金属配合物的合成
2010-11-26覃世辉吴振奕
覃世辉, 吴振奕
(1. 河池学院 化学与生命科学系,广西 宜州 546300;2. 厦门大学 化学化工学院 化学系,福建 厦门 361005)
富勒烯(C60)因具有独特的空间及电子结构,使它及其衍生物具有特殊的物理化学性质,已成为人们研究的热点。尤其是超导性[1]、磁性和非线性光学性质[2,3]等,更引起人们的关注,在光伏电池[4]、超导、催化[5~7]、建构纳米材料等方面有广泛应用。合成新型的含C60的化合物及研究其性质是富勒烯实际应用开发研究的基础,也是富勒烯化学研究的热点之一。
本文以1,5-双(二苯基膦)戊烷(dpppe)为配体,Pd为中心金属,采用配体取代法合成了新型富勒烯膦金属配合物——C60·双(二苯基膦)戊烷合钯[C60Pd(dpppe)](1, Scheme 1),其结构经UV-Vis, IR, XPS及元素分析表征。结果表明,在1的分子结构中,C60以σ-π配位方式与Pd配位,形成新型的η2-C60双齿膦金属配合物。
1 实验部分
1.1 仪器与试剂
日本岛津2501PC型紫外-可见分光光度计(甲苯为溶剂);美国PE Nieolet AVATAR FT-IR 360型红外分光光谱仪(KBr压片);意大利Calo Erba-1110型元素分析仪;英国VG ESCABMK-Ⅱ型能谱仪(XPS)。
dpppe,北京京泽旺化工有限公司;C60,武汉大学三维碳簇材料有限公司;柱层析用中性氧化铝,200目~300目;其余所用试剂均为分析纯。
1.2 合成
(1) 2的合成
在反应瓶中加入PdCl20.1 g,用N2气冲洗三次。加入dpppe 0.70 g的DMSO溶液1.8 mL,搅拌下于140 ℃反应30 min。缓慢滴加水合肼0.22 mL,反应激烈,有N2生成。水浴冷却,慢慢冷却至室温(在约125 ℃时析出黄色晶体),过滤,滤饼分别用乙醇(2×1 mL)和乙醚(2×1 mL)洗涤,真空干燥得土黄色粉末2 203 mg,产率36.8%; UVλ: 365.4 nm。
(2) 1的合成
在反应瓶中加入2 49.3 mg, N2气氛下加入C6036 mg的甲苯溶液15 mL(溶液呈墨绿色),于室温搅拌反应3 h。过柱(洗脱剂:甲苯),收集墨绿色溶液,减压浓缩至3 mL左右,加入正己烷,有墨绿色沉淀析出,过滤,滤饼分别用正己烷(2×1 mL)和乙醚(2×1 mL)洗涤,真空干燥得墨绿色粉末1 34 mg,产率53.7%; UVλ: 259.7, 331.5, 447.3, 619.8 nm; Anal.calad for C60Pd(dpppe): C 84.36, H 2.37; found C 83.60, H 2.09。
2 结果与讨论
在1的UV数据中,447.3 nm和619.8 nm为η2型C60金属配合物的特征峰[8],证明C60与Pd以σ-π方式配位;259.7 nm和331.5 nm为C60的特征峰。
1和2的IR谱图见图1。由图1可见,2中2 932 cm-1, 2 855(CH2) cm-1, 1 186(C-C) cm-1, 1 101[P-(CH2)] cm-1处的吸收峰向低波数方向移动,分别移至2 921 cm-1, 2 849 cm-1, 1 182 cm-1和1 099 cm-1处,这可能是C60取代了一个dpppe后,由于C60的缺电子性使Pd(dpppe)上的电子密度下降所致。1于576 cm-1和526 cm-1处出现新的吸收峰,而2原来的1 481 cm-1和999 cm-1处的吸收峰消失;1保留了C60和膦配体的特征吸收峰(526 cm-1, 576 cm-1, 739 cm-1, 695 cm-1)。吸收峰的变化和特征峰的有所保留印证了新化合物的生成。
1的XPS谱图见图2。单质Pd(0)的3d5/2的电子结合能(BE0)为335.1 eV,与1具有形似配位环境的Pd(PPh3)2Cl2的Pd(Ⅱ)的3d5/2的BE2为337.8 eV,而1的Pd 3d5/2的BE0为336.4 eV。可推知,1中心金属Pd的价态介于0价与+1价之间,呈低价态。这说明C60与Pd以σ-π协同作用方式成键。
综上所述,C60与2发生了配位取代反应,C60以σ-π配位方式取代了2中的一个dpppe生成了新配合物1,推测其结构如Chart 1所示。
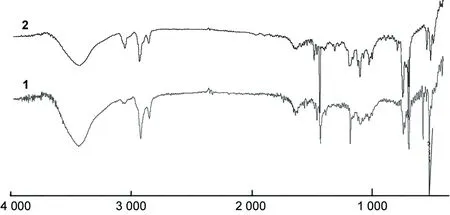
ν/cm-1图 1 1和2的IR谱图Figure 1 IR spectra of 1 and 2
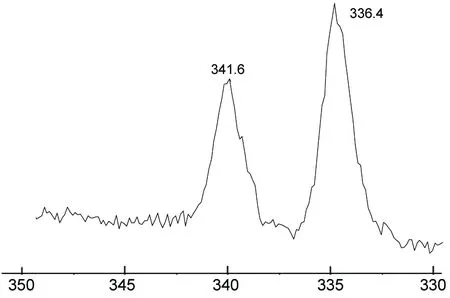
BE/eV图 2 1的XPS谱图Figure 2 XPS spectrum of 1
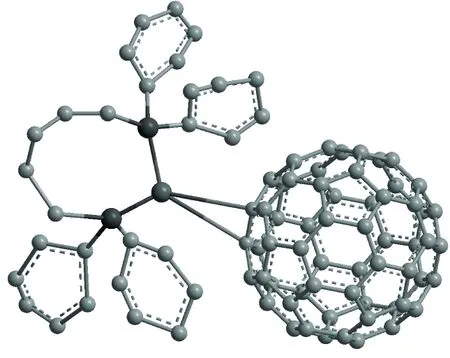
1Chart 1
[1] Ozadas E, Kortan A R, Kopylov N,etal. Superconductivity and cation-vacancy ording in the rare earth fulleride Yb2@C75[J].Nature,1995,375:126-129.
[2] Riggs J E, Sun Y P. Optical limiting properties of [60] fullerene and methano[60] fullerene derivative in solution versus in polymer matrix: the role of bimolecular processes and a consistent nonlinear absorption mechanism[J].J Phys Chem A,1999,103(4):485-495.
[3] Prato M. [60]Fullerene chemistry for materials science applications[J].J Mater Chem,1997,7(7):1097-1109.
[4] Imahori H, Kashiwagi Y, Hasobe T,etal. Porphyrin and fullerene-based artificial photosynthetic materials for photovoltaics[J].Thin Solid Films,2004,451-452:580-588.
[5] Pignolet L I. Homogenaus Catalysis with Metal Phosphine Complexes[M].New York:Plerum Press,1983.
[6] Alyea E C. Meek D W. Catalytic Aspects of Metal Phosphine Complexes[M].ACS Advanes in Chemistry Series,1982.
[7] Yuanyin Chen, Rongshen Sheng, Ying Liu.(η2-C60)Pt(PPh3)2as the catalyst for the hydrosilylation of olefins[J].Chemical Research in Chinese Universities,1994,10:338-340.
[8] Youichi I, Hidenori H, Yasushi H,etal. Preparation and characterization of rhodium C60complexes[Rh(acac)(L)2(C60)](L=Py,4-MePy,3,5-Me2Py)[J].Chem Lett,1994,(4):801-804.
