新型1,4,5,8-萘酰亚胺类衍生物的合成 *
2010-11-26刘万定吕良飞吴杰颖
刘万定, 吕良飞, 汪 维, 陈 梅, 唐 超, 吴杰颖
(安徽大学 化学化工学院,安徽 合肥 230039)
1,4,5,8-萘酰亚胺类衍生物具有较大的共轭体系,较好的分子共平面性,较低的LUMO能级,利于电子的交流与传输,使其在太阳能转化[1,2]、光导体、电致发光、n型半导体材料[3]、气体存储材料[4~6]、离子识别、生物荧光探针、DNA剪切[7]和抗癌药物等方面有着广泛的应用前景。近几年来,国内外已有很多此方面的研究报道,但文献报道的大多数是对称的萘酰亚胺类衍生物,而不对称的衍生物合成较困难,至今鲜见报道。
本文以1,4,5,8-萘四甲酸二酐(1)和2-乙基己胺(2)为原料,设计并合成了3种新型的1,4,5,8-萘酰亚胺类衍生物(L1~L3, Scheme 1),其结构经1H NMR, IR和MS表征。对中间体N-(2-乙基己基)-萘-1,8-二甲酸单酐-4,5-单甲酰亚胺(L0)的最佳反应条件进行了优化。
1 实验部分
1.1 仪器与试剂
Bruker 400 Ultrashield型核磁共振仪(CDCl3为溶剂,TMS为内标);Nicolet FT-IR-870SX型红外光谱仪(KBr压片);Micromass GCT-MS型质谱仪(EI源)。

Scheme1
1,工业品,用前经纯化处理;2, 2-氨基吡啶,Alfa Aesar;2-氨基-4,6-二甲基嘧啶按文献[8]方法合成;其余所用试剂均为市售分析或化学纯,直接使用或按标准方法纯化后使用。
1.2 合成
(1) L0的合成
在三口烧瓶中加入1 2.60 g(9.70 mmol)和DMF 20 mL, N2保护下加热至140 ℃;加入醋酸锌0.2 g,缓慢滴加2 1.14 g(8.82 mmol),滴毕,回流反应15 h。冷却至室温,过滤,滤液减压蒸除DMF,残留物用CH2Cl2溶解;过滤,滤液浓缩至干,经柱层析[洗脱剂:A=V(石油醚) ∶V(乙酸乙酯)=8 ∶1]纯化得浅黄色固体L00.92 g,产率25%;1H NMRδ: 0.87~0.92(t, 3H, CH3), 0.94~0.98(t, 3H, CH3), 1.28~1.40(m, 8H, CH2in Bu), 1.92~1.99(m, 1H, CH), 4.14~4.21(m, 2H, CH2CH3), 8.84(s, 4H, ArH); IRν: 3 084, 2 955, 2 928, 2 860, 1 795, 1 759, 1 705, 1 669, 1 582, 1 450, 1 333, 1 285, 1 238, 1 028, 764, 708 cm-1; EI-MSm/z: 379.14[M+]。
(2)N,N-(2-乙基己基)-萘四甲酰二亚胺(L1)的合成
在三口烧瓶中加入1 2.00 g(7.46 mmol)和冰乙酸50 mL, N2保护下慢慢滴加2 2.43 g(18.7 mmol),滴毕,于100 ℃(回流)反应5 h。冷却至室温,有大量白色固体生成,抽滤,滤饼用水洗涤多次,真空干燥得白色固体L13.47 g,产率95%;1H NMRδ: 0.88~0.92(t, 6H, CH3), 0.94~0.98(t, 6H, CH3), 1.27~1.43(m, 16H, CH2in Bu), 1.91~2.00(m, 2H, CH), 4.11~4.21(m, 4H, CH2CH3), 8.77(s, 4H, ArH); IRν: 3 080, 2 961, 2 930, 2 858, 1 702, 1 657, 1 581, 1 455, 1 375, 1 338, 1 243, 1 184, 1 090, 772, 717 cm-1; EI-MSm/z: 490.28[M+]。
(3) L2和L3的合成
在三口烧瓶中依次加入L00.31 g(0.82 mmol), 2-氨基吡啶0.15 g(1.60 mmol)及DMF 20 mL, N2保护下加热至140 ℃(回流)反应5 h。减压蒸馏除去溶剂,残留物用CH2Cl2溶解;过滤,滤液浓缩至干,经经柱层析(洗脱剂:A=2 ∶1)纯化得浅黄色固体N-(2-乙基己基)-N-(2-吡啶)萘四甲酰二亚胺(L2)0.21 g,产率57%;1H NMRδ: 0.90~0.93(t, 3H, CH3), 0.96~1.00(t, 3H, CH3), 1.34~1.46(m, 8H, CH2in Bu), 1.95~2.02(m, 1H, CH), 4.14~4.24(m, 2H, CH2CH3), 7.46~7.48(d, 1H, ArH), 7.53~7.56(q, 1H, ArH), 8.00~8.05(m, 1H, ArH), 8.77~8.78(m, 1H, ArH), 8.83(s, 4H, ArH); IRν: 3 082, 2 958, 2 931, 1 707, 1 659, 1 581, 1 452, 1 370, 1 346, 1 246, 1 195, 1 095, 881, 769, 746 cm-1; EI-MSm/z: 455.18[M+]。
用2-氨基-4,6-二甲基嘧啶(0.20 g, 1.60 mmol)替代2-氨基吡啶,同法制得深黄色固体N-(2-乙基己基)-N-(4,6-二甲基嘧啶)萘四甲酰二亚胺(L3) 0.11 g,产率43%;1H NMRδ: 0.90~0.94(t, 3H, CH3), 0.96~1.00(t, 3H, CH3), 1.32~1.46(m, 8H, CH2in Bu), 1.95~2.02(m, 1H, CH), 2.65(s, 6H, CH3), 4.13~4.24(m, 2H, CH2CH3), 7.25(s, 1H, PyH), 8.81(s, 4H, ArH); IRν: 3 079, 2 960, 2 929, 2 859, 1 722, 1 710, 1 669, 1 600, 1 583, 1 533, 1 449, 1 371, 1 348, 1 332, 1 249, 1 207, 880, 767, 723 cm-1; EI-MSm/z: 484.21[M+]。
2 结果与讨论
本文在合成一种对称的萘酰亚胺(L1)的同时,尝试并成功合成了两种不对称的萘酰亚胺L2和L3。 L0作为合成L2和L3的关键中间体,对其进行工艺优化十分须要。
2.1 合成L0的反应条件选择
(1) 投料比r=n(1) ∶n(2)
1 9.7 mmol, DMF 20 mL,其余反应条件同1.2(1),考察r对L0产率的影响,结果见表1。由表1可见,当r<1时,2过量,双边产物L1增多,L0产率降低;当r>1时,L0产率有明显的提高;r=1.1时,L0产率最高。
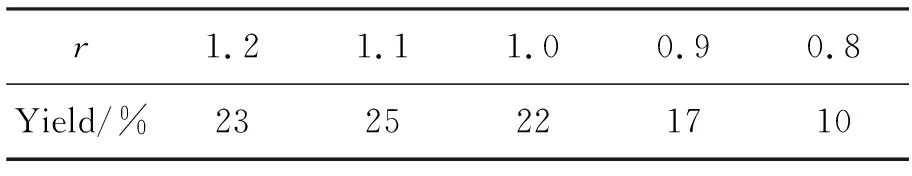
表 1 r对L0产率的影响*Table 1 Effect of r on yields of L0
*1 9.7 mmol, DMF 20 mL,其余反应条件同1.2(1);r=n(1) ∶n(2)
(2) 反应时间
r=1.1,其余反应条件同2.1,考察反应时间对L0产率的影响,结果见表2。由表2可见,反应时间以15 h为宜。反应时间过长,双边产物L1增多,L0则减少;反应时间过短,反应不完全,导致L0产率降低。

表 2 反应时间对L0产率的影响*Table 2 Effect of reaction time on yields of L0
*r=1.1,其余反应条件同表1
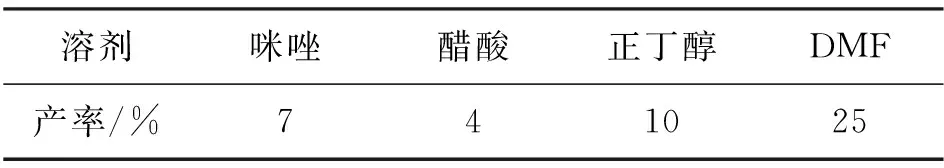
表 3 溶剂对L0产率的影响*Table 3 Effect of solvent on yields of L0
*r=1.1,其余反应条件同表1
(3) 溶剂
r=1.1,其余反应条件同2.1,考察溶剂对L0产率的影响,结果见表3。从表3可见,以DMF为溶剂时,L0的产率最高。
(4) 催化剂
r=1.1,其余反应条件同2.1,考察催化剂对L0产率的影响,结果表明,醋酸锌的加入与否对L0产率影响非常大。未加入醋酸锌时,L0的产率仅为8%;加入醋酸锌,L0产率可达25%。
综上所述,合成L0的最佳反应条件为:1 9.7 mmol,n(1) ∶n(2)=1.1,以醋酸锌为催化剂,在DMF(20 mL)中于140 ℃反应15 h,收率25%。尽管L0的产率不高,但以此为中间体合成了两种不对称的萘酰亚胺类衍生物,为萘酰亚胺类材料的合成提供了新的思路。
[1] Ganesan P, Yang X N, Sudholter E J R. Tetrahedral n-type materials:Efficient quenching of the excitation of p-type polymers in amorphous films[J].J Am Chem Soc,2005,127(42):14530-14531.
[2] Hoppe H, Sariciftci N S. Conjugated polymer-based organic solar cells[J].J Mater Res,2004,19:1924-1945.
[3] Kao C C, Lin P, Yan J Y,etal. Solid-state structure of the naphthalene-based n-type semiconductors and performance improved with mo-based source/drain electrodes[J].Synthetic Matels,2008,158(7):299-305.
[4] Ma B Q, Mulfort K L, Hupp J T. Microporous pillared paddle-wheel frameworks based on mixed-ligand coordination of zinc ions[J].Inorg Chem,2005,44(14):4912-4914.
[5] Mulfort K L, Hupp J T. Chemical reduction of matal-organic framework materials as a method to enhance gas uptake and binding[J].J Am Chem Soc,2007,129(31):9604-9605.
[6] Pantos G D, Pengo P, Sanders J K M. Hydrogen-bonded helical organic nanotubes[J].Angew Chem Int Ed,2007,46:194-197.
[7] Chu Y, Sorey S, Hoffman D W,etal. Structural characterization of a rigidified threading bisintercalator[J].J Am Chem Soc,2007,129(5):1304-1311.
[8] 孔繁蕾,王兰青,胡新华,等. 2-氨基嘧啶类系列化合物的合成[J].化学世界,1991,32(6):254-257.
