温度、PH和盐对乳清蛋白乳状液稳定性的影响
2010-11-10郦金龙梅雪莹殷丽君
崔 健,郦金龙,王 盼,梅雪莹,殷丽君
(中国农业大学食品科学与营养工程学院,北京100083)
温度、PH和盐对乳清蛋白乳状液稳定性的影响
崔 健,郦金龙,王 盼,梅雪莹,殷丽君*
(中国农业大学食品科学与营养工程学院,北京100083)
乳清蛋白具有一定的乳化能力,在食品工业中常作为乳化剂使用。以乳清浓缩蛋白(WPC)、乳清水解蛋白(WPH)和乳清分离蛋白(WPI)为乳化剂,经高压均质制备O/W型乳状液,以平均粒径和分层系数为稳定性指标,研究了温度、pH和盐对乳状液稳定性的影响。结果表明:WPI乳状液具有最小的平均粒径。各环境因素对乳状液稳定性的研究表明,pH是影响乳状液稳定性最显著的因素,当pH在蛋白质等电点(4~6)附近时,各乳状液中粒子均发生絮凝或聚合,乳状液发生脱稳。受环境因素影响,WPC乳状液具有最好的稳定性。这些结果为乳清蛋白作为乳化剂用于食品工业提供了重要依据。
乳状液,乳清蛋白,稳定性,pH,平均粒径
1 材料与方法
1.1 材料与设备
Thermax34乳清浓缩蛋白(WPC,蛋白含量34.0%)、Thermax690水解乳清分离蛋白(WPH,蛋白含量90.0%~93.0%)、Provon290速溶乳清分离蛋白(WPI蛋白含量92.0%~95.0%) Glanbia公司;叠氮化钠 sigma公司;金龙鱼大豆油 当地超市(未纯化);磷酸二氢钠、磷酸氢二钠 国药集团;其它试剂 均为分析纯;蒸馏水 自制。
NS1001L高压均质机 意大利Niro Soavi公司;LS230激光粒度分析仪 美国贝克曼—库尔特公司;T25高速混匀机 德国 IKA公司;PB-21酸度计 德国赛多利斯公司;恒温磁力搅拌器 上海司乐仪器厂。
1.2 实验方法
1.2.1 乳状液的制备 水相:将1.0wt%的蛋白质与0.02wt%的叠氮化钠(防止微生物腐败)溶于50mmol/L的磷酸缓冲液中(pH7.0),室温下磁力搅拌4~6h,使蛋白质充分溶解。将油相(市售大豆油)与上述水相按质量比1∶9混合(体系总质量为200g),利用高速混匀机于19000r/min下混合1min。
将混匀后的乳液采用两级控制高压均质机进行均质,一级压力为500bar,二级压力50bar,均质一次。均质后的乳液于4℃储存。
1.2.2 稳定性测定
通过南通地名变迁,考察南通社会的发展变迁,社会进步,从而产生对社会的认可、对社会制度的理解、对社会环境资源配置的厚重感。南通从条件恶劣转变为不受气候天灾影响,从最偏僻唯恐避之不及的边疆转变为各方打工者怀揣梦想追逐之地,从只能从事围土晾晒的制盐业发展到农工商各行业发达;从少有文明种子播撒的蛮荒之地进化为尊师重教已经内化为传统习俗的文明之所,通过历史演变激发可以民众爱家乡爱国热情。
1.2.2.1 温度对乳状液稳定性的影响 取8mL新制备乳状液-18℃冷冻20h,分别于60、80℃加热1h,90℃加热15min后,降至室温,于4℃贮藏过夜,进行稳定性测定。
1.2.2.2 pH对乳状液稳定性的影响 用浓度为1mol/L的盐酸、氢氧化钠溶液调节乳状液的pH至3~11,于4℃贮藏过夜,进行稳定性测定。
1.2.2.3 盐对乳状液稳定性的影响 取8mL新制备的乳状液(pH=7),加入2.5mol/L的氯化钾溶液或0.5mol/L的氯化钙溶液,使乳状液中氯化钾浓度为0~500mmol/L,氯化钙的浓度为0~20mmol/L,于4℃贮藏过夜,进行稳定性测定。
1.2.3 稳定性指标[3]
1.2.3.1 粒径检测(Particle size measurement) 利用LS230激光粒度分析仪进行乳状液中粒子的粒径测定。粒径采用体积分数表示的平均粒径(d4,3)或粒径分布图表示。实验中大豆油的折射率为1.436,蒸馏水的折射率为1.33,粒子的吸收值为0.001。
1.2.3.2 分层系数(Creaming index) 取8mL处理后的乳状液于离心管中,在4℃贮藏24h后,乳状液发生分层现象,上相浑浊,下相澄清。
分层系数(%)=下相的高度HS/乳状液总高度HT×100%
2 结果与讨论
2.1 乳状液的成粒特性
图1和表1列出了分别采用乳清浓缩蛋白(WPC)、乳清水解蛋白(WPH)以及乳清分离蛋白(WPI)制备乳状液的粒径及分布。结果表明,乳清分离蛋白(WPI)制备的乳状液粒径最小,这可能是由于其具有较高的蛋白质含量,当用作乳化剂时,有足够多的蛋白质吸附到油滴表面,降低界面张力,形成稳定的乳状液[4]。
另外,WPH虽然具有较高的蛋白质含量,但在本研究中其乳化能力最差,形成的乳状液中粒子平均粒径大,这个结果与Chu等人采用乳清蛋白及其水解物制备纳米乳液不符[1],这可能是与蛋白质的水解程度不同有关。乳清蛋白的过度水解产生了较多的小分子量多肽片段,可以降低水解蛋白的乳化能力[5]。此外,界面张力测定结果也表明本文选用的WPH界面张力大于WPI和WPC,也说明其乳化能力不如大分子蛋白质。
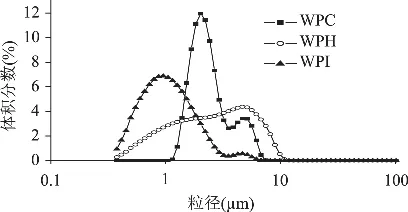
图1 不同乳清蛋白制备的乳状液粒子的粒径分布图

表1 不同乳化剂制备的乳状液粒子的粒径特性
2.2 温度对乳状液稳定性的影响
图2是几种乳清蛋白制备乳状液的热稳定特性。由图可见,几种乳清蛋白制备的乳状液表现出了不同的稳定特性。其中,WPC稳定的乳状液受温度影响变化较小,高温和冷冻-解冻处理下平均粒径都保持稳定;尽管加热处理对WPI稳定的乳状液粒径无明显影响,但冷冻-解冻处理对该乳状液的稳定性产生较大的影响,乳状液粒子平均粒径从1.26μm增加到2.29μm;WPH乳状液表现较好的稳定性,特别是冷冻-解冻处理对其粒径影响也很小,但是温度升高仍然会导致该乳状液粒子的平均粒径逐渐增大,并且90℃下处理15min后乳状液产生明显的絮凝或聚结现象,粒径也从2.65μm增加到3.48μm。在本文的各种温度处理条件下,所有乳状液都没有产生明显的乳状液分层现象。

图2 温度对乳状液粒子平均粒径的影响
从上述结果可知,在本文所研究的加热和冷冻处理条件下,WPH乳状液对热处理表现较为敏感,而WPI乳状液对冷冻-解冻处理比较敏感。蛋白质在乳化过程中通过自身结构旋转吸附在乳化界面上降低表面张力,然而加热过程可以改变蛋白质原有的吸附状态,蛋白质结构伸展,其内部非极性的基团更多地暴露在水相中,从而降低其稳定性。对于乳清蛋白来讲,其主要成分为球形蛋白α-乳白蛋白和β-乳球蛋白,加热可以使得展开的α-乳白蛋白和β-乳球蛋白将带二硫键的氨基酸片段和非极性端也暴露于水相中[6],这些活性氨基酸的暴露促进了蛋白质之间的疏水作用和二硫键作用,导致聚合[7]。本文中WPH表现出来的热稳定性较差,可能原因在于WPH自身的乳化能力较低,另外蛋白质的水解也暴露了更多的疏水基团,从而导致了较低的热稳定性。
冷冻处理可以在乳状液水相中形成冰晶,使得乳状液粒子浓度和水相中的离子强度升高,粒子间距缩小,蛋白质分子间相互作用力增强,从而引起乳状液在冷冻解冻过程中液滴的聚合,这可能是WPI乳状液对冷冻非常敏感的原因[8]。本文中WPC的蛋白质浓度较低,受蛋白质分子间作用力和离子强度升高的影响更小,而WPI和WPH具有较高的蛋白质含量,但是WPH大多为蛋白质的水解肽,具有更好的溶解能力,因此也表现出一定的蛋白质凝集现象。另外,形成的冰晶可以划破粒子界面乳化薄膜,引发乳状液的破乳,从而导致粒径的增大[9]。
2.3 pH对乳状液稳定性的影响
由图3可知,在乳清蛋白的等电点附近(pH4~6),各蛋白稳定的乳状液均表现出粒径增大、分层等脱稳现象;在pH=3和pH6~11时,各乳状液具有高的稳定性。这是由于在等电点附近,蛋白质的溶解度降低,形成乳状液的能力下降;而且此时蛋白质粒子表面的电荷量较低,粒子间的静电排斥力降低,易发生絮凝或聚合,表现为乳状液的粒子粒径增大。但当pH远离等电点时,液滴带负电荷(如pH=3)或带正电荷(pH≥6),带电液滴间排斥力大于相互吸引的范德华力,液滴不会相互凝聚,乳状液具有高度的稳定性[10]。
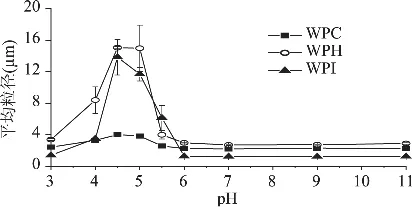
图3 pH对乳状液粒子平均粒径的影响
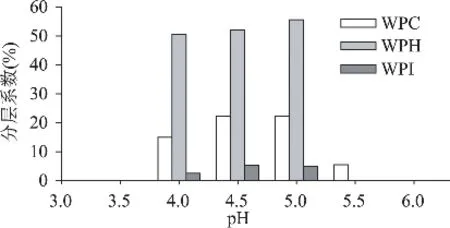
图4 pH对乳状液分层系数的影响
乳状液稳定性变化过程中,分层和粒径增大往往都是脱稳的表现,分层虽然使乳状液的均匀性受到破坏,但是乳状液并没有真正被破坏;粒径增大根据其表现会有不同的区分,絮凝通常表现为粒子的相互靠近,这个变化通常是可逆的,可以通过搅动重新分散;而聚合往往表现为粒子的相互融合导致不可逆的粒径增大,这些变化往往是由于不同的机理产生的。本文中乳状液经pH处理后,在等电点附近发生的聚合是乳状液真正的破坏。
WPC稳定的乳状液受pH处理后平均粒径变化幅度小,这可能也与其蛋白质含量低有关,乳化剂中存在的其它成分减小乳状液液滴对pH变化的敏感性,使粒径受pH影响小。
2.4 盐对乳状液稳定性的影响
图5为K+添加对乳状液稳定性影响的研究结果,加入K+对乳清蛋白乳状液稳定性没有明显的影响,乳状液的粒子粒径、分布均无明显变化(图未示),乳状液也仍保持较好的分层稳定性。
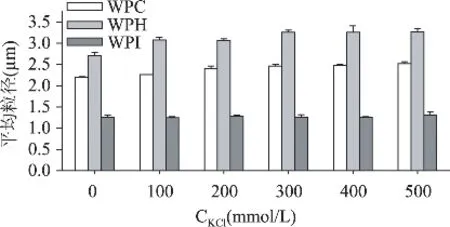
图5 KCl浓度对乳状液粒子平均粒径的影响
图6和图7为添加Ca2+对乳状液稳定性影响的研究结果。当CCaCl2≥15mmol/L时,各乳清蛋白稳定的乳状液均发生脱稳现象;具体表现在:WPI稳定的乳状液粒子平均粒径显著增加,发生明显的絮凝或聚合现象,而WPC和WPH稳定的乳状液粒径虽然没有明显增大,但是却发生了明显的分层现象。
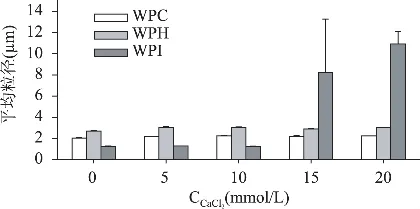
图6 CaCl2浓度对乳状液粒子平均粒径的影响
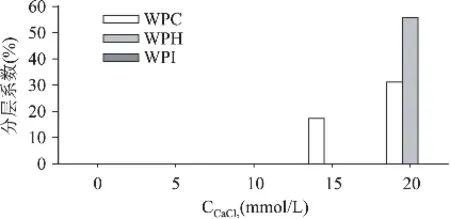
图7 CaCl2浓度对乳状液分层系数的影响
以前的研究已经表明,增加离子浓度可以提高乳状液中水相的离子强度,增加离子强度可以在乳状液中产生静电屏蔽,这些都降低粒子间的静电排斥力,诱发粒子絮凝或者聚合[12]。本文制备的乳状液为蛋白质稳定的乳状液,带电荷多的二价Ca2+与一价K+相比,是乳状液更有效的失稳剂。
3 结论
乳状液的稳定性对于产品的外观、货架期和质构都有很大影响,高品质产品的生产取决于对影响乳状液稳定性因素的理解。本文主要研究了几种乳清蛋白稳定乳状液的制备特性以及温度、pH和离子强度变化对几种乳清蛋白稳定乳状液稳定性的影响。研究结果表明高蛋白含量的乳清蛋白(WPI)制得的乳状液粒径虽然最小,但是稳定性较差;外界环境因素变化可以诱发不同机理的乳状液脱稳,WPC稳定的乳状液粒径增大较小,但是体系容易出现分层现象;相反,WPI稳定的乳状液不容易分层,但是粒径分布对环境变化最为敏感。比较结果显示WPC稳定的乳状液具有最好的稳定性。
[1]Chu B S,Ichikawa S,Kanafusa S.Stability of proteinstabilized β-carotene nanodispersions against heating,salts and pH[J].Journal of the Science of Food and Agriculture,2008,88:1764-1769.
[2]蔡志宁,赵谋明.蛋白质乳浊液体系稳定性研究进展[J].食品与发酵工业,2005,31(2):73-77.
[3]Ye A,Singh H.Interfacial composition and stability of sodium caseinate emulsions as influenced by calcium ions[J].Food Hydrocolloids,2001,15:195-207.
[4]Sun C,Gunasekaran S.Effects of protein concentration and oil -phase volume fraction on the stability and rheology of menhaden oil-in-water emulsions stabilized by whey protein isolate with xanthan gum[J].Food Hydrocolloids,2009,23:165-174.
[5]Agboola S O,Singh H,Munro P,et al.Destabilization of oil-in -water emulsions formed using highly hydrolysed whey proteins[J].Journal of Agricultural and Food Chemistry,1998,46:84-90.
[6]Dalgleish D G.Food emulsions,in emulsions and Emulsion stability[M].New York,1996:287-325.
[7]Kim H J,Decker E A,McClements D J.Role of postadsorption conformation changes of β-lactoglobulin during heating at neutral pH[J].Langmuir,2002,18:7577-7583.
[8]Saito H,Kawagishi A,Tanaka M,et al.Coalescence of lipid emulsions in floating and freeze-thawing processes:Examination of the coalescence transition state theory[J].Journal of Colloid and Interface Science,1999,219:129-134.
[9]Harada T,Yokomizo K.Demulsification of oil-in-water emulsion under freezing conditions:Effect of crystal structure modifier[J].Journal of the American Oil Chemists’Society,2000,77(8):859-863.
[10]张世春,曾晓燕,张铁涛,等.pH和NaCl对乳清蛋白油水乳浊液物理性质的影响[J].食品研究与开发,2004,25(1):134-136.
[11]Kulmyraev A A,Chanamai R,McClements D J.Influence of pH and CaCl2on the stability of dilute whey protein stabilized emulsions[J].Food Research International,2000,33:15-20.
Influence of temperature,pH and salts on the stability of emulsions stabilized by whey protein
CUI Jian,LI Jin-long,WANG Pan,MEI Xue-ying,YIN Li-jun*
(College of Food Science and Nutritional Engineering,China Agricultural University,Beijing 100083,China)
Whey protein has certain emulsifying ability in the food industry,often used as emulsifiers.Whey protein concentrate(WPC),whey protein hydrolysate(WPH)and whey protein isolate(WPl)were as emulsifier to prepare O/W emulsion by high pressure homogenization.With average particle size and layered coefficient as stability index,effects of temperature,pH and salt on emulsion stability were studied.pH was the most significant factor.Appreciable droplet flocculation occurred near the isoelectric point of whey protein(pH4~6).Near the isoelectric point of pH4~6,particles in emulsion occurred flocculation or aggregation to become unstable.WPC had the best stability of the emulsion.These results provided an important basis for the whey protein as an emulsifier for the food industry.
emulsion;whey protein;stability;pH;mean particle size
TS201.2+1
A
1002-0306(2010)11-0084-04
2009-11-18 *通讯联系人
崔健(1987-),女,在读硕士研究生,研究方向:食品材料的微细化加工及相关评价技术。
国家自然科学基金项目(20776151)。
