氟化剂的研究进展
2010-11-07西安建筑科技大学理学院应用化学专业710055
杨 燕 西安建筑科技大学理学院应用化学专业 710055
刘骞峰 西安瑞联近代电子材料有限责任公司 710077
氟化剂的研究进展
杨 燕 西安建筑科技大学理学院应用化学专业 710055
刘骞峰 西安瑞联近代电子材料有限责任公司 710077
介绍了氟化剂分类及其应用,其中最重要介绍亲电氟化剂。
氟化;氟化剂;应用;亲电氟化剂;手性氟化剂
氟原子的引入导致有机及无机化合物具有独特的物理、化学性能及生理活性。从20世纪30年代初期氟利昂问世以来,氟化学一直表现出蓬勃发展的趋势。向医药、农药等的各种物理活性物质或以色素、液晶为主的有机功能性化合物中特定位置上引入氟原子,可以使其效果由戏剧性的增强或化合物自身的性能大有改变。许多尖端技术(原子能工业、火箭、宇航等),和一些重大的工业项目及药物都采用了含氟的化合物。在液晶材料中,用于TFT-LCD的高档液晶必须是对热化学、光、电稳定性好,电荷保持中间、粘度低、电阻率大(ρ≥1.0×103Ωm)的高性能TN材料,以往,含氰基和酯类化合物无法满足这些要求,只有含氟液晶材料才能适用于TFT-LCD,近十年来几乎所有向列相材料的开发都是含氟液晶化合物。目前,对新型氟化剂的研究已成为合成含氟化合物最重要的分支。
用于含氟化合物合成的氟化剂大致可分为以F-形式进行氟化的亲核型氟化剂和以F+的形式进行氟化的亲电型氟化剂两种。
1 亲核型氟化剂
采用F-离子进行亲核取代的研究始于1863年,从那时起已相继提出多种氟化剂。如最初使用F2作为亲电试剂可成功地实现氟原子的引入。SF4在氟化学的发展史上是很重要的一种氟代剂,最重要的应用就是从羧酸合成三氟甲基化合物。但是上述经典的亲核氟化试剂存在着高毒性、反应不易控制和不易操作等缺点。随着二烷胺基氟化硫化合物等新型亲核氟化剂的发展,它们在氟化学中的应用逐渐减少。
二烷胺基三氟化硫化合物最早由Demitras小组在1964年首次合成[1]。20世纪70年代,Markovskii和Middleton制备了一系列二烷胺基三氟化硫并较详细地研究了它在制备有机氟化合物上的应用:二乙胺基三氟化硫(DAST)、二甲氧基乙基胺基三氟化硫(BAST)、4-吗啉三氟化硫(1a)、吡咯烷酮三氟化硫(1b)、氮杂环己烷三氟化硫(1c)。作为氟化剂,此类化合物除具有反应速度快,条件温和、收率较高、反应选择性好等优点外,同时具有对温度的适应范围较大,操作方便,消除反应和重排反应较少等优点。二烷胺基氟化硫易与羟基、羰基等官能团反应而实现氟的取代,已经广泛应用于含氟有机天然物的合成,如制备含氟糖类、含氟甾体、含氟氨基酸和含氟抗生素等。
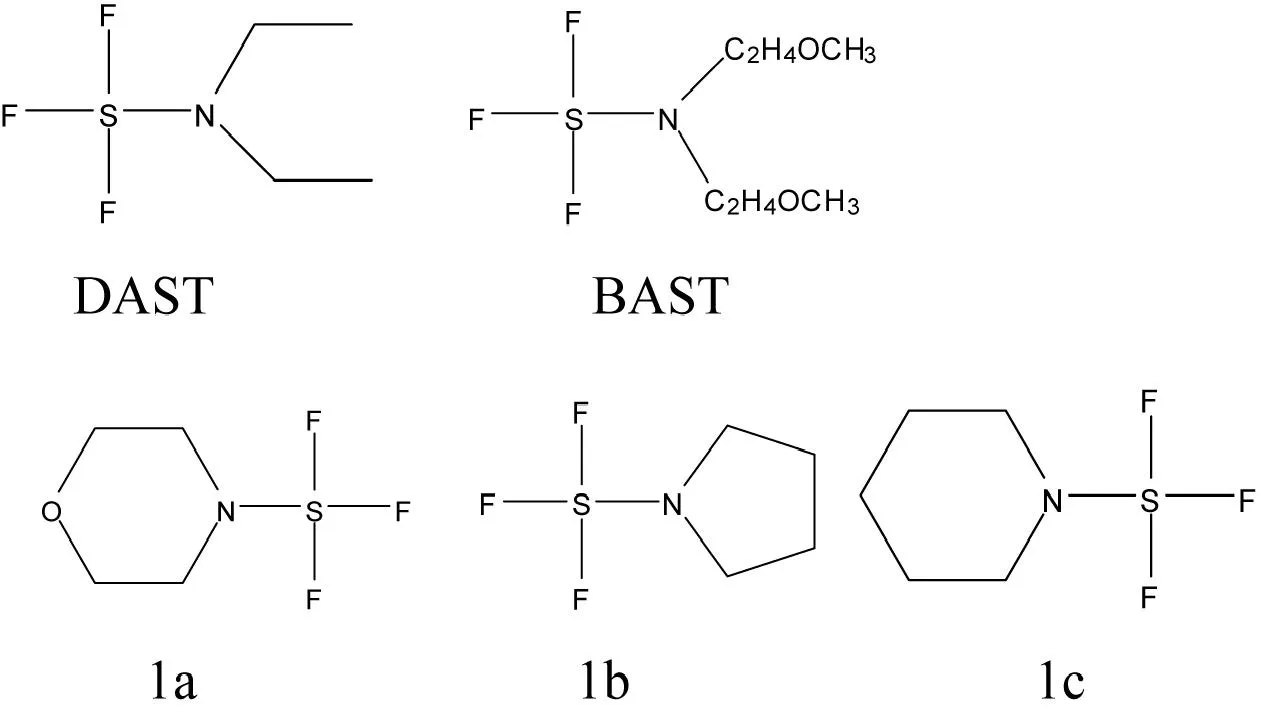
这类化合物在一定温度下会发生爆炸,早期对二烷胺基三氟化硫化合物机理研究主要以DAST作为研究对象,1979年报道关于DAST在其制备和使用过程中发生爆炸[2]。DAST是最早实现商业化,其它胺基硫氟试剂和DAST大多相似。DAST是液体,在干燥情况下室温或冰箱能长期保存,DAST在分解温度90℃,爆炸温度147℃,处理不当会有爆炸的危险。由于BAST比DSAT稳定,易于操作,常用BAST替代DAST。此试剂能将羟基化合物转化为单氟代化合物,醛和酮转化为二氟代化合物,而对羧酸及其衍生物的羰基则没有影响。
2 亲电氟化剂
自1968年Barton小组报道了第一例新的亲电氟化试剂CF3OF后,化学家们陆续合成了一些亲电氟化试剂,如FClO3、xeF2151、XeF2、FNO、CF3OF、NF氰化试剂。
亲电氟化反应研究进展较快,主要原因之一是发现了大量氮-氟亲电氟化剂。从1995年以来出现的亲电氟化剂绝大部分都具有氮-氟键。氮-氟化合物用于亲电氟化剂最早于20世纪60年代由Banks等提出,该氟化剂由于种类繁多、操作方便、反应选择性好等优点得到了广泛的应用。
2.1 N-氟代吡啶盐
Umemoto等在1990年报道了使用氮-氟吡啶-2-磺酸酯作为亲电氟化剂,缺点是在有机溶剂中稳定性较差而影响其氟化能力。近年来通过改变吡啶环上的取代基,合成了一系列化合物[3],开发了N’-氟代吡啶盐,结构通式为:
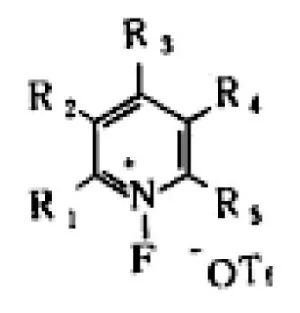
其中,Tf=CF3SO2,也可以用BF4、PF6、SbF6代替OTf。
该氟化剂的一大优点是稳定的晶体,氟化能力是可变的,通过改变吡啶环上R1~R5,可根据需要设计具有不同氟化能力的氟化剂,主要用于负碳离子、各种烯醇化合物、多电子芳香族化合物、从硫化物出发向α-氟代硫化物的转化、烯烃化合物的氟代乙酰氧基化反应等的氟化,涉及领域很广。该系列氟化剂具有反应条件温和、选择性可变、使用方便、易于工业化等优点,尤其适用于含有多个复杂官能团的化合物的氟化。
2.2 氮-氟三乙胺(F-TEDA)和奎宁盐
Umemoto等用三乙胺作原料,制得相应的N,N’-二氟-1,4-二氮二环[2,2, 2]辛烷盐。
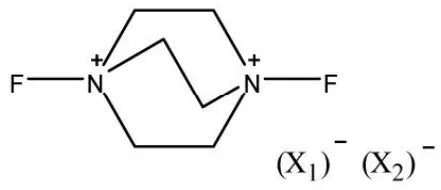
a.X1=X2=OSO2CF3
b.X1=X2=HSO4
c.X1=HSO4,X2=F(HF)2
d.X1=X2=BF4
e.X1=X2=SbF6
f.X1=X2=PF6
该类化合物对β-二羰基化合物、取代的苯乙烯、甾类化合物和活性芳香族化合物进行较好的氟化,且收率较高。
2.3 N-烷基-N’-氟1,4-二氮二环[2,2,2]辛烷
用于取代有剧毒和爆炸危险性氟化药剂如HF、FClO3和CF3OF的新型氟化剂。这种氟化剂乘坐Selectfluor,又称为F-TEDA-BF4,化学名称为1-氯甲基-4-氟-1,4-重氮化[2,2,2]二环辛烷双(四氟硼酸盐)[4]。这种氟化剂首先由英国曼彻斯特科技大学的R.E.Banks合成,空气产品与化学品公司对它作了进一步的开发。这种固化剂在温和条件下能有效地高选择性地进行迅速氟化,不需要特殊设备和操作技术这种氟化剂溶于多种溶剂,与普通反应器材料相容,并且能分解成可加以处理的废物。主要用途可对富电子双键、烯醇硅醚、烯醇锂盐等进行单氟化反应,用于制备含氟甾体药物等。
目前通过研究合成N-烷基-N’-氟1,4-二氮二环[2,2,2]辛烷一系列氟化剂,其通式如下:
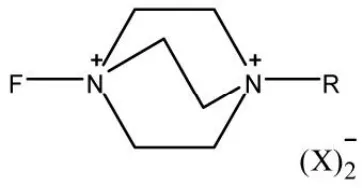
R=CH3,CH2Cl,C2H5, CH2CF3, C8H17; X=BF4, PF6, OTf, FSO3
此类氟化剂可以用来氟化烯胺、二羰基化合物、富电子的芳香族化合物,而且收率较高。
2.4 手性氮氟亲电氟化剂
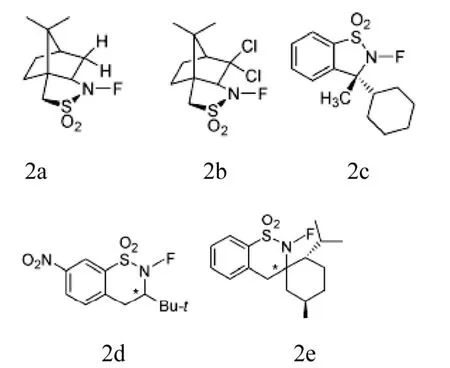
1999年以前,已有数种手性亲电氟化试剂,它们被称为第一代手性氮氟亲电氟化剂,如2a~2e所示化合物。第一代手性氟化试剂对不同底物的对映选择性表现出较大的差异, 化学反应性也有待于提高。
Shibata 和Cahard 等报道了新型的将奎宁生物碱衍生物转化为手性N-F奎宁生物碱季铵盐(F-CA-BF4)作为对映选择性亲电氟化剂,它们作为手性氟化试剂与底物发生对映选择性亲电氟化反应[5]。
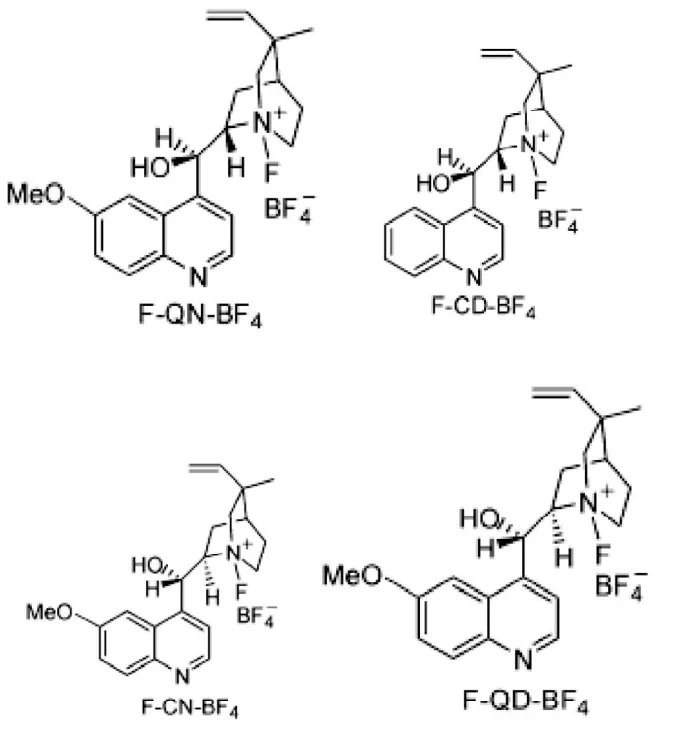
这些N-F 奎宁生物碱季铵盐的化学反应性非常好, 但对映体选择率不高, 其中试剂F-CD-BF4 的活性最高。以FCD-BF4 对其它底物进行了研究,同样,虽然几乎可以定量地得到相应的氟化产物,但对映体过剩率很不理想, 均在50%以下[6]。
[1]Demitras, G.. C.; Kent, R. A.; MacDiarmid, A. G. Chem. Ind.(London) 1964, 1712.
[2]J. Org. Chem. 1999,64,7048-7054
[3]杨柳,毛淑芬,谭兆海.亲电氟化剂研究进展[J]. 有机氟工业.2003;(3):43-46 [4]黄汉生等.化学合成中绿色技术的研究开发[J].化工科技动态.1995(7):12
[5]杨柳,毛淑芬,谭兆海.亲电氟化剂研究进展[J]. 化学试剂.2004;26(3):211-213
[6]Cahard, D.; Audouard, C.; Plaquevent, J. C.; Roques, N.,Org. Lett. 2000, 2, 3699.
10.3969/j.issn.1001-8972.2010.21.068
