过饱和五硼酸钠溶液结构
2010-11-06周永全房春晖
周永全 房春晖 房 艳
(1中国科学院盐湖资源与化学重点实验室,中国科学院青海盐湖研究所,西宁 810008;2中国科学院研究生院,北京 100049)
过饱和五硼酸钠溶液结构
周永全1,2房春晖1,*房 艳1,*
(1中国科学院盐湖资源与化学重点实验室,中国科学院青海盐湖研究所,西宁 810008;2中国科学院研究生院,北京 100049)
用快速X射线衍射法测量了298和323 K时过饱和五硼酸钠溶液的时间空间平均结构,得到了溶液径向分布函数.通过模型设计及理论计算获得了B-B、B-O、O-O、Na-O、Na-B原子对相互作用的理论偏径向分布函数,并讨论了浓度和温度对五硼酸钠溶液结构的影响.在五硼酸钠过饱和溶液中六水合Na+形成八面体结构,其平均配位数随浓度和温度变化不大,作用距离随温度升高及浓度减小而减小;给出了溶液中主要硼酸盐离子B3O3(OH)-4、B5O6(OH)-4和B(OH)3的水合结构,较高温度及较高浓度有利于更高聚合的多聚硼酸根离子的形成;浓度对硼酸盐离子的第一水合层的水合数影响较大,在较浓的五硼酸钠过饱和溶液中,五硼酸根离子的一个端氧单齿配位到Na+上形成离子对,Na-B特征距离为0.328 nm.
溶液结构;X射线衍射;五硼酸钠;过饱和溶液;径向分布函数;多聚硼酸根离子
研究硼酸盐溶液水合结构,不仅对阐述水合硼酸盐晶体的形成条件及其转化规律,制定和选择最优提取工艺具有实际意义[1],而且对阐述盐湖中硼酸盐的迁移和浓缩规律及其成矿机理等问题具有理论意义[2],还对于从微观尺度上解释硼酸盐在生物体内代谢机理[3]具有重要指导意义.硼酸盐在水溶液中的存在形式极其复杂,受到温度、总硼浓度、外加阳离子及pH影响[4].目前确定水溶液中硼酸盐阴离子的物种形态的研究方法主要有电导、电势滴定法[5-7]、傅里叶变换红外(FT-IR)光谱法[8-9]、Raman光谱法[10-11]、核磁共振(NMR)[12-13]及质谱(MS)[14]等.X射线衍射是一种既能直接测量溶液物种结构,也能直接获得物种水合结构的有效方法[15-16],但由于硼散射能力很弱,硼酸盐溶解度又很小,目前还未见报道.本文用衍射法测量了不同浓度过饱和五硼酸钠溶液在298和323 K的水合结构,通过对衍射数据的处理,获得了溶液体系的径向分布函数,通过模型设计和定量计算获得了溶液结构的定量研究结果.
1 实验部分
1.1 样品制备及性质测定
分析纯硼砂和硼酸经进一步提纯,按照Na2OB2O3-H2O相图[17]计算并合成五硼酸钠,经X′Pert Pro X射线衍射仪进行物相鉴定,确定为NaB5O8·5H2O.蒸馏水用SYZ-550型石英亚沸高纯水蒸馏器进一步蒸馏.在恒温水浴(±0.01℃)中,用密度瓶法测量五硼酸钠溶液密度,用Orion 310P-01 pH计测定溶液酸碱度.溶液组成用甘露醇法[18]测定.相对过饱和度可定义为:
σ=(w-w0)/w0(1)式中w为溶液质量百分浓度,w0是相同温度下对应固相的溶解度,取自文献[17].溶液线吸收因子(μ)由原子质量吸收因子[19]计算.化学计量体积(nm3)按V= 104/(6.02217c)计算.表1列出溶液浓度c、pH值、密度d、线吸收因子μ、化学计量体积V、水盐摩尔比R和被测样品温度T.
1.2 X射线衍射
液体样品的衍射实验在X′Pert Pro θ-θ型X射线衍射仪上完成.用超级恒温水浴接内腔式液体样品池,温度控制在±0.5℃以内.选择Mo Kα辐射源,波长为0.07107 nm.管电流为45 mA,管电压为50 kV.由于青海地区气候干燥,为防止样品蒸发引起组成改变,在样品表面覆盖一层厚度为6 μm Mylar膜(美国杜邦公司).测定2θ范围为3°-150°,对应散射矢量(s=4πsinθ/λ)范围为4.63-170.8 nm-1.分四段进行交叠测量,低中角区选用较小发散狭缝和较小步长,高角区选用较大发散狭缝和较大步长.累积计数范围为(2-8)×104,统计计数误差在1%以内.最小固定时间200 s,最大固定时间为3000 s.交叠测量区2θ一般为2°-5°.详尽实验细节参见文献[20-21].
2 衍射数据处理
首先进行Mylar膜窗口强度扣除,接着进行吸收校正、数据平滑、极化校正及多重散射校正,再将不同发散狭缝测量的衍射强度换算到相同条件下的强度数据.用积分法和高角法联用计算标度因子,并将衍射强度标度到电子单位.定义结构函数iobsd(s)为电子单位实验散射强度与计算的样品自身散射强度之差
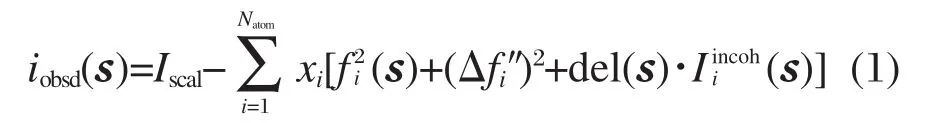
式中,Iscal为标度到电子单位的观察强度;Iiincoh(s)是原子i的不相干散射;xi是含有一个Na原子计量体积内第i种原子数目;fi(s)表示原子i异常散射实部校正的散射因子,△fi″为原子i异常散射虚部校正项[18];del(s)是到达计数器的不相干散射分数,本工作del(s)一律取值为1.0.采用Fourier变换,将s加权结构函数变换为差值径向分布函数D(r)-4πr2ρ0.
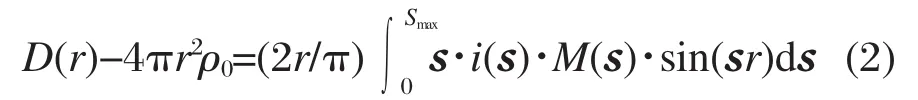
这里r是离散距离.ρ0为样品散射角零度时平均电子散射能力(e2·nm-3),即样品平均电子密度.fi(0)为第i种原子s=0时的原子散射因子.M(s)为修饰函数:
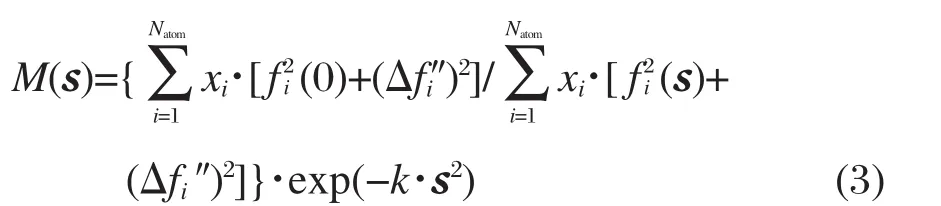
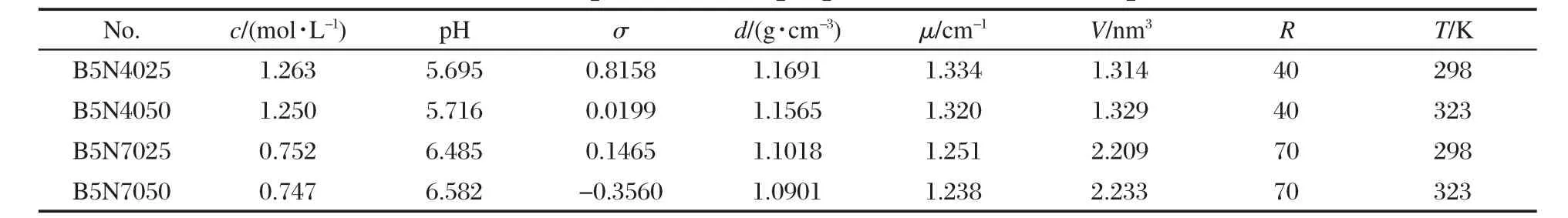
表1 样品溶液组成和性质Table 1 Compositions and properties of solution samples
式(3)中前一部分称为锐化因子,后一项中阻尼因子k可任意选择,以减少强度曲线对最外部分实验误差和积分截断误差的影响,同时抑制第一项引起的锐化作用.峰形计算和再次进行傅里叶变换,以除去乱真峰.
理论结构函数icalcd(s)由表征溶液结构的三个重要参数:原子对平均距离(rij)、相互作用数目(nij)和德拜温度因子(bij)计算得到.
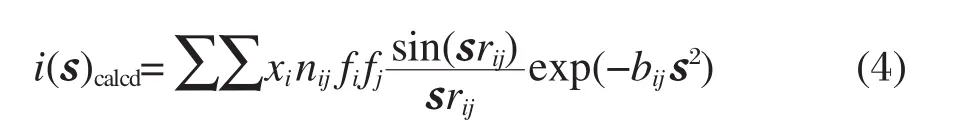
Mylar膜扣除、吸收校正、平滑及极化校正等在Origin8.0中完成,其余用液体X射线衍射数据处理FORTRAN程序包KURVLR计算[22-23].
3 结果与讨论
3.1 结构函数和差值径向分布函数
如图1所示,实验s加权结构函数(粗实线)在0轴上下震荡,表明实验和数据处理是可靠的.结构函数i(s)不包含与液体结构无关的散射部分,能透露一些溶液中的短程有序结构信息.从结构函数可以看出其第一个峰为一分叉的双峰,该峰是溶液中形成网状氢键的典型特征.常温常压下,上述两峰同时存在,而高压下只有第二个峰出现[24],表明高浓度硼酸盐对溶剂水四面体结构的破坏,相当于施加了高压[25].
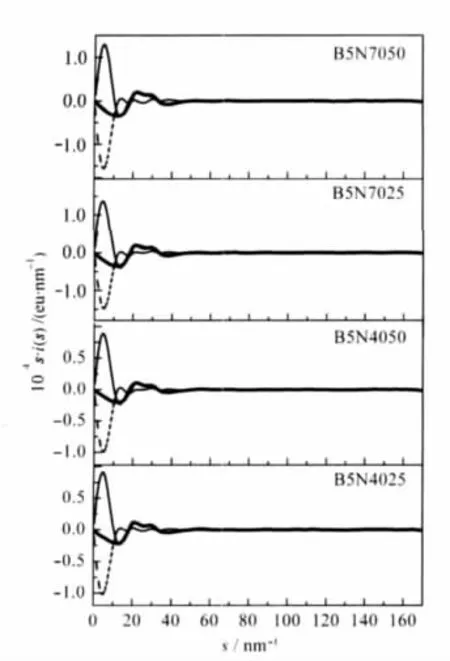
图1 样品实验结构函数(粗实线)、模型结构函数(细实线)及其差值曲线(虚线)比较Fig.1 Comparison among experimental(thick solid line),model calculated(thin solid line)structural functions and their differences(dash line)for samples
由图2可以看出,实验差值径向分布函数(DRDF)在r<0.1 nm内不存在乱真峰,0.5 nm以后震荡峰越来越小,表明在整个实验过程中统计计数和系统误差都降低到最小程度.DRDF曲线在0.6 nm之前出现11个峰.第一个小峰位于0.095 nm,为溶液中水分子内O-H峰;0.140 nm左右的峰为三角形硼氧(B△-O,0.1365 nm)和四面体硼氧(B□-O,0.1471 nm)距离的叠加峰[26],这比NaB5O6(OH)4[27]、NaB5O6(OH)4·3H2O[28]晶体中B△及B□中B-O距离加权平均值0.141 nm稍小,暗示溶液中B△所占比例大于4/5.0.18 nm处的小峰可能是氢键中氧原子与另一水分子上氢原子O-H相互作用和B△与氢氧根上氢原子相互作用B-H的叠加峰;位于0.23 nm峰可指认为Na-O(I)作用,该距离也在文献报道六配位钠离子Na-O(I)距离范围内[15];0.245 nm峰为B△和B□中O-O相互作用和五硼酸根六元环内B-B相互作用的叠加,这比NaB5O6(OH)4[27]、NaB5O6(OH)4· 3H2O[28]晶体中O-O距离加权平均值0.244 nm略大,与晶体中六元环内B-B距离0.246 nm相近; 0.29 nm峰为硼酸根六元环上端氧及环氧水合距离和溶液中相邻两个水分子中O-O距离的叠加峰[29]; 0.3-0.6 nm之间5个DRDF峰(0.32,0.37,0.39,0.44和0.47 nm)为溶液中离子内或离子与水分子之间多种相互作用的叠加,定性描述十分困难.
3.2 最佳几何模型设计
通过模型优化计算,从8种几何模型中筛选出最佳几何模型,如图3所示.分子间或者离子间相互作用,分别考虑为Na+水合,B(OH)3,B3O3(OH)4-和B5O6(OH)4-水合以及Na+与B3O3(OH)4-和B5O6(OH)4-缔合.对B(OH)3,B3O3(OH)4-和B5O6(OH)4-水合,仅考虑三角形平面上的赤道水合,假设每个OH-上有3个水分子参与水合,形成一个水合层.而六元环上环氧和端氧位置发生水合,满足O原子变形四面体稳定结构,也能形成一个水合层.其中一个端氧形成接触离子对NaB3O3(OH)4和NaB5O6(OH)4.由于硼原子散射能力非常低,三角形轴向水合的配位数(2)很低,模型设计未进一步考虑轴向水合.

图2 实验(虚线)、理论(粗实线)D(r)-4πr2ρ0及其理论偏径向分布函数(细实线)比较Fig.2 Comparisons among experimental(thin solid line),model calculated(dash line)D(r)-4πr2ρ0and calculated partial radial distribution functions(think solid line)
分子内或离子内的相互作用,虽然浓度相对较低,但有序程度很高,可以用变形二联六元环模型描述.三聚硼酸根离子B3O3(OH)4-由两个B△和一个B□构成六元环;而五硼酸根离子B5O6(OH)4-,可看成是由两个三聚硼酸根离子通过公共顶点(B□)构成,两个六元环平面互相垂直.假设三个物种中的B△和B□中B-O距离与晶体中一致,即r△=0.139 nm和r□=0.148 nm.在物种未知的情况下,由总硼浓度可以求出两者的平均距离和平均配位数.三角形B△和四面体B□中O-O距离,其中包括B3O3(OH)-4和B5O6(OH)4-中六元环meta-O-O距离,由总硼浓度计算O2-O3平均距离和配位数.输入距离初值选择在B△中OO距离为(3)1/2×r△=0.236 nm和B□中O-O距离为(8/3)1/2× r□=0.240 nm之间,相互作用数在3和6之间.B3O3(OH)4-和B5O6(OH)4-中六元环内meta-B1-B7距离计算,考虑B□变形,假定∠B1-O-B7=125°,可按照余弦定理(r△2+ r□2-2×r□×cos125°)1/2=0.254 nm,而meta-B1-B4距离为(3)1/2×r△=0.236 nm,配位数为6.环内para-B-O包含B1-O6和B7-O3距离,前者由勾股定理估算(3r△2+ r△2)1/2=0.273 n m,后者由余弦定理计算为0.293 nm,配位数分别4和2.B1与另一六元环上O8距离为(r△× (3)1/2/2)2+(0.293-r△/2+r□×cos55°)2+(r□×sin55°)2]1/2= 0.357 nm,配位数为8;B4与另一B1原子上端氧O2距离rO2-B4=[r△2+((3)1/2×r△)2-2×r△(3)1/2×r△×cos150°]1/2=0.368 nm,配位数为4;对位环氧O3与另一六元环环氧 O8之间距离 rO3-O8=[0.2932+r2□-2×0.293×r□× cos125°]1/2=0.397 nm,配位数为4;环氧O6与对位B原子上端氧O2之间距离rO2-O6=3×r△=0.417 nm,配位数为4;端氧O2与另一环上最近环氧O8之间距离rO2-O8=[(r△×(3)1/2)2+(0.293+r□×cos55°)2+(r□×sin55°)2]1/2=0.442 nm,配位数为8;B1-B9之间距离rB1-B9=[(r△(3)1/2/2)2+(0.293×2-r△)2+(r△×sin60°)2]1/2=0.479 nm,配位数为8;同一六元环上端氧-端氧O2-O5之间距离rO2-O5=2×(3)1/2×r△=0.484 nm,配位数为2.
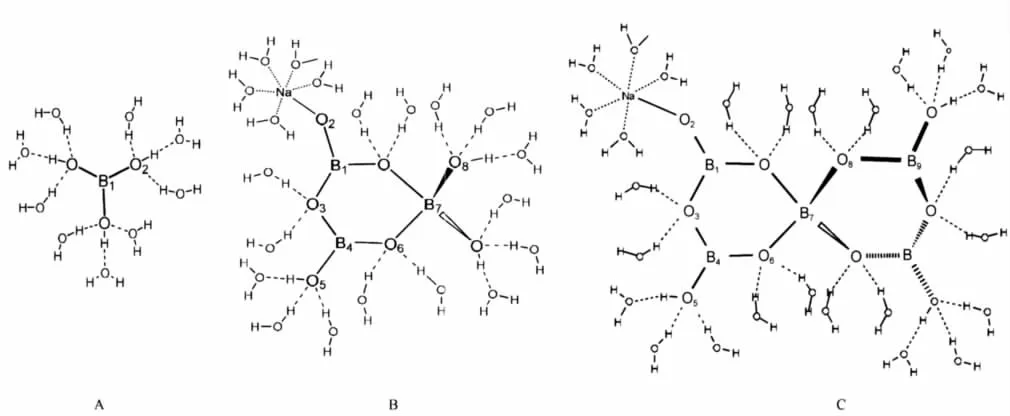
图3 几何模型示意图Fig.3 Schematic diagram of geometric model
3.3 结构参数的定量计算
将上述模型设计得到的原子相互作用结构参数(c,rij,nij,bij)输入KURVLR程序,构造理论DRDF,通过反复改变rij,nij,bij,使模型计算的加权结构函数和实验加权结构函数几乎重合,其差值曲线在0.0 e·nm-1上下震荡(图1),在10 nm-1左右理论和实验结构函数线之间存在一些差异,这主要是因为未考虑长程相互作用[24].模型计算和实验DRDF形状和相对强度一致,每个峰都有很好的对应关系(图2),表明模型计算结构参数与实验值吻合得很好,差值径向分布函数的定量结果如下表(表2).
由文献[5,30-31]给出的化学平衡常数和五硼酸钠溶液的pH值,计算得到了五硼酸钠溶液在298.15 K下存在主要物种分布如(图4).其中在过饱和五硼酸钠溶液中最主要的物种为B5O6(OH)4-,B3O3(OH)4-和H3BO3,298 K样品B5N4025中参与形成B5O6(OH)4-, B3O3(OH)-4和B(OH)3的硼占总硼的分数分别为0.327, 0.414和0.226;B5N7025分别为0.539,0.219和0.237. 323 K样品B5N4050分别为0.614,0.164和0.217; B5N7025分别为0.409,0.352和0.203.样品溶液中B4O5(OH)24-(<0.03),B3O3(OH)25-(<4×10-4)和B(OH)4-(<0.03)可忽略不计.由于X射线衍射法不能对环氧和端氧水合精确定位,只能给出O-O(w)相互作用的离散距离和平均配位数.
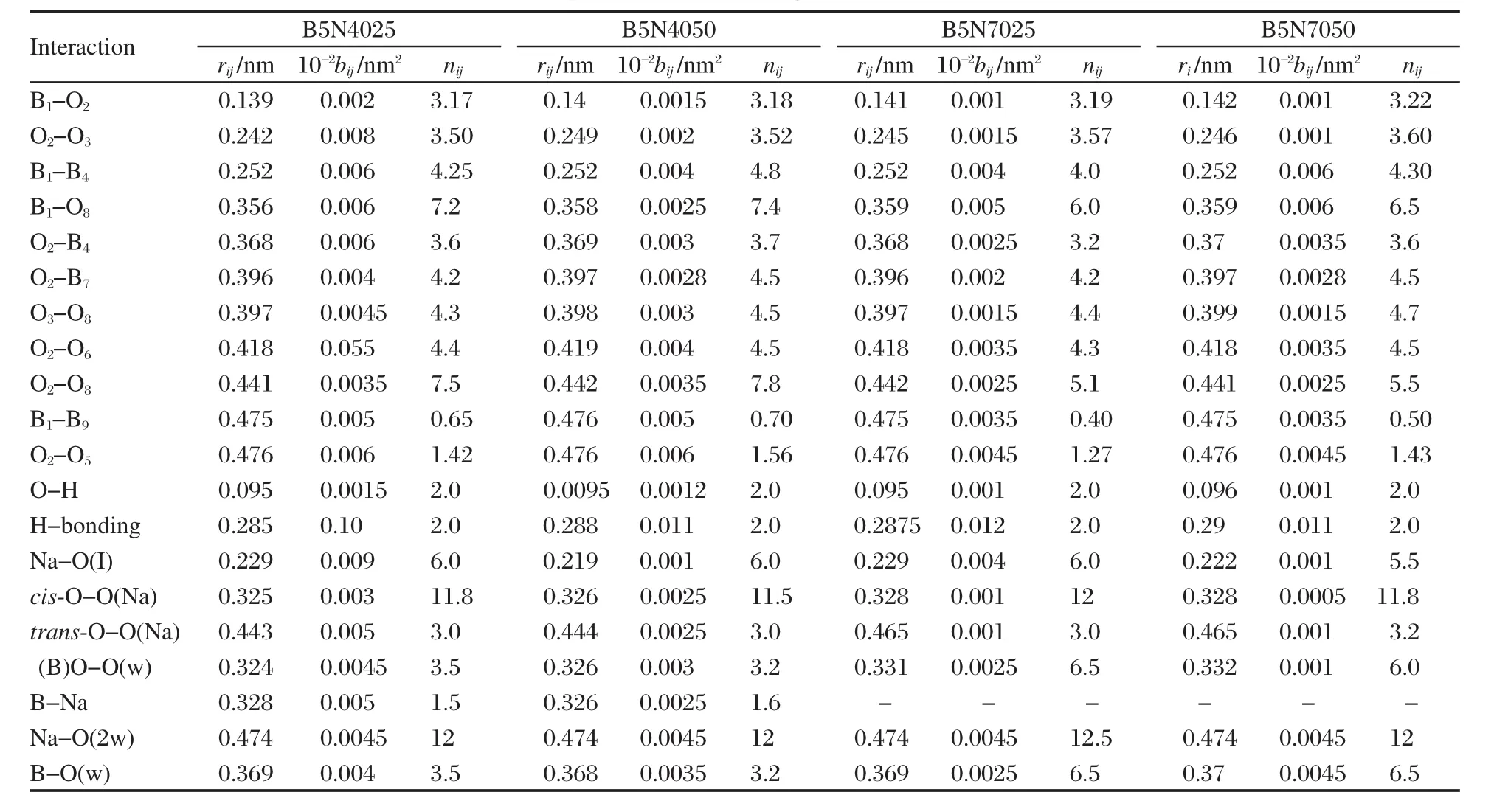
表2 模型计算的结构参数Table 2 Structure parameters from geometrical model calculation
溶液中水分子内H-O距离为0.095 nm,配位数为2.以总硼浓度计,B1-O2距离rB-O=0.139 nm,配位数为3.17,恰好处在模型估算三角形和四面体B-O距离的中间,表明该样品三角形BO3占优势,而四面体BO4相对较少;以总硼浓度计,O2-O3距离为0.242 nm,与模型设计估算值一致,其中包含六元环内meta(间位)-O-O相互作用;六元环内meta-B-B距离0.252 nm,在模型估算值的B1-B4距离0.241 nm和B1-B7距离0.253 nm之间.环内para-B-O距离0.282 nm,位于模型设计B1-O6距离0.274和B7-O3距离0.293 nm之间,其原因可能受到氢键计算的不确定性因素的影响;环B1与支链B7距离0.285 nm与模型设计一致;B到另一环O原子上B1-O8计算值0.356 nm与模型设计0.352 nm接近;B4与端氧O2距离计算值为0.368 nm,与几何模型0.368 nm一致;B7与端氧O2距离计算值为0.386 nm,比几何模型0.379 nm大;O3-O8计算值为0.397 nm,与几何计算值 0.397 nm一致;O2-O6计算值为0.418 nm与模型设计值0.417 nm一致;O2-O8计算值为0.441 nm与模型设计值0.442 nm一致;B1-B9计算值为0.475 nm,比模型设计值0.479 nm稍小;同环端氧O2-O5计算值为0.476 nm,比模型设计值0.482 nm小.模型计算结果表明溶液中确实存在B3O3(OH)4-和B5O6(OH)4-,并且离子内相互作用具有高度有序性.
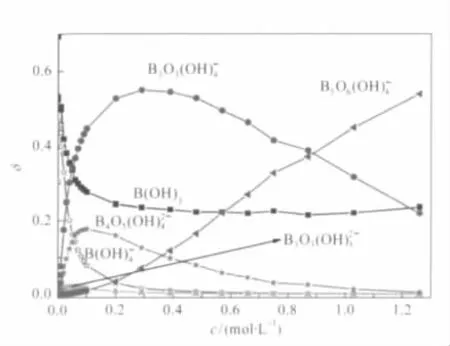
图4 298 K下五硼酸钠溶液在不同浓度下主要物种的分布Fig.4 Distribution of main polyborates in aqueous sodium pentaborate solution at 298 K
离子与水分子之间的相互作用计算,主要考虑O上的水合满足其四面体稳定结构.垂直于三角形平面的轴向水合,B-w距离大约在0.32 nm,由于B原子散射能力极低和轴向水合数也很低(2),精确计算该距离是困难的.三角形平面上的赤道水合与六元环上环氧和端氧水合,以总硼浓度计,水合距离为0.369 nm,比晶体B-OH2距离很接近.平均配位数在3.2到6.5之间,表明随着溶液浓度的升高,由于硼酸根的聚合,B3O3(OH)-4和硼酸根浓度逐渐降低, B5O6(OH)-4浓度急剧升高,以及阴离子与阳离子的缔合作用,平均水合数降低.
五硼酸根离子与钠离子的缔合,只存在端氧位置的单齿水合.从表2可找出B3O3(OH)-4和B5O6(OH)4-离子内O-O 相互作用共有五种,即O2-O3距离为0.242,O3-O8距离为0.397,O2-O6距离为0.418,O2-O8距离为0.441,O2-O5距离为0.476 nm.其中任何3个O原子之间平面边长都不能满足同时配位到钠离子的条件,即不可能与八面体上边长为0.325 nm等边三角形平面,或四面体上边长为0.356 nm等边三角形平面嵌套在一起.因此可以排除钠离子与三硼酸根和五硼酸根三齿螯合的情况.同样在B3O3(OH)-4和B5O6(OH)-4离子中没有任何一组O-O直线距离,与八面体棱长0.325 nm或四面体棱长0.356 nm嵌套在一起,因此二齿螯合也不可能发生.因而唯独存在单齿水合一种情况.单齿水合的位置,也有3种可能性,即BO3和BO4之间的环氧配位到钠离子,BO3和BO3之间的环氧配位到钠离子,端氧配位到钠离子.单齿配位要满足3个条件,首先是满足配位O原子的四面体稳定结构,第二是满足水合钠离子八面体或四面体稳定结构,第三是配体上其它位置上的羟基与受体水合离子顶点的距离不能小于0.28 nm.因此两种环氧缔合也能完全排除,唯一满足三个条件的只有端氧缔合.由于总硼越高,B3O3(OH)4-浓度变低,B5O6(OH)4-浓度变高,因此B5O6(OH)4-缔合可能性最大.端氧缔合的特征距离Na-B被确定在0.328 nm,与五水五硼酸钠晶体一致.
将计算得到的溶液结构参数,分别按B-B、BO、O-O、Na-O、Na-B原子对相互作用计算得到的偏径向分布函数(图2),计算的偏径向分布函数与DRDF相比,能更有效排除重叠峰的影响,更容易确定各作用对的作用距离及其对衍射强度的贡献.与简单无机盐溶液结构[16,22,32-33]对比,水与五硼酸根离子中水合,能够引起多聚离子的解聚,以及解聚伴随的水分子电离,这就是硼酸盐溶液物种与pH值关系密切的根本原因.
3.4 温度及浓度对五硼酸钠溶液结构的影响
从表2可以看出,温度增加时,50℃下多聚硼酸盐离子分子内B1-B3、B1-O8、O2-B4、O2-B7、O3-O8、O2-O6、O2-O8、B1-B9、O2-O5等距离基本不变,而相互作用数均有一定程度的增加,表明随着温度增加,高聚硼酸盐离子B5O6(OH)-4浓度增加.随着温度升高,B△和B□中的O2-O3平均距离增大,而钠离子第一配位层Na-O(I)作用距离有所变小而水合数变化不大.298 K时Na-O(I)与O2-O3作用峰重合,而323 K这个峰重叠峰分裂为0.22 nm及0.242 nm两个小峰.
随着浓度减小,溶液中溶剂水分子数量增加, H-O及H-bonding相互作用增强,DRDF曲线上相应位置峰高增加,面积也增大;溶液中0.140 nm B△-O及B□-O,0.245 nm O-O(B△),0.230 nm Na-O(I)和0.325 nm八面体水合钠离子cis(顺式)-O-O作用峰高和峰面积等都相应减小;多聚硼酸盐离子内B1-B3、B1-O8、O2-B4、O2-B7、O3-O8、O2-O6、O2-O8、B1-B9、O2-O5等相互作用数也都减小,表明随着水加入,溶液中高聚硼酸根离子发生解聚.
在五硼酸钠浓溶液中五硼酸离子为最主要的物种,其水合结构如图3C所示,当两个水分子进攻五硼酸离子中的水合环氧时,环氧发生断裂得到水合B3O3(OH)-4和B2O(OH)4硼酸根离子,该过程(图5A)平衡常数较大反应速度较慢;上述过程得到的水合二聚硼酸盐分子(B2O(OH)4)中的水合桥氧再在一个水分子进攻下断裂得到水合硼酸分子,该过程(图5B)进行较快,因此很少有人检测到[12].这些物种之间复杂的聚合、解聚及缔合作用,尤其是离子与溶剂水的作用,达到平衡需要较长的弛豫时间,这就可解释硼酸盐溶液往往具有较高过饱和度[14].
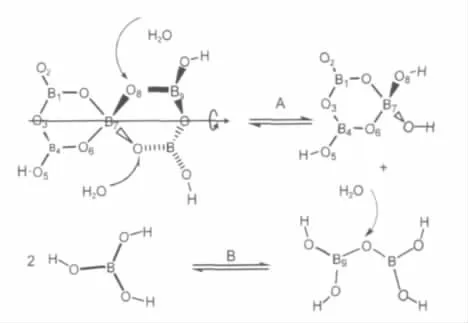
图5 溶液中水合硼酸盐离子的相互作用Fig.5 Interactions between hydration polyborates in solution samples
根据模型计算得到的相互作用数,还可估算出在过饱和五硼酸钠溶液中主要硼酸盐离子的大致比例:据B1-O2或O2-O3相互作用的作用数,设B□占总硼的分数为x□,可按4x□-3(1-x□)=nB1-O2或6x□-3(1-x□)=nO2-O3估算出硼酸盐溶液中B□分数x□,在B5N4025、B5N4050、B5N7025、B5N7050样品中x□分别为17%、18%、19%和22%;以B1-B9相互作用也可粗略给出溶液中分别有65%、70%、40%和50%的硼参与形成五硼酸根离子(xB5O6(OH)-4);还可以据xB3O3(OH)-4= 3(x□-xB5O6(OH)-4/5)估算出溶液中参与形成三硼聚硼酸根离子的硼分别为12%、16%、40%和36%;结合上述结论我们可由(1-xB5O6(OH)-4-xB3O3(OH)-4)大致得出样品中硼酸含量分别为23%、14%、20%和14%.这与我们计算出在各样品溶液中主要硼氧聚离子的分布情况(图4)基本一致.
4 结论
用衍射法测量了不同浓度和温度下过饱和五硼酸钠溶液的结构.结果表明,Na+水合结构随浓度和温度变化敏锐,但其平均配位数变化不大,温度升高其作用距离减小,浓度增大作用距离增大;给出了样品溶液中主要硼酸盐离子(B3O3(OH)4-,B5O6(OH)4-和B(OH)3)的水合结构,温度及浓度对硼酸盐离子的水合结构影响较大,高温及高浓度有利于更高聚合多聚硼酸根离子的形成,浓度对硼酸盐离子的第一水合层的水合数影响较大,在较稀的五硼酸钠溶液中硼水平均作用数为6.0,在较浓样品中该平均作用数为3.0.在浓溶液中,钠离子单齿配位到五硼酸根离子的端氧上形成离子对,其Na-B距离约为0.328 nm,且高温、高浓度有利于该离子对的形成.当浓度降低时,水分子和水合硼酸盐离子之间的相互作用使高聚硼酸盐离子解聚.致谢: 感谢中国科学院青海盐湖研究所分析测试部对实验工作提供的帮助.作者对徐光宪、张慧心、杨家振、韩万书、尉志武等教授多年来关心、支持和指导溶液结构研究,表示衷心感谢.
1 Chen,C.;Lin,Z.;Wang,Z.Appl.Phys.B,2005,80(1):1
2 Aleksandrov,S.;Troneva,M.Geochemistry International,2009, 47(9):914
3 Goldbach,H.;Huang,L.;Wimmer,M.Advances in plant and animal boron nutrition,Netherlands:Springer Press,2007:3-25
4 Gao,S.Y.;Song,P.S.;Xia,S.P.;Zheng,M.P.Salt lake chemistry——new type borate salt lake.Beijing:Science Press, 2007:179-200 [高世扬,宋彭生,夏树屏,郑绵平.盐湖化学——新类型硼锂盐湖,北京:科学出版社,2007:179-200]
5 Spessard,J.E.J.Inorg.Nucl.Chem.,1970,32(8):2607
6 Ingri,N.Acta Chem.Scand.,1963,17:573
7 Ingri,N.Acta Chem.Scand.,1962,16:439
8 Liu,Z.H.;Gao,B.;Hu,M.C.;Li,S.L.;Xia,S.P.Spectrochim. Acta A,2003,59(12):2741
9 Liu,Z.H.;Gao,B.;Li,S.;Hu,M.;Xia,S.Spectrochim.Acta A, 2004,60(13),3125
10 Hirao,T.;Kotaka,M.;Kakihana,H.J.Inorg.Nucl.Chem.,1979, 41(8):1217
11 Li,X.P.;Gao,S.Y.;Liu,Z.H.;Hu,M.C.;Xia,S.P.Spectrosc. Spect.Anal.,2005,25(1):48
12 Salentine,C.G.Inorg.Chem.,1983,22(26):3920
13 Li,W.;Gao,S.Y.J.Indian Chem.,1997,74:525
14 Tsuyumoto,I.;Oshio,T.;Katayama,K.Inorg.Chem.Commun., 2007,10(1):20
15 Ohtaki,H.;Radnai,T.Chem.Rev.,1993,93(3):1157
16 Fang,C.H.;Toshio,Y.;Hisanobu,W.;Hitoshi,O.Chin.Sci.Bull., 1996,41(16):1353
17 Nies,N.P.;Hulbert,R.W.J.Chem.Eng.Data,1967,12(3):303
18 Qinghai Institute of Salt Lakes,Chinese Academy of Sciences. Analysis methods for brines and salts.Beijing:Science Press,1988: 437 [中国科学院青海盐湖研究所.卤水和盐的分析方法.北京:科学出版社,1988:437]
19 Prince,E.International tables for crystallography.3rd ed.London: Kluwer Academic Publishers,2004,Vol.C:230,255,555,658
20 Xu,J.X.;Fang,Y.;Fang,C.H.Chin.Sci.Bull.,2009,54(12): 2022
21 Feng,W.S.;Fang,Y.;Xu,J.X.;Fang,C.H.;Jia,Q.J.Acta Phys.-Chim.Sin.,2008,24(3):497 [冯望生,房 艳,徐继香,房春晖,贾全杰.物理化学学报,2008,24(3):497]
22 Xu,J.X.;Fang,Y.;Fang,C.H.Comput.Appl.Chem.,2009,26 (5),553 [徐继香,房 艳,房春晖.计算机与应用化学,2009, 26(5),553]
23 Fang,C.H.;Fang,Y.;Jia,Q.J.;Wang,H.H.;Jiang,X.M.;Wang, Y.Z.;Chen,Y.;Lin,L.J.;Qin,X.F.Nucl.Technol.,2007,30(7): 560 [房春晖,房 艳,贾全杰,王焕华,姜晓明,王玉柱,陈 雨,林联君,秦绪峰.核技术,2007,30(7):560]
24 Ohtaki,H.;Fukushima,N.A.J.Solution Chem.,1992,21(1):23
25 Leberman R.;Soper,A.K.Nature,1995,378(655):364
26 Filatov,S.K.;Bubnova,R.S.Borate crystal chemistry[C]//3rd International Conference on Borate Glasses,Crystals and Melts. Sofia,Bulgaria,Jul 04-09,Soc Glass Technology:Sofia,Bulgaria, 2000:216-224
27 Menchetti,S.;Sabelli,C.Acta Crystallogr.Sect.B:Struct.Sci, 1978,34:45
28 Merlino,S.;Sartori,F.Acta Crystallogr.Sect.B:Struct.Sci,1972, 28:3559
29 Sorenson,J.M.;Hura,G.;Glaeser,R.M.J.Chem.Phys.,2000, 113(20):9149
30 Mesmer,R.E.;Baes,C.F.;Sweeton,F.H.Inorg.Chem.,1972,11 (3):537
31 Weres,O.J.Solut.Chem.,1995,24(5):409
32 Fang,C.H.;Ma,P.H.Acta Chim.Sin.,2000,58(11):1393 [房春晖,马培华.化学学报,2000,58(11):1393]
33 Fang,C.H.;Fang,Y.;Guo,Y.M.;Yang,B.;Lei,Y.C.Acta Chim. Sin.,2004,62(3):268 [房春晖,房 艳,郭亚梅,杨 波,雷亚川.化学学报,2004,62(3):268]
Structure of Supersaturated Aqueous Sodium Pentaborate Solution
ZHOU Yong-Quan1,2FANG Chun-Hui1,*FANG Yan1,*
(1CAS Key Laboratory of Salt Lake Resources and Chemistry,Qinghai Institute of Salt Lakes,Chinese Academy of Sciences, Xining 810008,P.R.China;2Graduate School of Chinese Academy of Sciences,Beijing 100049,P.R.China)
Wedeterminedthetime-averagedandspace-averagedstructuresofsupersaturatedaqueoussodiumpentaborate solutions by rapid liquid X-ray diffractometry at 298 and 323 K.Difference radial distribution functions(DRDF)and their theoretical partial radial distribution functions for B-B,B-O,O-O,Na-O and Na-B atom pairs were obtained from accurate diffraction data.The effects of concentration and temperature on the structure of the solutions were also discussed.Three main species(B3O3(OH)-4,B5O6(OH)-4and B(OH)3)were found to exist in supersaturated aqueous sodium pentaborate solutions and their hydrated structures were determined by model design and quantitative calculations. Higher temperature and higher concentration result in higher polyborates.As the concentration decreases,interaction distances and the average coordination number of the octahedral hexahydrated Na+ion hardly changes while the hydration numberof the polyborate increases.In concentrated solutions,the terminal-oxygen of the polyborates connects with the hydrated Na+in a monodentate form to produce a contact ion pair with a characteristic distance of 0.328 nm.
Solution structure; X-ray diffraction; Sodium pentaborate; Supersaturated aqueous solution; Radial distribution function; Polyborate anion
O645
Received:January 20,2010;Revised:June 1,2010;Published on Web:July 7,2010.
*Corresponding authors.FANG Chun-Hui,Email:fangch@isl.ac.cn.FANG Yan,Email:fangy8@isl.ac.cn;Tel:+86-971-6317021.
The project was supported by the Major State Basic Research Development Program of China(973)General Program(2008CB617612)and National Natural Science Foundation of China(20873172).
国家重点基础研究发展计划前期专项(2008CB617612)和国家自然科学基金(20873172)资助项目
ⒸEditorial office of Acta Physico-Chimica Sinica
