硅胶柱层析分离纯化TPGS的工艺*
2010-11-02常银子杨亦文任其龙张子安
常银子,杨亦文,任其龙,张子安
1(浙江农林大学农学院,浙江临安,311300)2(浙江大学材料与化工学院,浙江杭州,310027)
硅胶柱层析分离纯化TPGS的工艺*
常银子1,杨亦文2,任其龙2,张子安1
1(浙江农林大学农学院,浙江临安,311300)2(浙江大学材料与化工学院,浙江杭州,310027)
采用硅胶层析法对自制的聚乙二醇1 000 VE琥珀酸酯(TPGS)进行分离纯化,考察了柱温、上样量、上样浓度和流量等因素对TPGS分离效果的影响,优选出TPGS分离的工艺条件,并对其进行了验证。结果表明:随着柱温、上样量或流量的增加,TPGS分离纯度和回收率均表现为“先增后降”趋势;TPGS分离适宜工艺条件为40℃柱温、4 g上样量、0.3 g/mL上样浓度和3mL/min流量,在此条件下,TPGS分离的平均纯度和回收率可达93.13%和97.72%。
TPGS,水溶性VE,分离,硅胶柱
聚乙二醇1 000VE琥珀酸酯(TPGS)是由VE琥珀酸酯(VES)与聚乙二醇 (PEG)1 000酯化反应生成的一种VE水溶性衍生物,结构上含有VE亲脂基团和聚乙二醇长链的亲水基团,亲水亲油平衡值(HLB)约为13~17,具备表面活性剂的性质和良好的水溶性[1]。TPGS为淡黄色的蜡状固体,近乎无味,熔点约39℃,能稳定存在于高温(200℃以下)和空气环境中[2]。鉴于TPGS的两性特性(亲水性与亲脂性)、良好的水溶性以及热稳定性等理化性质,该物质可作为增溶剂、乳化剂、吸收增强剂、可塑剂以及脂溶性药物载体等的理想材料。目前,TPGS在国外已被广泛应用于制药和营养品添加剂等领域[3],但国内对TPGS的研究甚少,主要集中于TPGS的制备和性能方面[4]。作者前期研究发现[5],TPGS 合成产物中存在一定量的VES,而VES和TPGS在极性上有很大差别,有必要对TPGS进行精制。本文采用硅胶柱层析法对自制的TPGS进行分离纯化,考察其影响因素,进而运用正交试验设计方法优化出层析分离TPGS的最佳工艺条件。
1 材料与方法
1.1 材料与仪器
TPGS,实验室自制;TPGS标准品(含量99%),美国Eastman公司;硅胶(粗孔硅胶Ⅱ号)100目,青岛海洋化工厂;乙酸乙酯、石油醚、氯仿、甲醇、无水乙醇:均为分析纯,中国医药集团上海化学试剂公司;常压带夹套层析柱(玻璃,φ20 mm×500 mm);RE52-99型旋转蒸发器,上海亚荣生化仪器厂;BS400S型电光分析天平,北京赛多利斯天平有限公司;DZF-6050型真空干燥箱:上海一恒科技有限公司;SC-15型数控超级恒温箱,宁波天恒仪器厂;LC-10AT型高效液相色谱仪,717型Plus型自动进样器,1525型泵,2487双波长吸收检测器(均为Waters公司)。
1.2 试验方法
1.2.1 预试验
通过梯度洗脱后,发现硅胶柱可以对TPGS实现提纯,采用纯三氯甲烷时,无法洗脱吸附在硅胶上的TPGS,溶剂V(石油醚)∶V(三氯甲烷)=9∶2洗脱出来的基本上是前面合成反应后过量的PEG,而用V(石油醚)∶V(三氯甲烷)∶V(乙酸乙酯)=6∶2∶1 混合溶剂刚洗脱出来的产品,通过HPLC分析检测,发现在292 nm波长范围内有2个峰,可能是VES琥珀酸单酯(VES)和聚乙二1 000VE琥珀酸双酯,同时出现3个峰可能是VS、TPGS双酯和TPGS单酯,并且VES的峰面积逐渐变小。后面出现1个峰可能是TPGS双酯和单酯,只有1个峰的可能是TPGS单酯。由于目前尚未对TPGS双酯和单酯进行研究,实验中未把TPGS单酯和双酯分离出,因此在之后的实验分析中均以TPGS单酯和双酯混合物的纯度和回收率作为指标,而以TPGS单酯和双酯混合物作为产品。
1.2.2 单因素影响试验程序
试验选取纯度和回收率作为TPGS分离纯化效果的衡量指标,依次考察柱温、上样量、上样浓度和流量等分离条件对TPGS分离效果的影响[6-7]。
(1)装柱:称取50 g左右硅胶,150℃下活化2 h,湿法装柱。
(2)上样:取1~5.5 g已制备好的TPGS,用甲醇溶解,浓度控制在0.1~0.4 g/mL。

图1 标准曲线
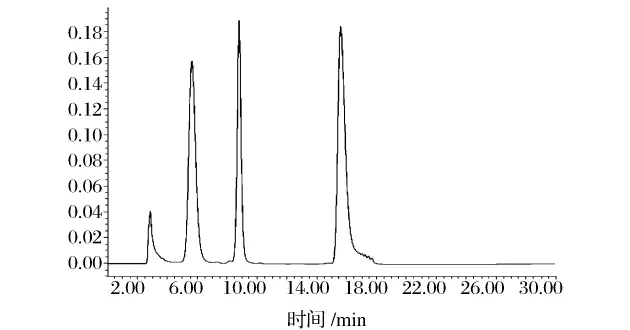
图2 预试验结果
(3)硅胶柱层析:以石油醚-三氯甲烷-乙酸乙酯梯度洗脱,先后用 V(石油醚)∶V(三氯甲烷)=9∶2、V(石油醚)∶V(三氯甲烷)∶V(乙酸乙酯)=6∶2∶1、V(三氯甲烷)∶V(乙酸乙酯)=7∶2依次以2~5mL/min的流量进行洗脱。每组梯度分别为550、600和450mL,直至无TPGS流出时停止。
(4)流分收集:每份50mL,旋蒸法蒸干,称重,取样,定容。V(石油醚)∶V(三氯甲烷)=9∶2、V(石油醚)∶V(三氯甲烷)∶V(乙酸乙酯)=6∶2∶1 处流分收集作为产品,并依次标号。
(5)含量检测:采用高效液相色谱法,双波段检测。分析方法按TPGS的合成工艺中检测方法进行[7]。
(6)计算纯度和收率:根据HPLC分析结果,以标准样品浓度为横坐标,峰面积坐标,得到一直线,拟和得到拟和的标准曲线方程,得到回归方程y=3×106-684 072,相关系数R2=0.999 4。将待测产物的峰面积值相应标准曲线方程内,得出相应产物浓度[8~9]。
TPGS的纯度(x)/%=n×100/m
TPGS的收率(y)/%=n* ×100/n
其中:m为1 050mL流分旋蒸蒸干后的质量,g;n为原料中PEG的量,g;n*为分离后TPGS的量,g。
1.2.3 正交试验设计
在单因素试验基础上,选取对TPGS分离效果影响较大的因素进行多因素正交试验(表1)。
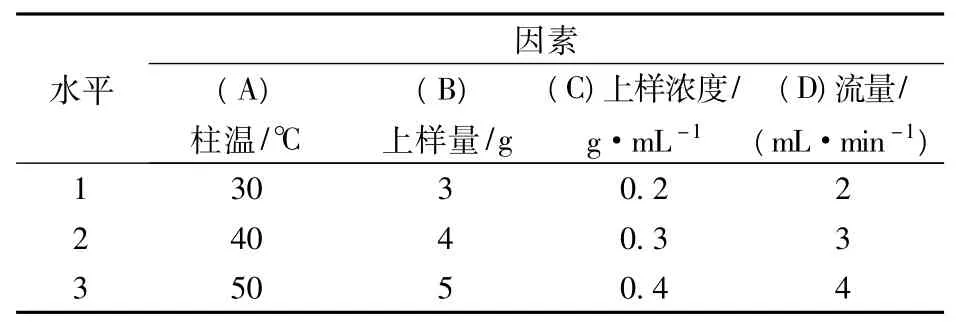
表1 正交试验所考察因素及其水平
2 结果与讨论
2.1 单因素试验
2.1.1 柱温对分离效果的影响
柱温考察范围为20~50℃。具体反应条件为:上样量4 g,上样浓度为0.3 g/mL,流量3mL/min。柱温对于分离的影响结果如图3和表2所示。
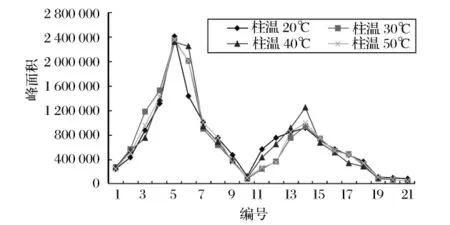
图3 不同柱温的洗脱曲线
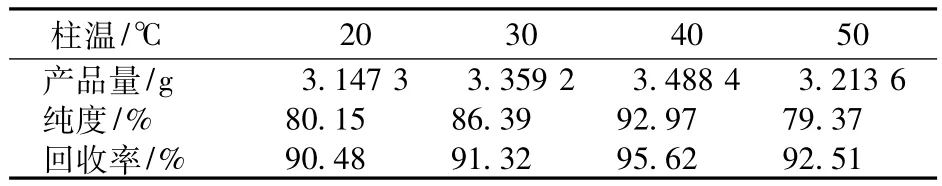
表2 柱温对纯度和回收率影响
由表2可以看出,柱温对TPGS分离效果影响较大,当柱温由20℃升至40℃,纯度和回收率均呈现增加趋势。但进一步升高温度至50℃,2个标值明显下降。图3和表2均表明,在40℃柱温条件下可分离出最大量的TPGS,且对TPGS单酯和双酯分离效果最佳,此时纯度和回收率分别高达92.97%和95.62%。因此以下试验采用40℃柱温进行TPGS分离。
2.1.2 上样量对分离效果影响
控制40℃柱温、3mL/min流量和0.3 g/mL的上样浓度,考察上样量在1~5.5 g内对TPGS分离效果的影响,结果见图4和表3。
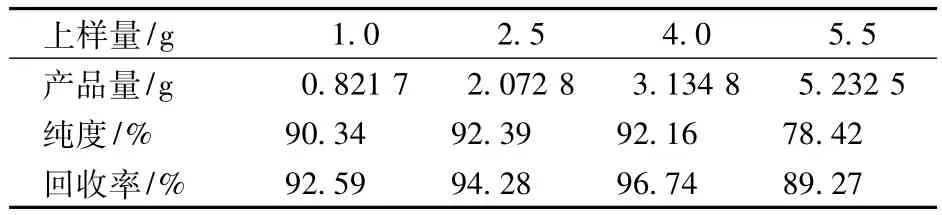
表3 上样量对TPGS的影响
从表3可以看出,上样量对TPGS的分离也有较大影响,随上样量的增加,回收率也表现为“先增后降”的趋势。上样量为4.0 g时,回收率达到最大值(96.74%)。而纯度在上样量较小时变化不大,均在90% 以上,但当上样量增至5.5 g,纯度下降明显。图4也同样反映出高上样量条件下TPGS的分离效果欠佳。原因可能是上样量过高,超过了硅胶柱所能达到的吸附量,因而反应后期难以分离出杂质,导致TPGS洗脱效果下降。以下试验上样量控制在4 g。
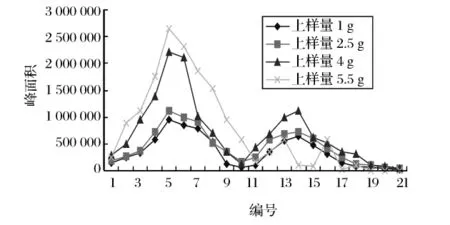
图4 不同上样量的洗脱曲线
2.1.3 上样浓度对分离效果的影响
上样浓度可能会影响到硅胶柱的吸附效果,由此对分离效果产生一定影响。本试验考察了上样浓度于0.1~0.4 g/mL内变化对分离效果的影响。试验在柱温为30℃、上样量为4 g、流量为3mL/min的条件下进行,试验结果见图5和表4。
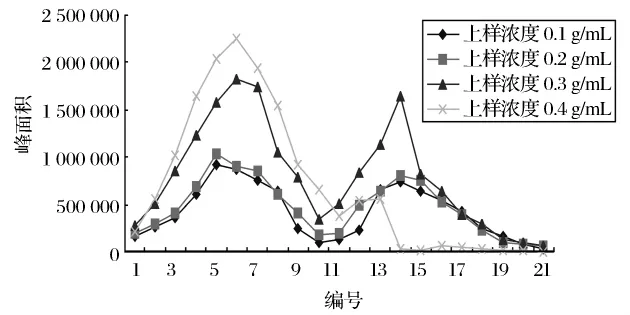
图5 不同上样浓度的洗脱曲线
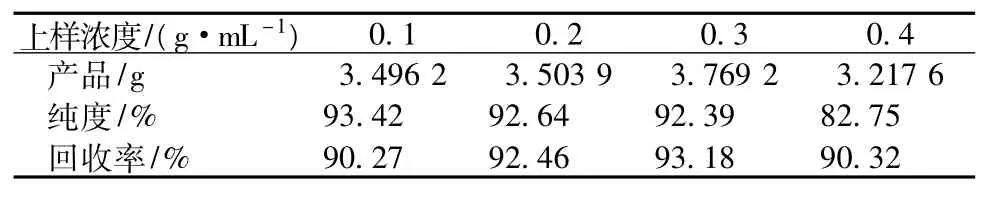
表4 上样浓度对TPGS的影响
从图5和表4可以看出,上样浓度较低时(0.1~0.3 g/mL),TPGS纯度较高且稳定。但上样浓度增至0.4 g/mL时,TPGS纯度急剧下降。回收率受上样浓度的影响相对小,当上样浓度为0.3 g/mL时,TPGS回收率最大,达到93.18%。以下试验选择0.3 g/mL上样浓度。
2.1.4 流量对分离效果的影响
试验控制柱温为30℃,上样量为4 g,上样浓度为0.3 g/mL。调节流量由2mL/min梯度递增至5mL/min,考察流量对分离效果的影响,结果见图6和表5。从图6和表5看出,随着流量的增加,TPGS分离纯度及其回收率为先增后降。流量增大TPGS的各项指标都会减少,当流量在4mL/min时,产品量为3.139 2 g,同时纯度为90.59%,比低流量的TPGS量要低,之后纯度、回收率都降到最低点。产生这种结果的原因可能是由于当流量过大时,TPGS与硅胶的接触时间要短,在这种情况下TPGS在硅胶柱上可能无法达到吸附平衡,导致TPGS伴随洗脱剂的流出而流出,因此达不到分离的效果。但流量太少会导致分离过程太过漫长,耗费大量的人力物力,因此本实验的流量选择3mL/min。
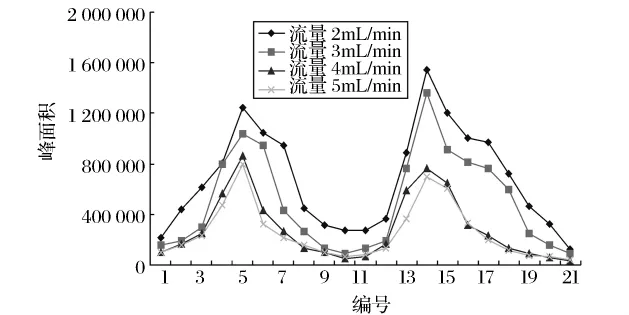
图6 不同流量的洗脱曲线
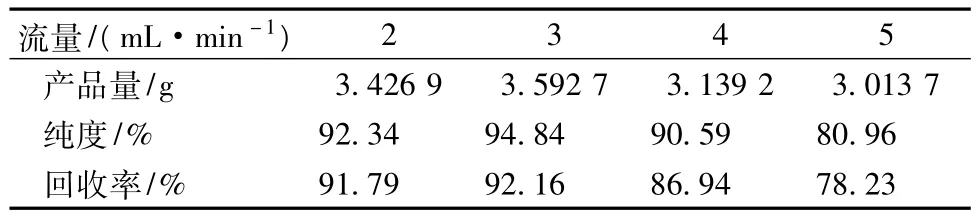
表5 流量对TPGS总的影响
2.2 分离条件的优化
单因素试验结果表明,柱温、上样量、上样浓度和流量对TPGS的分离效果均产生一定影响。为优化出硅胶柱层析分离TPGS的理想工艺条件,并区分出主次影响因素,本研究在单因素试验结果基础上,借助不完全多因素试验方法与理论,安排了4因素3水平的正交试验,结果见图7与表6。
对比表6中纯度和回收率数值可知,2号(A1B2C2D2)和8号(A3B2C2D3)分离效果相对较好。而图7显示出在不同分离条件下的TPGS分理效果差异比较显著,其中 2号(A1B2C2D2)和 5号(A2B2C3D1)分离效果具有明显优势。
表6中k值为各因素在相应水平下的试验结果之和与水平数的比值,其值排除了其他因素的干扰,可反映该因素的水平效应。比较表6中k值大小可以看出,若以纯度为考察指标,因素A(柱温)对应的k2与k3值相差很小,因而可取 A2-3B2C2D2为最大程度提高TPGS纯度的理想工艺条件组合;而若以回收率为考察指标,考虑到因素A对应的各k值无明显差别,而因素C(上样浓度)对应的k1与k2值相差甚微,故认为A1-2-3B3C1-2D2组合为回收TPGS的较佳工艺条件。
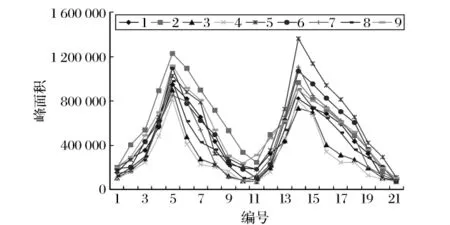
图7 不同分离条件组合的TPGS洗脱曲线
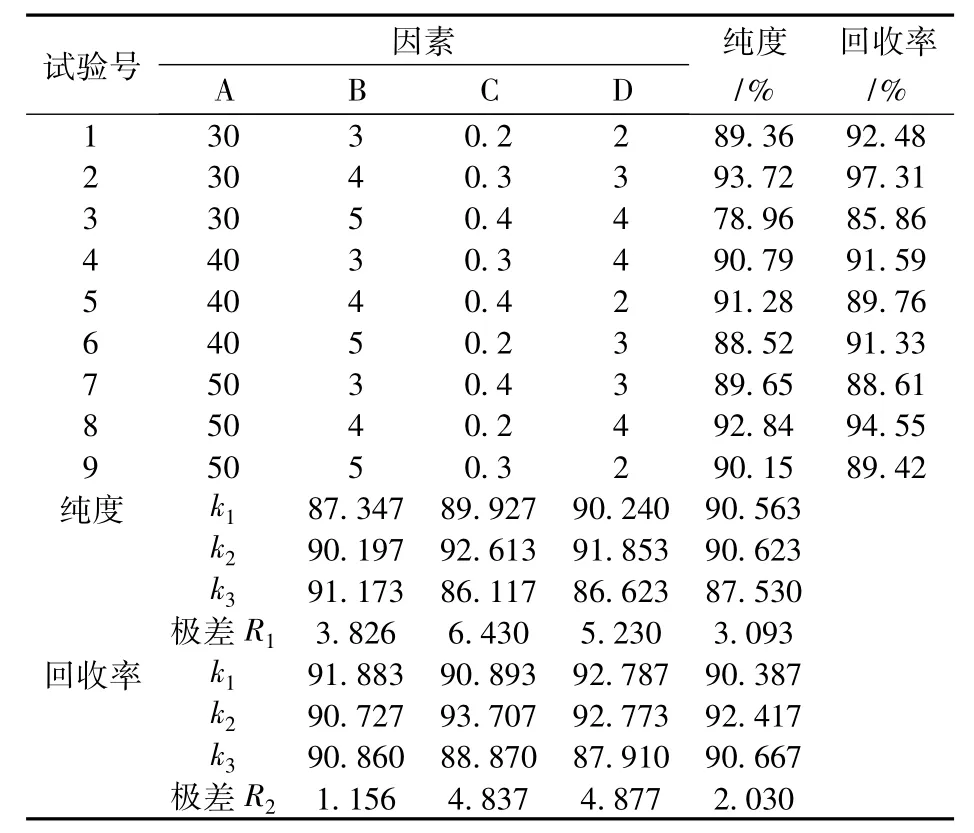
表6 TPGS分离正交试验结果
R值可反映出相应因素对试验结果影响的显著性。由表6可看出,各因素对纯度指标的影响主次顺序为B>C>A>D,对回收率指标的影响主次顺序为C>B>D>A。
综合考虑上述分析结果,衡权纯度和回收率两项指标,并结合实际物耗与能耗等因素,可取A2B2C2D2组合(柱温30℃、上样量4 g、上样浓度0.3 g以及流量3mL/min)为硅胶柱层析分离TPGS最佳工艺条件。
2.3 验证试验
按上述正交试验最佳水平组合进行3次重复试验,考察优化结果的稳定性与重现性,结果见表7所示。由表7可知,该最优分离条件下,TPGS平均纯度和回收率分别达到97.72%和93.13%。3次试验结果差异较小,说明该工艺条件组合稳定可靠。
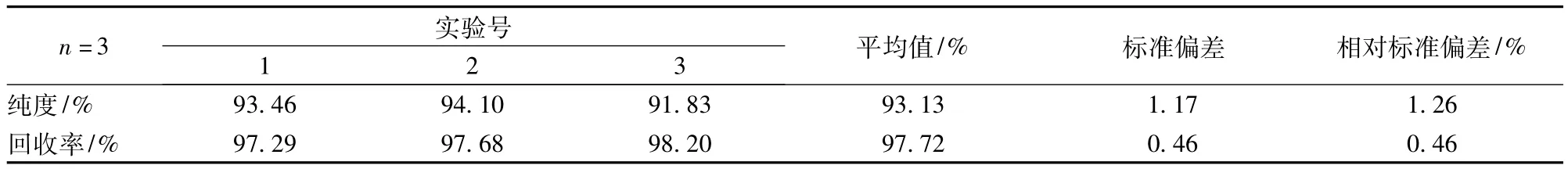
表7 合成条件的验证结果
3 结论与展望
(1)单因素试验结果表明,各考察因素对分离效果均产生不同程度地影响。试验条件下,随着柱温、上样量或流量的增加,TPGS分离纯度及其回收率均表现为“先增后降”的趋势,表明TPGS分离过程中该三因素存在着最佳值。上样浓度对两项考察指标影响规律各异。
(2)正交化化试验结果表明,硅胶柱层析分离TPGS的最佳工艺条件为:柱温30℃,上样量4 g,上样浓度0.3 g和流量3mL/min。各因素对纯度指标的影响主次顺序为:上样量 >上样浓度 >柱温 >流量,对回收率指标的影响主次顺序为:上样浓度 >上样量 >流量 >柱温。
(3)验证试验结果表明,硅胶层析法分离纯化TPGS具有较好的稳定性与重现性。在最佳工艺条件下,TPGS平均纯度和回收率分别可达93.13%和97.72%。
预试验发现TPGS的产品非单一物质,至少存在TPGS单酯和双酯两种成分,因此下一步拟开展TPGS单酯和双酯分离条件的影响规律及其优化等方面的研究。
[1]于永新,俞红凯,王中彦.聚乙二醇1000维生素E琥珀酸酯应用进展[J].沈阳药科大学学报,2006,23(6):407-412.
[2]伍林,王艳,鲁亮,等.维生素E琥珀酸酯的研究[J].食品科学,2005,26(9):320-322.
[3]许牡丹,汤木红,王小燕.硅胶柱层析法分离纯化甘露低聚糖[J].食品工业技术,2008(9):188-190.
[4]Weber T,Lu M,Andera L,et al.Vitamin E succinate is a potent novel antineoplastic agent with high selectivity and cooperativity with tumor necrosis factor-related apoptosisinducing ligand(Apo2 ligand)in vivo[J].Clinieal Cancer Researech,2002-8:863-869.
[5]常银子,杨亦文,任其龙,等.水溶性维生素E的合成工艺研究[J].安徽大学学报:自然版,(已录用).
[6]辛嘉英,吴小梅,赵永杰,等.脂肪酶催化水解反应纯化a一生育酚琥珀酸酯[J].分子催化,2005,19(4):285-288.
[7]Fische R.Pharmaceutical preparation with cyclosporinA[P],US.6696413,2004-02-24.
[8]金萱,杨亦文,任其龙,等.天然维生素E琥珀酸酯的HPLC测定[J].中国医药工业杂志,2005,36(9):560-561.
[9]樊明涛,吴守一,马海乐.维生素E测定方法的研究进展[J].江苏大学学报:自然科学版,2002,23(1):54-57,74.
Separation and Purification of TPGS by Silica Gel Column Chromatography
Chang Yin-zi1,Yang Yi-Wen2,Ren Qi-long2,Zhang Zi-an1
1(College of and Food Food and Agriculture,Zhejiang Forestry University,Lin'an 311300,China)2(College of Materials Science and Chem ical Engineering,Zhejiang University,Hangzhou 310027,China)
We purified the TPGS though Silica gel column chromatography.In order to improve separation conditions,chromatography temperature,load of sample,concentration of sample and flow rate factors were tested to see the influence to the separation.The optimal conditions of silica gel column chromatography were as follows:Chloroform,Petroleum ether and Acetic ether were used as mobile phases,the chromatography temperature is 40℃,the load of sample is 4g,the concentration of sample is 0.3g/mL,and the flow rate is 3ml/min.Finally the average purity is 93.13%,and the average yield is 97.72% .
TPGS,water-soluble vitamin E,separation,silica gel column chromatography
硕士,讲师。
*2009年浙江省高等学校青年骨干教师国内访问学者项目
2010-04-03,改回日期:2010-06-25
