钼酸盐缓蚀剂在A20碳钢表面成膜行为研究*
2010-09-30冉文斌马凤云刘景梅
冉文斌,马凤云,刘景梅
钼酸盐缓蚀剂在A20碳钢表面成膜行为研究*
冉文斌1,马凤云2*,刘景梅2
(1.新疆康佳投资(集团)有限责任公司,新疆克拉玛依834014;2.新疆大学化学化工学院,新疆乌鲁木齐830046)
在标准配制水条件下,通过失重法、跟踪测定试验水中MoO42-和O2浓度及SEM形貌分析,研究了MoO42-对A20碳钢在循环冷却水中的缓蚀行为,分析其成膜机理。结果表明,钼酸盐在碱性水中具有一定缓蚀作用;是一种阳极型成膜剂,成膜过程分为诱导期、生长期和稳定期3个阶段。诱导期约24 h,生长期约48 h,药剂浓度愈高,愈有利于膜的生长。在稳定期,维持药剂质量浓度为100 mg/L即可;FeMoO4在生长期其晶核呈竹签状,在稳定期晶体呈玉米棒状。
钼酸盐;缓蚀剂;成膜机理;标准配制水
随着人类对环境保护的呼声愈来愈高,金属缓蚀剂已向绿色、高效发展。众多研究表明,钼酸盐作为工业循环冷却水金属缓蚀剂[1-3],因具有无毒、稳定、配伍性好、适应工况宽等特点[4-6],愈来愈被青睐。本研究旨在以A20碳钢为对象,以标准配制水为工作环境,通过跟踪测定相关参数、SEM成膜分析和EDS元素分析,考察其对A20碳钢的缓蚀率、缓蚀机理和成膜行为。
1 试验部分
1.1 试验材料、药品和仪器
1.1.1 试验材料与处理
试验材料为50 mm×25 mm×2 mm和10 mm×10 mm×2 mm的A20碳钢挂片。试验前,先用游标卡尺精密测量挂片的三维尺寸,准确计算表面积。后用蒸馏水、无水乙醇依次清洗,擦干,放入干燥皿24 h后,准确称重至0.000 1 g,待用。试验后,挂片用10%HCl+1.0%六次甲基四胺洗液、蒸馏水、无水乙醇依次清洗,擦干,置于干燥皿中干燥24 h,再准确称重至0.000 1 g。
1.1.2 试验药品和仪器
药品:分析纯 CaCl2、NaCl、NaHCO3、MgSO4和Na2MoO4。
仪器:RCC-I旋转挂片仪,江苏高邮仪器厂;JYD-1A溶解氧测定仪,江苏电分仪器厂;722-1分光光度计,上海第三仪器厂;扫描电镜SEM,德国LED-143OVP;能谱耗散仪EDS。
1.1.3 标准配制水制备
称 取 14.45 g CaCl2、16.45 g NaCl、4.20 g NaHC O3和12.33 g MgSO4,用少许蒸馏水完全溶解后,移置25 L蒸馏水中,制得如表1所示的标准配制水。pH≈8.15,L.S.I.=0.085>0,为结垢型水。

表1 标准配置水组成Table 1 Composition of prepared water mg/L
1.2 试验方法
1.2.1 静态失重法
依照HG/T 2159-1991[7]进行。
试验条件:温度=(50±1)℃,时间=168 h,c(MoO42-)=0,50,100,200 和 400 mg/L,烧杯必须密封。
缓蚀率计算:
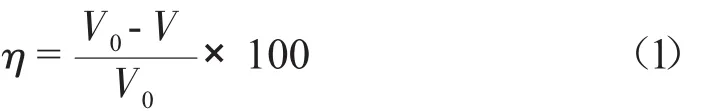
式
(1)中:η-缓蚀率,%;
V0-空白挂片腐蚀速率;
V-试验挂片腐蚀速率。
1.2.2 MoO42-工作曲线绘制和浓度测定[8]
试验前,按照文献[8]绘制MoO42-工作曲线,如图1所示。工作曲线y=0.068 3 x,R2=0.999 1。试验时,每4 h取样1次,测定其吸光度,由图1确定试液浓度。
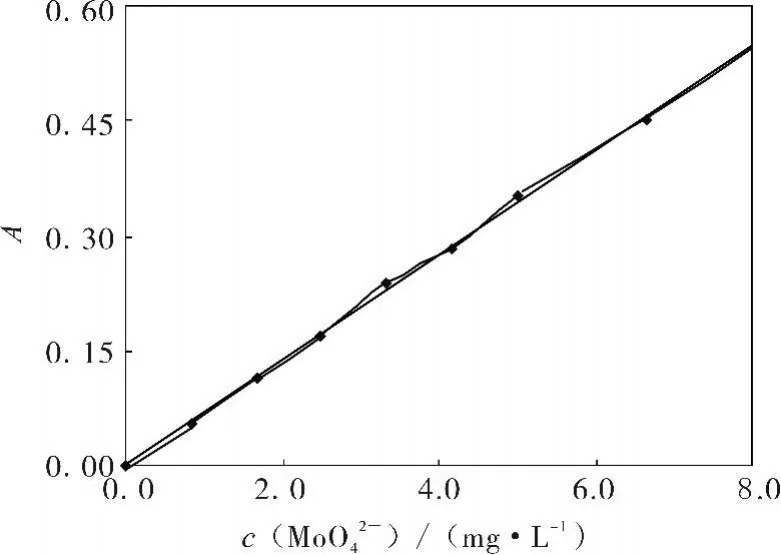
图1 MoO42-工作曲线Fig.1 Working curve of MoO42-
1.2.3 溶解氧浓度和pH值测定
每4 h取样1次,用JYD-1A溶解氧仪和pHS-3B计测定试液溶解氧浓度和pH值。
1.2.4 成膜SEM扫描和EDS元素分析
试验结束后,取出10 mm×10 mm×2 mm挂片,用蒸馏水轻轻冲洗,擦干,做SEM和EDS分析。
2 试验结果与分析
2.1 MoO42-浓度变化
MoO42-初始质量浓度为 0,50,100,200 和 400 mg/L,在0~168 h内随时间的变化如图2所示。
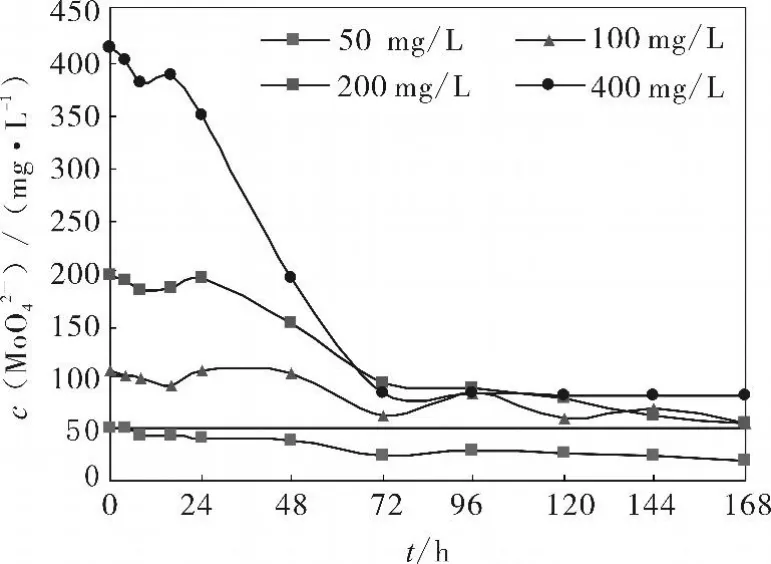
图2 S.I=-5.465时MoO42-工作曲线Fig.2 Working curve of MoO42-at S.I=-5.465
由图2可见,无论MoO42-初始浓度高低,在试验初始的24 h,变化甚微。这意味着挂片表面尚处于成膜的诱导期。在24~72 h内,均有降低。尤其在初始浓度>100 mg/L时,浓度愈高,下降幅度愈大,但最终稳定在约100 mg/L。这表明挂片表面进入成膜的生长期,推测MoO42-浓度愈高,成膜厚度应愈厚,缓蚀率应提高。100 mg/L是MoO42-在试验条件下的最大浓度。这基本与FeMoO4溶解度数据吻合。20℃下,FeMoO4的溶解度=76 mg/L[10]。试验温度为50℃,故稍高。当初始浓度≤100 mg/L时,有降低,但幅度小,减小量未超过50%。在72~160 h内,浓度几乎不变。这表明挂片表面已进入成膜的稳定期。
2.2 溶解氧浓度变化
图 3 是 MoO42-初始浓度分别为 0,50,100 和200 mg/L时,在0~168 h时间内试液中O2浓度随时间的变化。
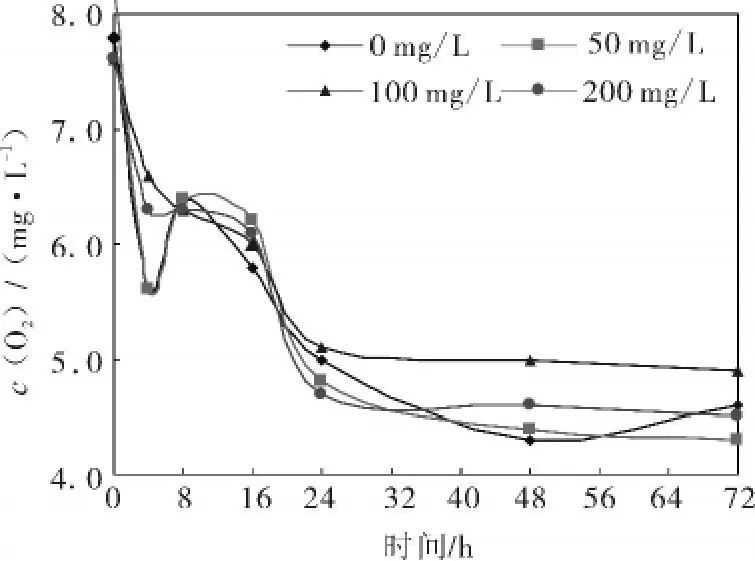
图3 S.I=-5.465时O2浓度随时间变化情况Fig.3 Change of O2concentration with time at S.I=-5.465
由图3可知,O2浓度随时间变化与药剂无关。在试验初始8 h,急速下降,从初始的7.5 mg/L降到约4.2 mg/L。这是由于初始挂片表面完全裸露,腐蚀电池的阳极反应使Fe=Fe2++2e,阴极反应使水中的氧离子化,,迅速取走金属表面的离子,加速了腐蚀过程的进行,氧浓度迅速衰减。根据经验回归分析,得其回归公式为c(O2)=0.05t2-0.8t+7.5,R2=1。氧浓度随时间增加呈二次幂函数关系降低。在8~72 h内,O2浓度随时间变化为c(O2)=-0.011 3 t+4.75,R2=0.934 6。这一现象可用金属的平衡电位理论[9]解释。平衡电位理论认为,随着金属Fe不断的氧化成Fe2+进入试液,挂片表面上留下相应的电子愈来愈多,负电子与Fe2+的相互吸引愈来愈强烈,使金属Fe的离子化愈来愈困难,最终达到Fe=Fe2++2e平衡。
2.3 缓蚀速率曲线
不同浓度下缓蚀速率曲线如图4所示。
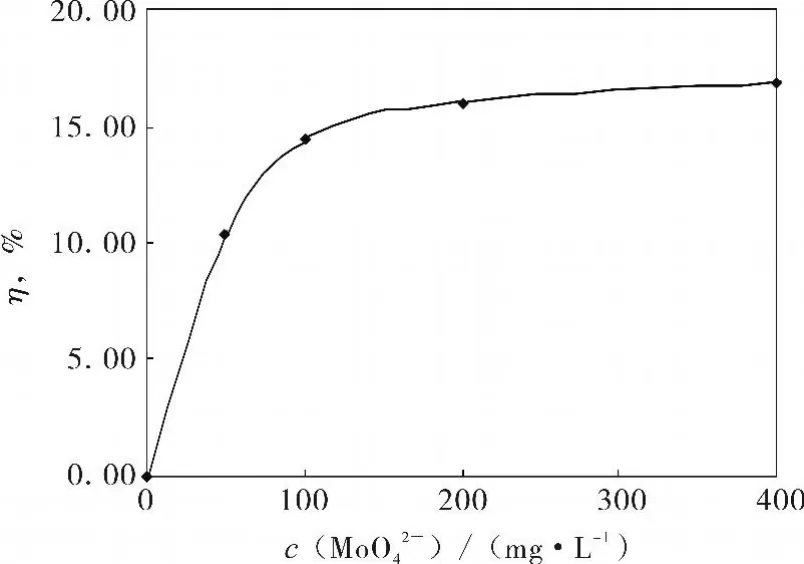
图4 S.I=-5.465时不同MoO42-浓度下缓蚀速率曲线Fig.4 Corrosion inhibition curve of MoO42-concentration at S.I=-5.465
由图4可知,药剂浓度低时,随浓度增加,缓蚀速率提高幅度较大;当浓度较高时,缓蚀速率提高幅度减小;当质量浓度超过100 mg/L时,缓蚀速率基本不变。由此,表明两个问题。其一,该药剂的“浓度-缓蚀性能”具有“低剂量效应”特点,结果可信;其二,缓蚀速率未超过20%。究其原因是结垢型水质。另外,也表明对A20碳钢而言,钼酸盐作为单一缓蚀剂使用有可能达不到预期效果。
2.4 成膜表面SEM分析
图5是试片SEM放大5 000倍的图片。其中:图 5(1) 为试验前试片,5(2、3、4) 分别为试验后MoO42-浓度为 0、50 和 200 mg/L 的试片。图 5(1)可知,试验前,除机械加工痕迹外,试片表面光洁平整。图5(2)为空白试片,表面已变得粗糙,有明显的均匀腐蚀的痕迹。上面的固体颗粒,可能是试验时溶液中析出的盐分未被冲洗干净。图5(3)中,试片表面除可观察到竹签状、玉米棒状和雪花状晶体颗粒外,确有一层膜存在,只是厚度较薄。因扫描前已自然干燥,故上面有裂痕。图5(4)与图5(3)非常相似,只是玉米棒状晶体增多,生长均匀,更加密实,成膜更加致密、厚实,无裂痕。将这两张图与图5(2)比较,显然,竹签状晶体是FeMoO4的晶核,玉米状晶体是生长成熟的FeMoO4,而雪花状晶体应该是CaCO3。因铁氧化物属无定形固体,故底层成膜的主要成分应该是氧化铁。

图5 试片的5000倍SEM图Fig.5 SEM of A20 carbon steel
2.5 成膜元素EDS谱分析
图6中3张谱图分别是MoO42-浓度为0、50和200 mg/L时,挂片表面成膜元素的EDS谱图。
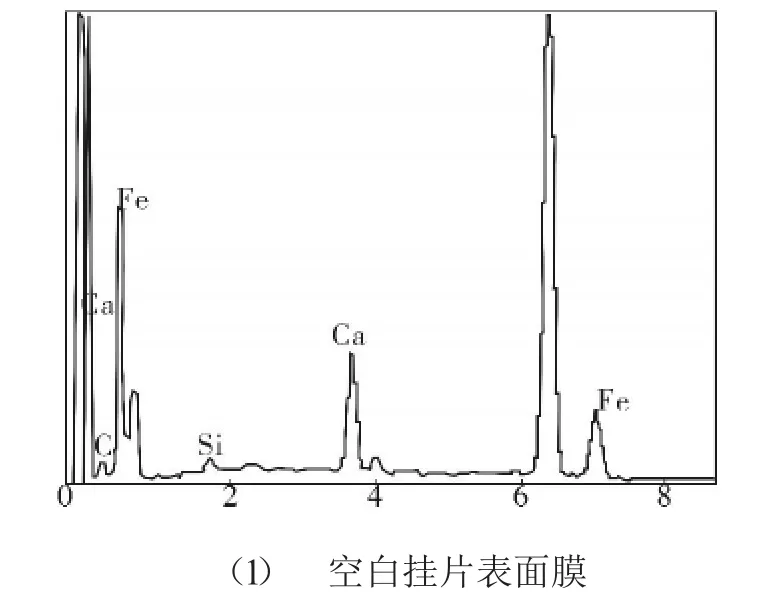
表2是据图6计算的成膜元素质量百分数和摩尔百分数。
图 6(1)表明,空白挂片表面是由 Fe、O、Ca、C和 Si元素组成。图 6(2)和 6(3)显示,除 Fe、O、Ca和C等外,有Mo存在,而无Si存在。这表明在药剂作用下,金属的腐蚀被减缓,有钼酸铁产生。从峰面积看,MoO42-初始浓度高,Mo元素含量高。
根据相关盐类的基本性质,表2数据表明:(1)当药剂浓度为零时,因Si含量仅为0.43%,故可忽略;(2)因溶液呈碱性,C应该完全以CO32-的形式存在。Ca的摩尔数远远小于CO32-的摩尔数,CaCO3的溶度积又较其他钙盐小得多。故可认为Ca完全以CaCO3的形式存在;(3)在碱性溶液中,铁的元素电势图[10]为:
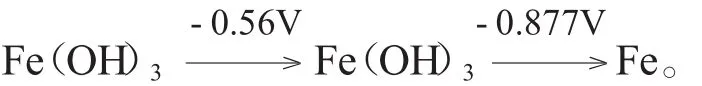
显然,后者比前者的反应趋势要强烈得多。但比较两者的溶度积常数[11]KspFe(OH)2=8.0×10-16,KspFe(OH)3=4×10-38,前者又比后者大得多。从电极电位和溶度积综合考虑,铁元素应以Fe2+为主。因此,钼酸根主要以FeMoO4形式存在,多余的CO32-以Fe CO3形式存在。据此,通过各元素的物料衡算,获得膜中各种盐类的组成见表3。
表3表明:当MoO42-含量为50 mg/L时,膜的主要组成是FeO、CaCO3和Fe CO3。这一结果与图6(2)吻合。图 6(2)中雪花状晶体很多,FeMoO4晶体呈针状,粒径小,稀疏,并未铺满整个成膜。当MoO42-含量为200 mg/L时,Fe MoO4增加到21.03%,FeO增加到78.52%,而CaCO3含量大大减小,仅为0.45%。当溶液中MoO42-初始浓度从50 mg/L提高到200 mg/L,成膜中Mo含量提高了10倍。这与图2中溶液中的MoO42含量降低相一致,说明在低浓度下提高MoO42-浓度,可在一定程度上提高缓蚀率。当MoO42-为50 mg/L,CaCO3含量达到52.92%,高于空白和200 mg/L,这一现象表明,水质结垢倾向严重。故结合阻垢的要求,药剂浓度也应高于50 mg/L为好。
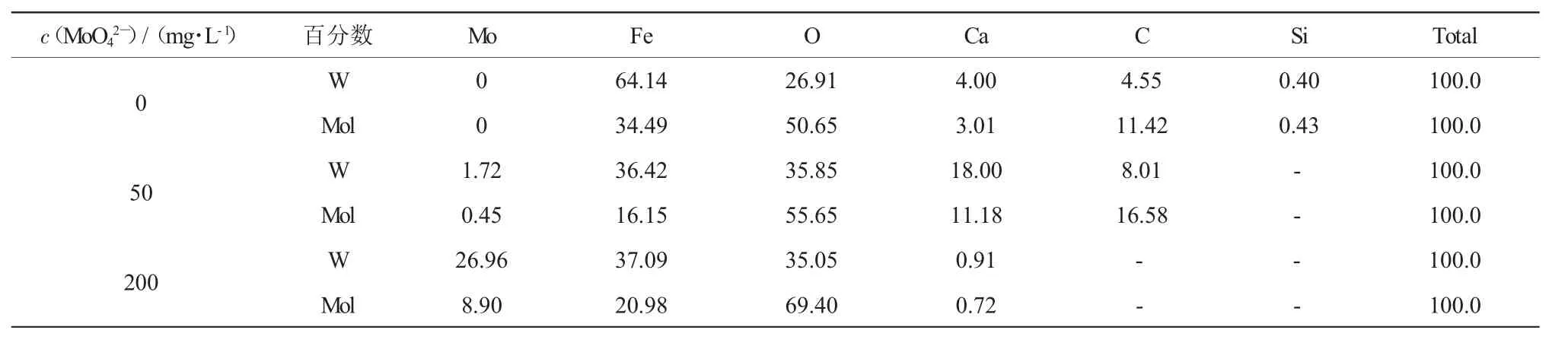
表2 由EDS谱图得到的成膜中各元素相对含量Table 2 Contents of elements in forming films by EDS %
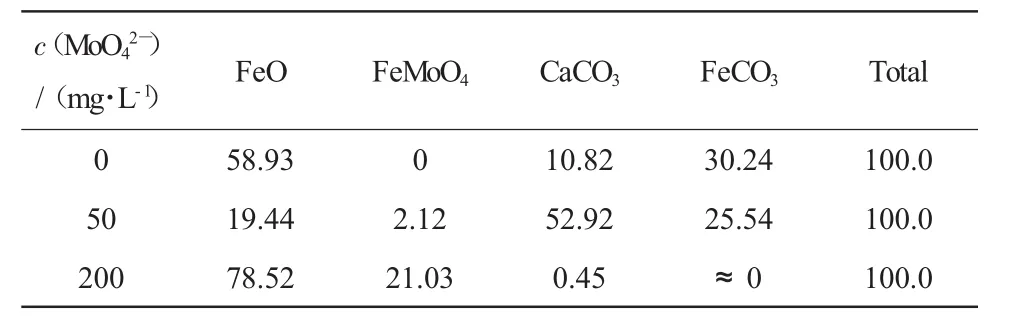
表3 膜中各种盐类的组成Table 3 Compositions of forming films %
2.6 成膜机理
综上所述,可认为钼酸盐属于阳极型成膜剂。它在阳极区反应,促进阳极极化,在金属表面生成保护膜,使阳极过程变慢,起到缓蚀作用。其成膜过程明显的分为3个阶段,即诱导期、生长期和稳定期。成膜诱导期大约为24 h。这一阶段恰好是金属铁和水中的氧同步发生离子化,是腐蚀速率最快的阶段。因此,若要提高缓蚀率,应从缩短该阶段采取措施。生长期大约48h。在此阶段,金属表面发生如式(2)所示化学反应:
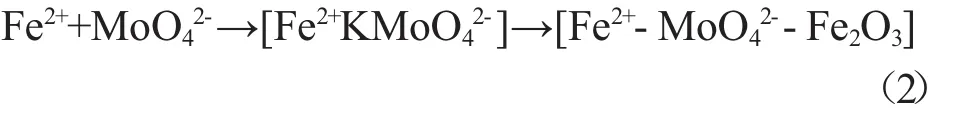
3 结论
(1)在结垢型水环境,钼酸盐对A20碳钢具有一定缓蚀作用,但缓蚀率未超过20%。因此,需复配阴极型缓蚀剂,才可能达到满意的缓蚀率。
(2)钼酸盐是一种阳极成膜剂。其成膜过程分为3个阶段,即诱导期、生长期和稳定期。诱导期大约24 h,是腐蚀过程最为迅速的时期。因此,只有缩短该阶段,才能有效地提高药剂的缓蚀率。生长期大约48 h,药剂浓度愈高,愈有利于膜的生长,且致密、厚实。其后,均为稳定期,维持药剂质量浓度为100 mg/L即可。
(3)当处于成膜生长期时,FeMoO4晶粒为针状,而成膜稳定时晶粒为棒状。氧化物为无定形状,CaCO3为雪花状。
(4)试片表面的成膜由上下两层组成,下层紧靠金属壁面,主要成分为FeO。高浓度时,上层主要成份是FeMoO4和FeCO3,膜与垢的摩尔比FeMoO4/(FeCO3+CaCO3)=46.7︰1;低浓度时,膜与垢的摩尔比 FeMoO4/(FeCO3+CaCO3)=0.027︰1,FeMoO4含量甚低。从成膜的主要成分看,金属铁和水中的氧同步发生离子化过程,这是单一钼酸盐缓蚀剂成膜的必要因素。
[1]M.Saremi,C.Dehghanian,M.MohammadiSabet[J].Corrosion Science,2006,489:1404-1412.
[2]G.Grundmeier,B.Rossenbeck,K.J.Roschmann,etal.Corrosion Science[M].2006.
[3]Celeste Rabacal Alentejano,Idalina Vieira Aoki[J].Electrochimica Acta,2004,49:2779-2785.
[4]吴宇峰.绿色环保型软化水缓蚀剂的研究[J].工业水处理,2000,20(12):31.
[5]李田.钼系复合缓蚀剂化水水质稳定的动态模拟研究[J].工业水处理,2000,20(6):9.
[6]唐俊.循环冷却水系统缓蚀剂的现状及绿色化进展[J].工业处理,2004,24(6):1.
[7]HG/T 2159-1991.化工行业标准[S].
[8]梁江庆,马凤云.工业循环冷却水肿钼酸盐类缓蚀剂M0O42-测定方法的改进[J].化工进展,2005,24(4):421-424.
[9]百科全书编委会.化工百科全书第5卷[M].北京:化学工业出版社:196-216.
[10]大连理工大学无机化学教研室.无机化学(下册)[M].3版.北京:高等教育出版社:774.
Study on Forming Film Performance of Molybdate Corrosion Inhibitor on the Surface of A20 Carbon Steel
RAN Wen-bin,MA Feng-yun,LIU Jing-mei
(School of Chemistry&Chemical Engineering,Xinjiang University,Urumq Kelamayi 830046,China)
The corrosion inhibition performance of molybdate corrosion inhibitor for A20 carbon steel was investigated by means of weight loss measurements,testing concentrations of MoO42-and O2,and scanning electron microscopy (SEM)at conditions of standard prepared water,the mechanism of forming film on the surface was studied.The results indicate that molybdate corrosion inhibitor in alkaline water has corrosion inhibition,is an anodic type film forming agent;its forming film process is divided into three steps including induction period of 24 h,growing period of 48 h and stabilization period.And the higher MoO42-concentration,the denser membrane.In stabilization period,the suitable concentration is 100 mg/L;The crystal form of FeMoO4is like bamboo sticker in the growing period,and like maize in the stabilization period.
Molybdate ;Corrosion inhibitor;Mechanism of forming film;Standard prepared water
TQ050.9
A
1671-0460(2010)05-0501-05
2010-06-07
冉文斌(1972-),男,新疆克拉玛依人,助理工程师,2006年毕业于中国石油大学工商管理专业,一直从事石油化工专业工作,E-mail:xjklmyr@163.com。
马凤云(1955-),新疆哈密人,教授,硕士生导师。Tel:0991-4556660,E-mail:ma_fy@126.com。
图6 EDS谱图Fig.6 EDS spectrums
