丁二酸二乙酯与乙醇混合液密度和黏度的测定及关联
2010-08-28李娜王秀玲
李娜,王秀玲
(天津渤海职业技术学院,天津 300402)
丁二酸二乙酯与乙醇混合液密度和黏度的测定及关联
李娜,王秀玲
(天津渤海职业技术学院,天津 300402)
在常压下采用U形振动管密度计和乌氏黏度计分别测定了丁二酸二乙酯与乙醇的混合液在298.15~343.15K下的密度和黏度,并由密度数据和黏度数据分别计算出了不同温度和组成下的超额体积VE和超额黏度Δη;VE为正值,Δη为负值,同时分别将不同温度下的超额体积、超额黏度与组成的关系用Redlich-Kister方程进行了关联。
丁二酸二乙酯;乙醇;密度;黏度
丁二酸二乙酯是重要的合成香料和有机溶剂,测定丁二酸二乙酯和乙醇二元混合物系的粘度、密度数据具有重要的现实和理论价值。而目前丁二酸二乙酯和乙醇二元混合物系的粘度、密度测定还未见相关报道。
本文测定了丁二酸二乙酯和乙醇二元混合物系在298.15K~343.15K温度之间整个组成范围内的密度和黏度数据,分别计算出了超额摩尔体积和超额黏度,并用Redlich-Kister方程进行了回归。
1 试验部分
1.1 试验仪器和试剂
德国产BP210S电子天平;精度为0.01 s电子秒表;乌式黏度计;超级恒温水浴;日本产Density/Specific Gravity Meter DA-505型U型振动管密度仪。
丁二酸二乙酯(分析纯,含量为99.0%,天津市光复精细化工研究所);无水乙醇(分析纯,含量为99.5%,天津大学科威公司);环己烷(分析纯,含量为99.5%,天津大学科威公司)。
为了验证试验方法和仪器的准确性,同时检验试剂的纯度,测定了环己烷和乙醇在298.15 K和常压下的密度和黏度,与文献值进行了比较,其结果见表1。
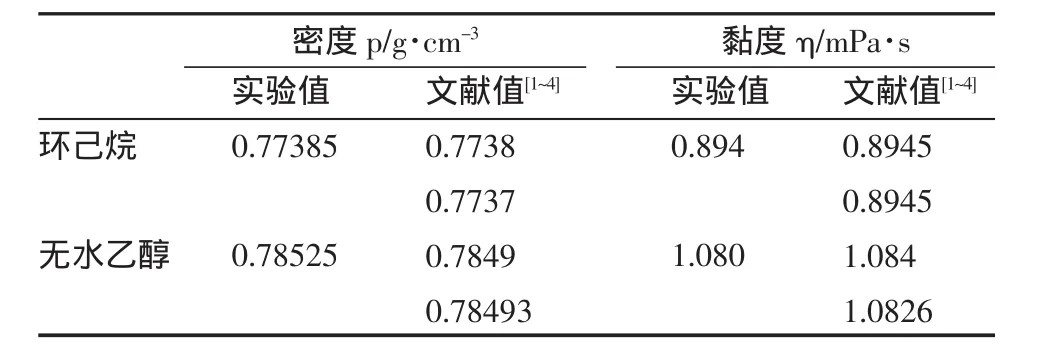
表1
由表1可知,环己烷和无水乙醇的试验值与文献值符合的较好,说明所用仪器和测定方法可靠。
1.2 溶液的配制
二元混合物通过容量瓶称重法配制,电子天平的精度为0.1 mg,在配制过程中首先称取所需量的丁二酸二乙酯,在不接触容量瓶的情况下,用注射器直接注入乙醇溶液,摇匀。摩尔分率的误差小于1×10-4。
1.3 密度的测定
本实验是通过U形振动管密度计来测定物系的密度。在测定过程中首先用去离子二次蒸馏水和干空气对密度计进行校正,测量池的温度读数精确到±0.01K,密度测量时仪器的误差为±1×10-5g·cm-3。
1.4 黏度的测定
利用乌式黏度计测量黏度,恒温水浴的温度通过数字控制仪表控制在±0.1K,然后再用精密温度计读取温度,精度为±0.01K,液体流过黏度计毛细管的时间通过精度为±0.01 s的电子数字秒表读取。每个数据点至少进行三次重复试验,每两次试验的差值不大于0.05 s,取三次测量的平均值作为最终试验结果。黏度的测量精度为±0.003 mPa·s。液体的黏度由下式进行计算:

其中,η、η0、ρ、ρ0和t、t0分别表示待测液与标准液的黏度(mPa·s)、密度(g·cm-3)和液体流过黏度计毛细管的时间(s)。
2 实验结果及讨论
丁二酸二乙酯与乙醇组成的混合液在不同组成和不同温度下的密度测量结果列于表2。
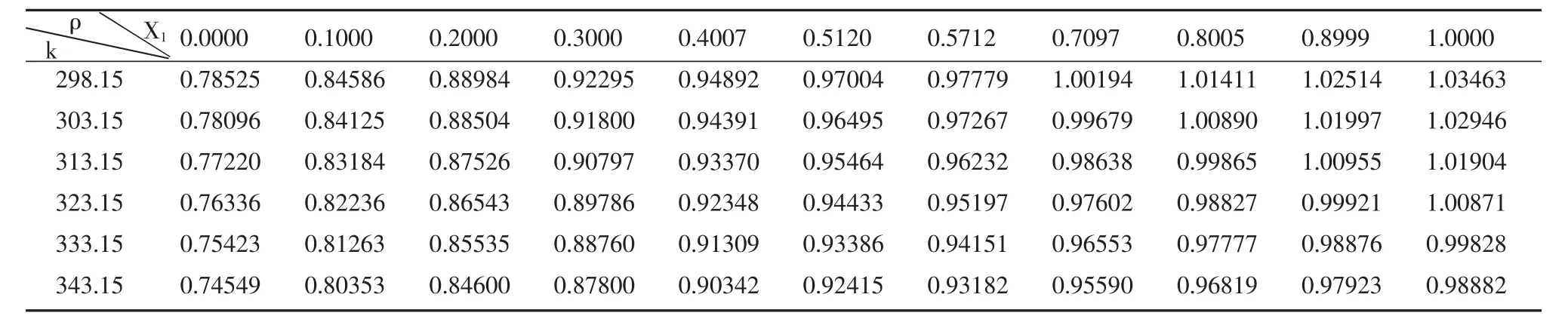
表2 混合溶液密度(g·cm-3)测定值
由表2可知,不同组成下的丁二酸二乙酯-乙醇混合液的密度随着温度的升高均匀下降,在各组成下的密度与温度呈很好的线性关系。
丁二酸二乙酯与乙醇混合液在不同组成和不同温度下的黏度测量结果列于表3。
由表3可以看出不同组成下的丁二酸二乙酯-乙醇混合液的黏度随着温度的升高呈明显的下降趋势,但并不与温度呈线性关系,且在同一温度不同组成下的黏度数据也不与丁二酸二乙酯的摩尔分数呈线性关系。

表3 黏度(mPa·s)测定值
利用密度数据可以通过下式计算超额摩尔体积[5]
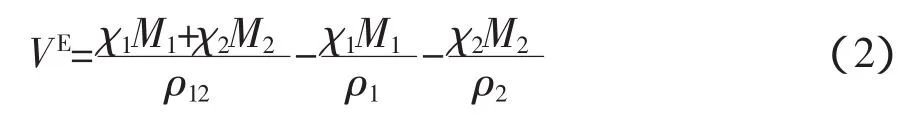
上式中χ1、M1、ρ1和χ2、M2、ρ2分别表示纯组分丁二酸二乙酯与乙醇的摩尔分数,摩尔质量(g·mol-1)和密度(g·cm-3),ρ12是溶液的密度,计算结果列于表4中。
不同温度下超额摩尔体积随组成的变化曲线如图1所示。
从图1可以看出对于丁二酸二乙酯和乙醇体系在所有组成范围内超额体积VE为正值,且在不同温度下的等温线都存在一极大值点,同时所有等温线的极值点基本聚集在x=0.57附近。不同温度下超额体积VE的变化趋势相似,呈开口向下的抛物线型,但在组成相同的情况下随着温度的增加超额体积VE的绝对值越来越大。
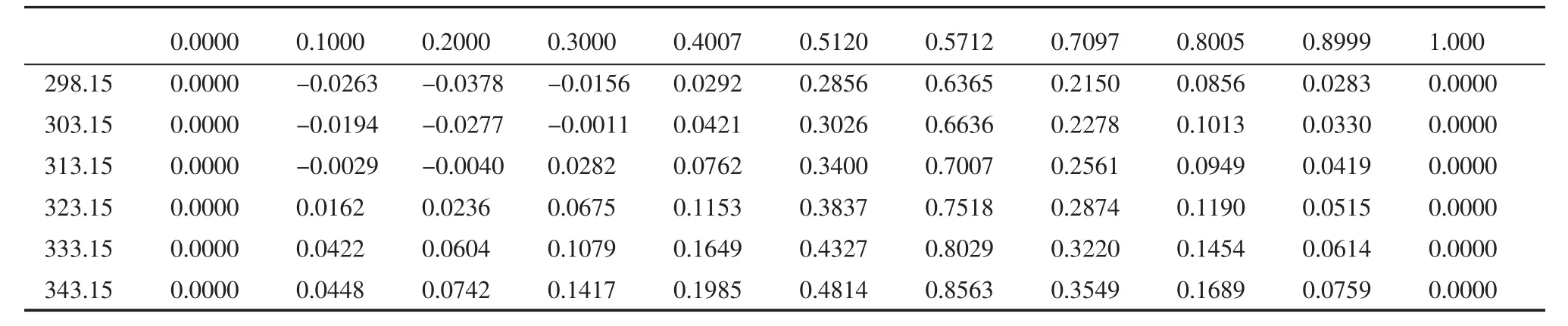
表4 不同温度及组成下的VE(cm3·mol-1)
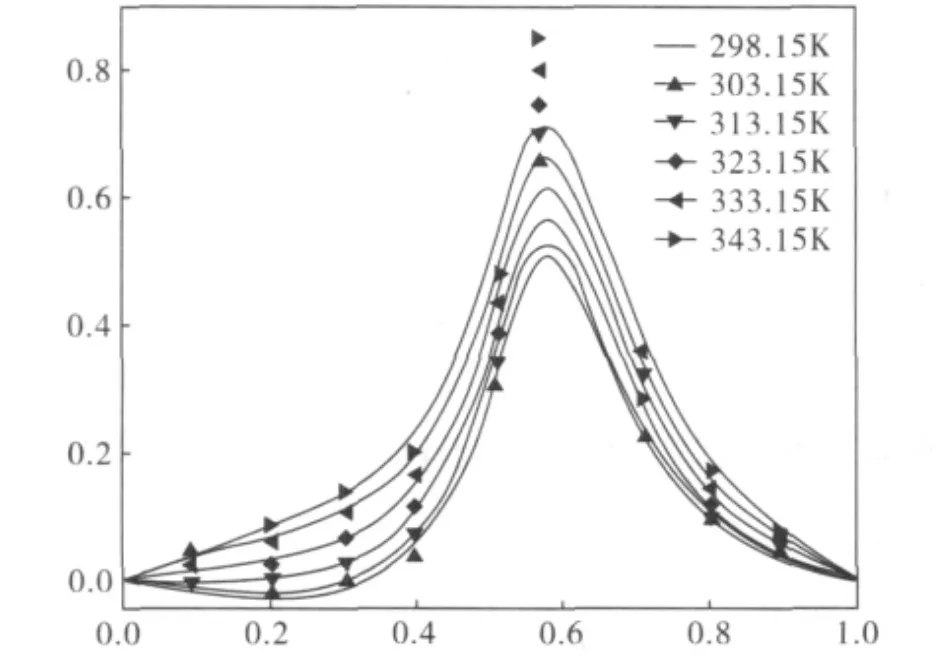
图1 不同温度下丁二酸二乙酯和乙醇溶液的x1-VE图
根据Redlich-Kister方程,超额摩尔体积VE按(3)式关联,其关联结果列于表5中。
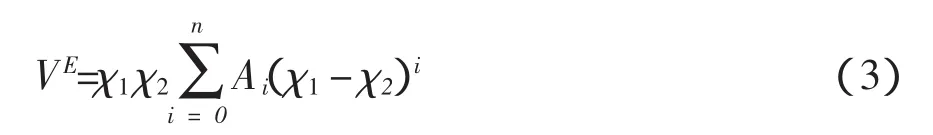
其中χ1、χ2分别表示丁二酸二乙酯和乙醇的摩尔分率,Ai是方程的回归系数。
平均误差和标准偏差SD分别由公式(4)和(5)计算而得。
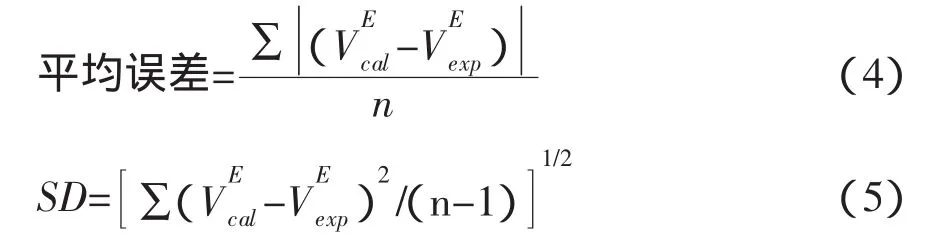
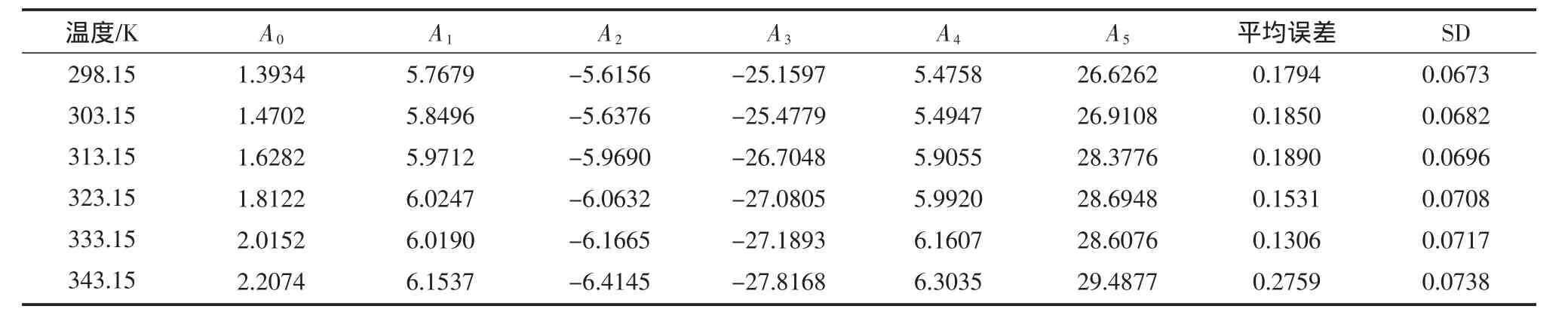
表5 VE按方程进行回归的系数及标准偏差
与超额体积的计算方法相似,溶液的黏度和按纯组份的黏度与摩尔分率计算的差即超额黏度由(6)式计算:

其中η、η1和η2分别表示混合液和纯物质1、2的黏度,两个体系对应的在不同温度下混合黏度的变化计算值列于表6,变化曲线于图2中。

表6 丁二酸二乙酯超额黏度
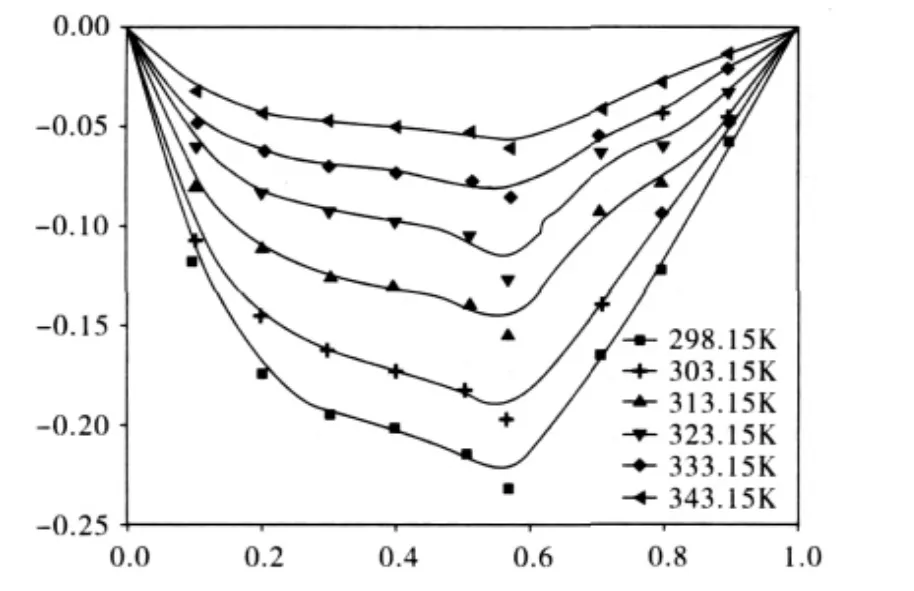
图2 不同温度下丁二酸二乙酯+乙醇溶液的χ1-Δη
由图2可以看出丁二酸二乙酯-乙醇这种二元体系的混合黏度的变化均为负值,且在同一组成下Δη的绝对值均随温度的升高而减小。
根据Redich-Kister方程,超额黏度Δη按(7)式进行回归,其回归结果列于表7中,表中的平均误差和标准偏差SD也分别由公式(4)和(5)计算而得和分别由Δηcal和Δηexp代替,Δη与组成的关联式为:

其中χ1、χ2分别表示丁二酸二乙酯和乙醇的摩尔分率,Ai是方程的回归系数。
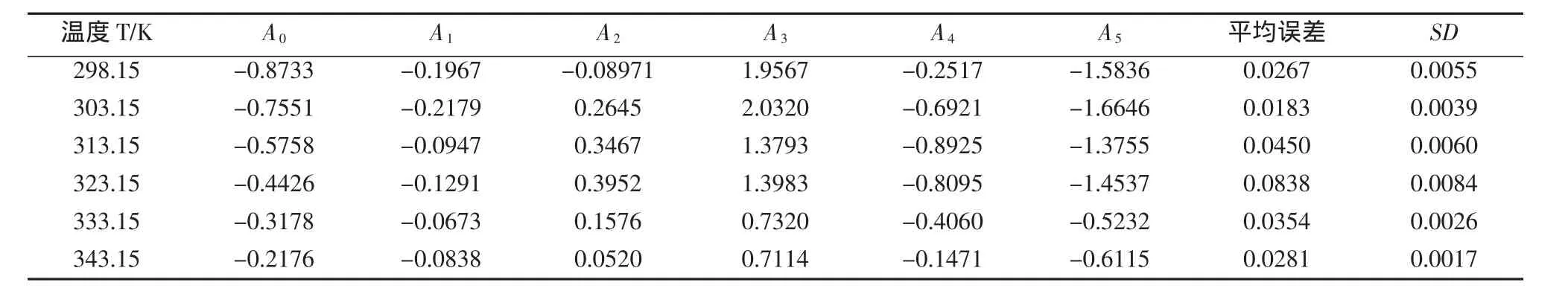
表7 丁二酸二乙酯-乙醇体系超额黏度Δη按Redlich-Kister方程进行回归的系数及标准偏差
3 结论
3.1 本文测定了丁二酸二乙酯-乙醇二元混合物系在不同温度及组成下的密度和黏度。
3.2 由密度数据计算出超额体积VE、由黏度数据计算出了超额黏度Δη。
3.3 对不同温度下的超额体积、超额黏度与组成的关系案Redlich-Kister方程进行关联,得出关联系数以及标准偏差。
[1] Kazuyoshi O,Katsutoshi T,Sachio M,Excess volumes and isentropic compressibilities of the binary mixtures of cyclohexanone with globular species at T=298.15K [J].J Chem Thermodynamics, 1997,29(3):287-294.
[2] Jagan N,Sanjay K M,Excess molar volumes and kinematic viscosities of binary liquid mixtures of cyclohexanone+dichloromethane,+ trichloromethane,+1,2-dichloroethane,+trichloroethene,+1,1,1-trichloroethane,and+cyclohexane[J].J Chem Eng Data,1998,43(2): 196-200.
[3] Vittalaprasad T.E.,Mythili R.,G.S.Nirmala,D.H.L.Prasad.Densities and Viscosities of Binary Mixtures of Chloroethylenes with Some Aliphatic Alcohols[J].J Chem Eng Data2002,47,68-71.
[4] Riddick,A.:Bunger,W.B.:Sakano,T.K.Organic Solvents,Physical Prop erties and Method of Purification[J].4th ed.,Wiley-Interscience: New York,1986.
[5] YawsCL,ChemicalPropertiesHandbook[M].Beijing:WordPublishing Corporation.1999.488.
Densities and Viscosities for diethyl succinate and ethanol at Diferent Temperatures
LI Na,WANG Xiu-ling
(Tianjin Bohai Technical Vocational Collgeg,Tianjin 300402,China)
The densities and viscosities were measured by a vibrating densimeter(model DA-505U)and a Ubbelohde suspended-level viscometer at atmospheric pressure for diethyl succinate+ethanol.The temperature rang was from 298.15K to 343.15K.Densities and viscosities of solutions were used to calculate excess molar volumes and excess viscosities respectively with Redlich-Kister Eq.
diethyl succinate;ethanol;density;viscosity
book=2010,ebook=71
10.3969/j.issn.1008.1267.02.008
TQ225.24+2
A
1008-1267(2010)02-0021-04
2009-10-20
