葛根提取物的快速提取工艺研究1)
2010-08-07赵景辉王再幸王英平赵伟刚周丽斯郭崇民张凤龙
赵景辉,王再幸,王英平,赵伟刚,周丽斯,郭崇民,张凤龙
(中国农业科学院特产研究所,吉林 吉林 132109)
葛根为豆科植物柴葛[Pueraria lobata(Willd.)Ohwi]和甘葛藤(Pueraria thomsonii Benth.)的干燥根,前者习称柴葛,甘葛藤习称“粉葛”[1],始载于《神农本草经》,味甘、辛,性平,具有增加脑及冠状动脉血流量、降低血管阻力、收缩平滑肌、降血糖及解热等多种功效[2]。民间用于治疗伤寒、温热头痛、烦热消渴等症,也是中医常用的祛风解毒药。现代研究表明,葛根含葛根异黄酮,主要为葛根素(perarin)、大豆苷(daidzin)、大豆苷元(daidzein)3种活性成分,其中葛根素是本属的特征成分,也是主要成分[3]其提取方法有冷浸、渗漉、超声、加热回流等,成本高、费时、费力,耗能巨大。本试验以葛根素和浸膏得率为指标,采用正交试验法优化高频电场提取工艺,具有快速、节能、低温提取等特点。
1 仪器与试药
1.1 实验材料
葛根购于吉林市药材站,经中国农业科学院特产研究所王英平研究员鉴定为柴葛[Pueraria lobata(Willd.)Oh wi]。
1.2 试药
葛根素对照品(中国药品生物制品检定所,含量测定用,批号110752-200511),甲醇为色谱纯,水为超纯水,其余试剂均为分析纯。
1.3 仪器
LDT-100/4-25.2型中药高压脉冲电场提取装置(长春华迪生物科技开发有限公司);OSB-2000旋转蒸发器(日本东京理化株式会社);电子天平ALC-210.4(Sartorius group);DZKW-D恒温数显水浴锅(河北黄骅市航天仪器厂);101-3C型烘箱(上海实验仪器厂);600 E高效液相色谱仪(美国Waters)。
2 方法与结果
2.1 单因素试验
溶剂浓度选择。本试验选择了水、50%乙醇、60%乙醇、70%乙醇、80%乙醇、90%乙醇等6种溶液为提取剂。以电场强度15kv/cm,脉冲数12个,料液比1∶10为提取参数。称取葛根干品,粉碎至100目,分别称取100 g,加入不同浓度的提取液浸湿、混匀,用泵将样液打入中药高压脉冲电场提取装置中进行提取,所得提取液过滤后减压浓缩至100m L,取2 m L用HPLC检测葛根素含量,其他真空干燥至恒重,计算浸膏得率。结果见表1。经比较可以看出以60%乙醇作为提取液,葛根素的得率最高。因此确定60%乙醇溶液为最佳提取剂。
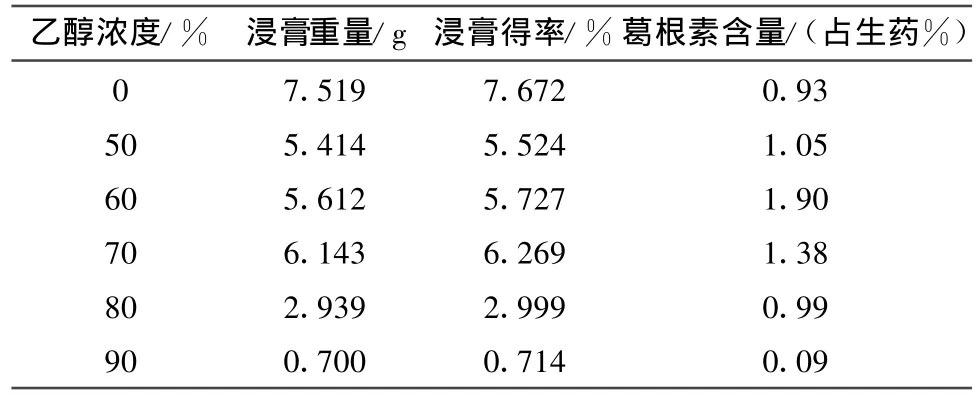
表1 乙醇浓度的影响
2.2 正交实验
2.2.1 因素水平设计。由于是连续流动进样提取,不考虑提取温度、提取时间和提取次数的影响;又因为流速与脉冲数成相关,所以影响提取的因素主要有:电场强度、脉冲数、料液比。采用L9(34)正交表优化提取条件,重点考察上述三个因素,以浸膏得率和葛根素为考察指标,见表2。
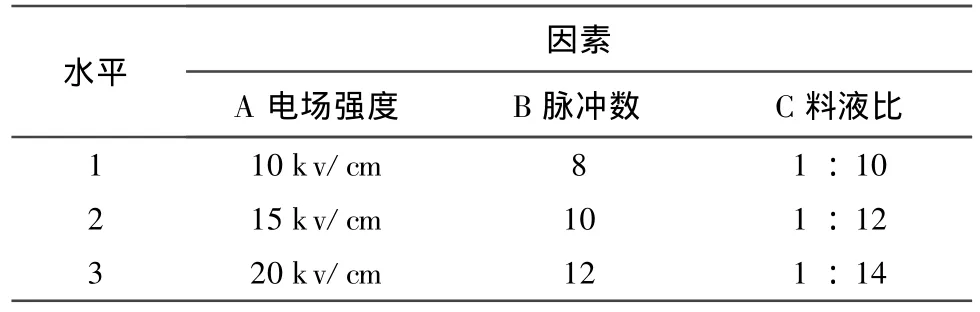
表2 L9(34)实验因素水平表
2.2.2 样品制备。取葛根80目干品,分别称取100 g,按L9(34)正交表所列实验因素和实验水平进行试验,所得提取液过滤后减压浓缩至100m L,取2 m L用HPLC检测葛根素含量,其他真空干燥至恒重,计算浸膏得率,见表3。
2.2.3 含量测定
2.2.3.1 色谱条件。色谱柱:Agilent Hypersil ODS,5μm,4.6×200mm;柱温:25℃;流动相:甲醇-水(27 ∶73);流速:1.0m L/min;检测波长:250nm;进样量10μL 。
2.2.3.2 对照品溶液的制备。精密称取葛根素对照品0.41mg,置5m L的容量瓶中,加30%的乙醇溶解,并定容至刻度,摇匀,即得。
2.2.3.3 供试品溶液的制备。葛根不同浓度的乙醇提取液2m L,分别用30%的乙醇溶解,转移至100m L的容量瓶中,用30%的乙醇定容至刻度,再从中吸取1~10m L的容量瓶中,用 30%的乙醇定容至刻度,摇匀,即得。
2.2.3.4 线性关系的考察。分别精密吸取对照品溶液0.1、0.3、0.5、0.7、1m L,置 5 个 1m L 的容量瓶中,加30%的乙醇定容至刻度,摇匀,备用。分别精密吸取上述浓度的溶液10μL,注入高效液相色谱仪检测,记录色谱图及峰面积。以葛根素对照品进样量为横坐标,色谱峰面积为纵坐标,绘制标准曲线。结果表明葛根素在0.0082~0.082μg范围内呈良好的线性关系。
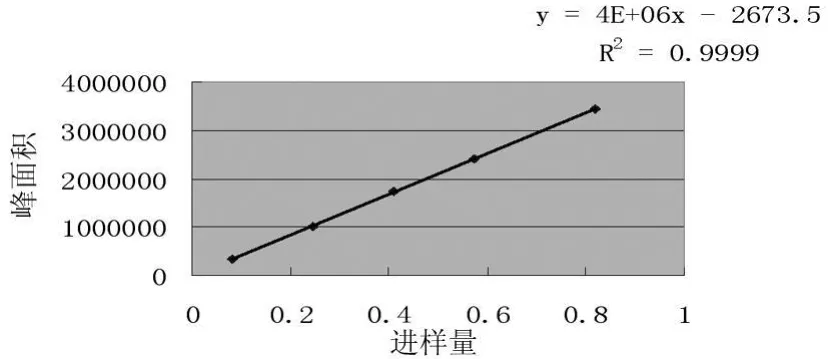
图1 葛根标准曲线
2.2.3.5 样品的测定。分别精密吸取葛根不同浓度乙醇提取液各10μL,注入高效液相色谱仪,测定峰面积,按外标法计算各提取液中葛根素的含量。结果见表 1,表3。
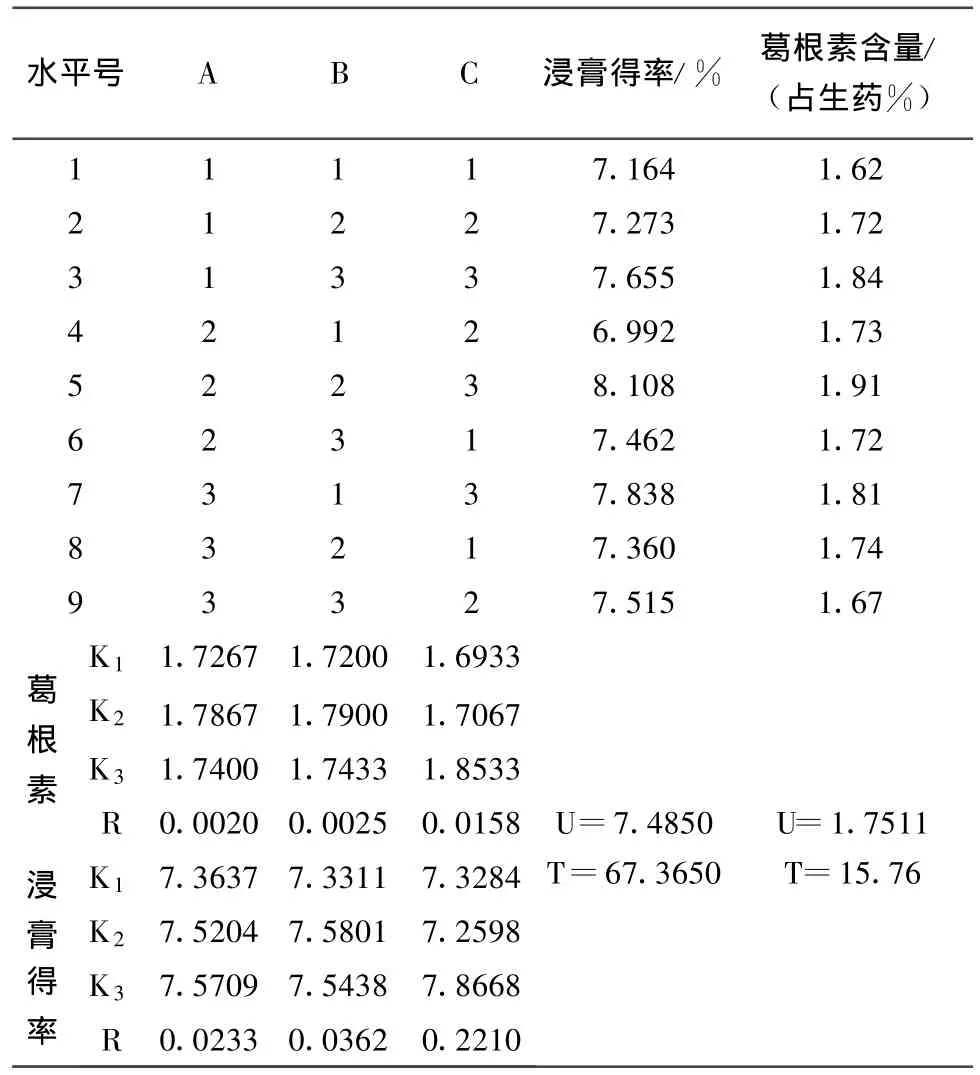
表3 L 9(34)正交实验结果
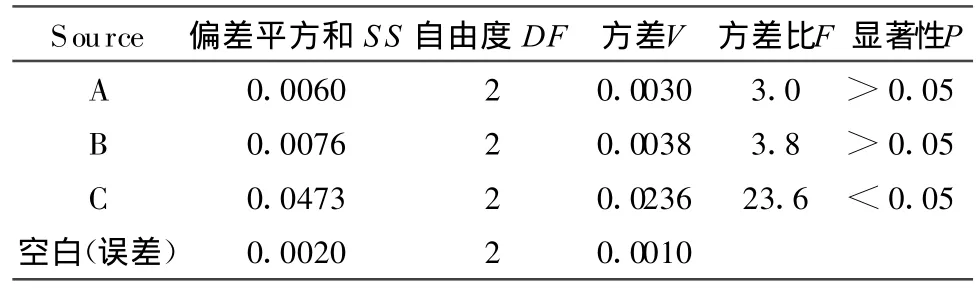
表4 葛根素正交实验结果与分析

表5 葛根浸膏得率正交实验结果与分析
经过表3、表4、表5的直观分析、方差分析和显著性检验结果表明:影响葛根素提取的主次因素为C>B>A,即料液比>脉冲数>电场强度。最佳提取工艺为A2B2C3,即电场强度15 kv/cm,脉冲数为 10,料液比1∶14。影响葛根浸膏得率的主次因素为C>B>A,即料液比 >脉冲数>电场强度。最佳提取工艺为A3B2C3,即电场强度20 kv/cm,脉冲数为10,料液比1∶14。方差分析可知,料液比对提取葛根素和葛根浸膏得率有显著影响;电场强度、脉冲数对提取葛根素和葛根浸膏得率均无显著影响。
由于A3B2C3组合并不在上述的正交试验设计里,需另做一组正交试验加以验证。
2.2.4 提取工艺试验验证。取葛根干品,粉碎至100目,分别称取100 g,按A3B2C3组合进行试验,所得提取液过滤后减压浓缩至100m L,真空干燥至恒重,计算浸膏得率。重复验证试验(n=3),葛根浸膏得率为8.32%(占生药),RSD=1.38%。
结果显示:采用此方法提取,3次实验结果中葛根浸膏得率均无明显变化。
3 讨论
本方法利用调制的高频电流直接作用生物质材料,使材料分子产生震荡,激发了生物分子活性,使有效成分快速溶解在溶剂中。这种新的提取技术省略了一般提取时所需要的能量交换,能量传导过程,提取所需要能量直接做功在生物分子上,因此比较其他提取方法节能50%以上。
国外自20世纪初开始利用高压电场对牛奶进行灭菌,以后逐渐发展到对各种食品灭菌[4]。进入21世纪,我国科技工作者将此技术应用于中药提取,并取得一定进展。该技术用于葛根有效成分提取,具有提取时间短,1s以内;常温提取,对葛根活性成分及风味无影响;处理均匀,在电场中各部分的物料均受到相同大小场强的处理(电极边缘除外);耗能小,对环境无污染等优点。但是,应当根据需求采取不同的工艺参数,若想得到大量提取物应当以电场强度20 kv/cm,脉冲数为10,料液比1∶14的参数进行提取;如果以葛根素为目标物则以电场强度15 kv/cm,脉冲数为10,料液比1∶14为参数进行提取。
该方法稳定、可行、适用于工业化生产,可作为葛根的快速提取工艺。
[1]朱丽华,贺浪冲.葛根中有效部位及有效成分的高效液相色谱分析[J].西安交通大学学报(医学版),2005,26(3):216.
[2]张妤琳,梁敬钰.葛根素的研究进展[J].海峡药学,2005,17(1):2.
[3]王言才,段金廒,华永庆,等.不同品种葛根中葛根素及总黄酮的含量测定[J].时珍国医国药 2008,19(1):132-133.
[4]曾新安,陈勇.脉冲电场非热灭菌技术.1版[M].中国轻工业出版社,2005.
