双氯芬酸钠乳膏的微生物限度检查方法验证试验研究
2010-07-31林小毅
郑 笠,林小毅
(福建省福州市药品检验所,福建福州 350007)
双氯芬酸钠乳膏为乳剂型基质的类白色乳膏,在建立双氯芬酸钠乳膏的微生物限度检查方法时应进行方法验证,选择正确的方法降低或消除该药品抑菌作用对试验的干扰,以证明所采用的方法适合于该药品细菌、霉菌和酵母菌数的测定及控制菌的检查。因此,笔者采用《中国药典》2005年版一部附录微生物限度检查法项下方法建立伤痛宁膏的细菌、霉菌和酵母菌及控制菌的检查方法并验证。
1 仪器与试药
1.1 试验环境
在环境洁净度万级、局部洁净度百级的单向流空气的无菌室中进行。
1.2 样品
双氯芬酸钠乳膏由福州某药业有限公司提供。
1.3 验证菌种
枯草杆菌[CMCC(B)63501]、金黄色葡萄球菌[CMCC(B)26003]、大肠埃希菌[CMCC(B)44102]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]、铜绿假单胞菌[CMCC (B)10104]均由中国药品生物制品检定所提供。
1.4 稀释液
pH=7.0无菌氯化钠-蛋白胨缓冲液(批号:091217,福州市药品检验所菌检室)。
1.5 仪器
SW-GJ-1BU标准型洁净工作台、YXQ-LS-50S数显立式压力蒸汽灭菌器、SHP-250生化培养箱、MJX-250BZ霉菌培养箱。
1.6 培养基
干粉:营养琼脂培养基(批号:080304),玫瑰红钠琼脂培养基(批号:081217),营养肉汤培养基(批号:081119),胆盐乳糖培养基(批号:081210),甘露醇氯化钠琼脂培养基(批号:080628),溴化十六烷基三甲胺琼脂培养基(批号:091107),改良马丁琼脂培养基(批号:081031),改良马丁培养基(批号:090307)均由北京三药科技开发公司提供。
2 方法与结果
2.1 菌液制备
取经37℃培养18~24 h的金黄色葡萄球菌、铜绿假单胞菌、大肠埃希菌、枯草杆菌肉汤培养物1 ml加9 ml 0.9%无菌氯化钠溶液逐管 10 倍稀释至 10-5~10-7,为 50~100 cfu/ml,备用;取经25℃培养48~72 h的白色念珠菌液体培养物1 ml加9 ml 0.9%无菌氯化钠溶液逐管10倍稀释至10-5~10-7,为50~100 cfu/ml,备用;取经25℃培养1周的黑曲霉斜面培养物,加3~5 ml盐水洗下霉菌孢子,吸取出菌液,取1 ml加9 ml 0.9%无菌氯化钠溶液逐管10倍稀释为10-4,为50~100 cfu/ml,备用。
2.2 供试品溶液制备
取本品5 g,与5 g司盘80、3 g单硬脂酸甘油酯、5 g聚山梨酯80混合于无菌烧杯中,用无菌玻棒搅拌成团后,慢慢加入45℃的pH=7.0无菌氯化钠蛋白胨缓冲液至100 ml,边加边搅拌,使供试品充分乳化,作为1∶20供试品溶液。
2.3 细菌、霉菌和酵母菌检查法的验证
2.3.1 常规法 采用常规法进行3次独立的平行实验,每种菌液做平行2皿。
2.3.2 菌液组 分别取枯草杆菌、金黄色葡萄球菌、大肠埃希菌3种菌液各1 ml,注入培养皿中,然后注入45℃营养琼脂培养基约 15 ml,待凝固后,置 30~35℃培养 24~48 h,逐日观察结果。分别取白色念珠菌、黑曲霉2种菌液各1 ml,注入培养皿中,然后注入45℃改良马丁琼脂培养基约15 ml,待凝固后,置 23~28℃培养 48~72 h,逐日观察结果。
2.3.3 供试品对照组 取本品1∶20供试品溶液1 ml,倾注琼脂培养基,待凝固后,置规定温度培养24~72 h,逐日观察结果,测定供试品本底菌数。
2.3.4 试验组 取本品 1∶20供试品溶液 1 ml、50~100 cfu/ml试验菌液1 ml,分别注入平皿中,倾注琼脂培养基,待凝固后,置规定温度培养24~72 h,逐日观察结果。
2.3.5 稀释剂对照组 取稀释剂1 ml、50~100 cfu/ml试验菌液1 ml,分别加入平皿中,倾注琼脂培养基,待凝固后,置规定温度培养24~72 h,逐日观察结果。
2.3.6 实验结果 见表1。由表1可知,经3次平行试验,结果试验组及稀释剂对照组的5种阳性试验菌株的回收率均大于70%,因此可采用常规法测定该供试品的细菌数、霉菌和酵母菌数。
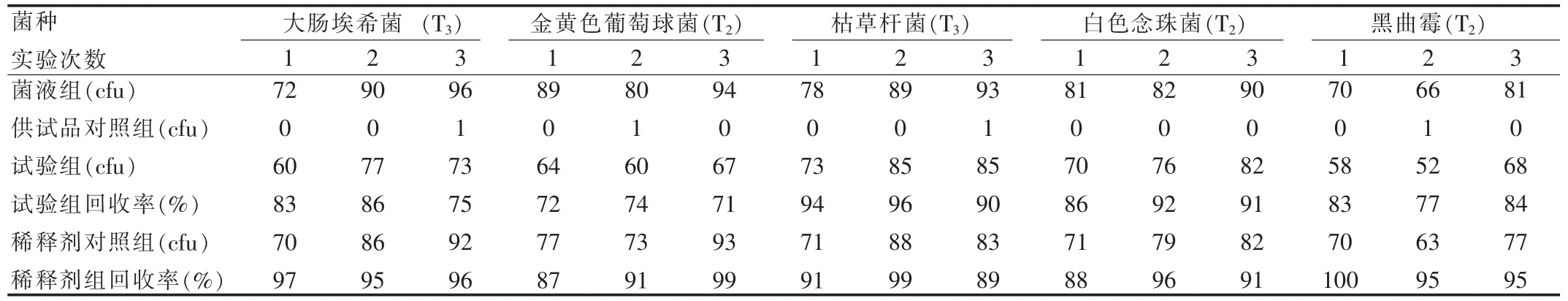
表1 细菌、霉菌和酵母菌常规法平皿计数方法的验证
2.4 控制菌检查方法验证
2.4.1 试验组 取1∶20的供试品溶液 20 ml及 10~100 cfu试验菌加入增菌培养基中,依相应控制菌检查法检查。
2.4.2 阴性菌对照组 取1∶20的供试品溶液20 ml及10~100 cfu的阴性对照菌,加入增菌培养基中,依相应控制菌检查法检查,阴性对照菌不得检出。
2.4.3 阳性对照组 取10~100 cfu的阳性对照菌加入增菌培养基中,依相应控制菌检查法检查,阳性对照试验应检出相应的控制菌。
2.4.4 阴性对照组 取稀释剂20 ml加入控制菌检查用的增菌培养基中,培养,应无菌生长。
2.4.5 本底对照组 取1∶20的供试液20 ml加入增菌培养基中,依相应控制菌检查法进行检查。
2.4.6 实验结果 见表2、3。

表2 金黄色葡萄球菌验证试验结果

表3 铜绿假单胞菌验证试验结果
由表2验证试验可知,金黄色葡萄球菌(试验组100 ml、200 ml营养肉汤增菌培养基经培养后划线于甘露醇氯化钠琼脂平板均未检出,营养肉汤增菌培养基至300 ml经培养后划平板检出),因此采用培养基稀释法依法检查。表3验证试验结果可知,铜绿假单胞菌各组生长良好,阴性菌无生长,可采用常规法检查。
3 讨论
由试验结果可以看出,试验组及稀释剂对照组的试验菌株的回收率均大于70%,因此可采用常规法测定该供试品的细菌数、霉菌和酵母菌数。控制菌金黄色葡萄球菌应采用培养基稀释法检查、铜绿假单胞菌采用常规法依法检查。
稀释剂对照组用以评价供试品溶液制备方法对微生物的影响,本次试验稀释剂对照组的回收率均大于70%,说明采用pH=7.0无菌氯化钠-蛋白胨缓冲液作为稀释液对试验不产生干扰。
精确测定菌数是回收率测定最为关键的步骤,为减少操作误差,一般应取每毫升含菌 50~100 cfu的菌液1 ml进行验证实验。
验证试验进行3次独立平行试验,倾注培养基时每次试验各平皿所加的培养基体积应尽量保持一致,注入后快速转动平皿使供试品溶液与培养基混匀,以使回收试验结果重现性良好。
双氯芬酸钠乳膏为非水溶性供试品,为使其充分乳化溶解,先将供试品5 g置无菌烧杯中,再加入适量的单硬脂酸甘油酯、司盘80,聚山梨酯80用无菌玻棒搅拌有利于分散均匀,再慢慢加入45℃的pH=7.0无菌氯化钠-蛋白胨缓冲液至100 ml,边加边搅拌,使其成为均匀的乳液。
[1]国家药典委员会.中国药典[S].一部.北京:化学工业出版社,2005.
[2]苏德模,马绪荣.药品微生物学检验技术[M].北京:华龄出版社,2007:1.
[3]解翠珠.银黄颗粒微生物检查方法学验证[J].海峡药学,2007,19(11):56-57.
[4]戴慧雯,杨丽娜.无极膏微生物限度检查法的验证[J].海峡药学,2007,19(6):59-60.
[5]周建平.药剂学进展[M].南京:江苏科学技术出版社,2008:6.
[6]中国药品生物制品检定所.中国药品检验标准操作规范[S].北京:中国医药科技出版社,2005:313.
[7]钱之玉.药理学进展[M].南京:东南大学出版社,2005:5.
[8]刘兴兰,王灿,文晓玲.药品检验菌种的保藏方法[J].中国药事,2007,21(4):43.
