老年钙化性心脏瓣膜病临床分析
2010-06-19刘立新赵玉生武云涛万晓荆
刘立新,赵玉生,武云涛,陈 瑞,万晓荆
钙化性心脏瓣膜病(calcific valvular heart disease,CVHD)是老年人常见的一种随增龄发病增多、病程加重的退行性疾病。其由瓣膜组织的老化、退行性改变、纤维化及钙盐沉积所致,可伴有单个或多个瓣膜功能异常。目前钙化性主动脉瓣狭窄已成为国外老龄患者外科换瓣或经皮瓣膜支架置换术的主要病因[1]。笔者回顾分析了230例经超声心动图诊断为CVHD的住院患者临床资料,探讨可能的发病情况及临床特点。
1 资料与方法
1.1 研究对象 选择2000-2007年期间,在解放军总医院老年病区、北京军区总医院干部病房住院、资料较全且经超声心动图诊断为CVHD的患者共计230例,其中男145例,女85例,年龄60~103岁(72±9)岁。
1.2 研究方法 采用 HP GElogiq-500、HP SONOS 1000、Acuson Sequoia 512彩色多普勒超声诊断仪检查,选用胸骨旁长轴、短轴切面及心尖四腔、五腔切面,观察各瓣膜厚度、回声及活动度,明确钙化灶形态、位置,同时观察各心腔的大小、室壁厚度,计算左室射血分数;借助彩色多普勒观察各瓣口有无射血及反流。诊断标准:(1)>60岁患者;(2)超声心动图显示瓣膜局限性增厚(>3 mm)、僵化,回声反射明显增强(超过主动脉根部后壁回声),病变主要累及瓣环、瓣膜基底部或瓣体,而无瓣叶间黏连融合及瓣叶边缘变形;(3)排除其他原因所致的瓣膜病变,如风湿热、梅毒、胶原病、先天性心脏病、感染性心内膜炎和瓣膜置换术后及瓣膜创伤等。
1.3 临床指标 收集患者的主要临床资料,记录超声心动图、胸部X线、心电图及(或)动态心电图主要结果和相关生化指标,如总胆固醇、高密度脂蛋白、低密度脂蛋白、甘油三酯、血钙、血磷、血碱性磷酸酶水平。
2 结 果
2.1 临床表现 患者主诉胸痛、胸闷、呼吸困难、乏力有183例(79.6%),心悸、停搏感 28例(12.2%),晕厥、黑朦3例,无明显不适者22例。体检时,51.3%患者可于心尖部闻及1~3/6级收缩期杂音,22.2%于主动脉瓣听诊区闻及 1~3/6级收缩期杂音,5.2%于主动脉瓣区闻及轻至中度舒张期杂音;7例出现周围血管征,此外,6例闻及S4,4例闻及S3。
2.2 伴发疾病 70%患者伴发高血压病,60%伴发冠心病,28.7%伴发糖尿病,14.8%伴发高脂血症,18.7%伴发脑卒中,23.5%伴发心功能不全,16.1%伴发慢性阻塞性肺病;其他疾病还包括肿瘤、周围血管病等。
2.3 瓣膜受累情况 全部患者共检出203例主动脉瓣钙化(88.3%)、89例二尖瓣钙化(38.7%)、9例三尖瓣钙化和肺动脉瓣钙化(3.9%)。病变部位以单纯主动脉瓣钙化最多,达到139例(60.4%),其次为主动脉瓣合并二尖瓣钙化52例(22.6%),再次为单纯二尖瓣钙化26例(11.3%);未见单纯性三尖瓣、肺动脉瓣钙化,各有9例与主动脉瓣及(或)二尖瓣钙化同时发生。主动脉瓣钙化中,以无冠瓣受累率最高(88.3%),其后分别为右冠瓣(36.2%)和左冠瓣(24.5%)。二尖瓣钙化中,前叶、后叶受累相似,分别为62.1%和63.6%。各年龄组及性别的瓣膜受累情况见表1,2,其中主动脉瓣钙化检出率存在年龄差异性(P<0.05),而二尖瓣钙化检出率女性多于男性(P<0.05)。
2.4 受累瓣膜功能状况 根据彩色多普勒测定,203例主动脉瓣钙化者共检出单纯主动脉瓣反流89例(43.8%),主动脉瓣反流+主动脉瓣狭窄20例(9.9%),单纯主动脉瓣狭窄8例(3.9%)。28例主mm。*P <0.05动脉瓣狭窄患者有6例为中、重度狭窄。89例二尖瓣钙化者共检出单纯二尖瓣反流42例(47.2%),轻度二尖瓣狭窄1例(1.1%),轻度二尖瓣狭窄+二尖瓣反流1例(1.1%)。9例三尖瓣及肺动脉瓣钙化中未发现狭窄改变,各有8例合并轻、中度反流(88.9%)。
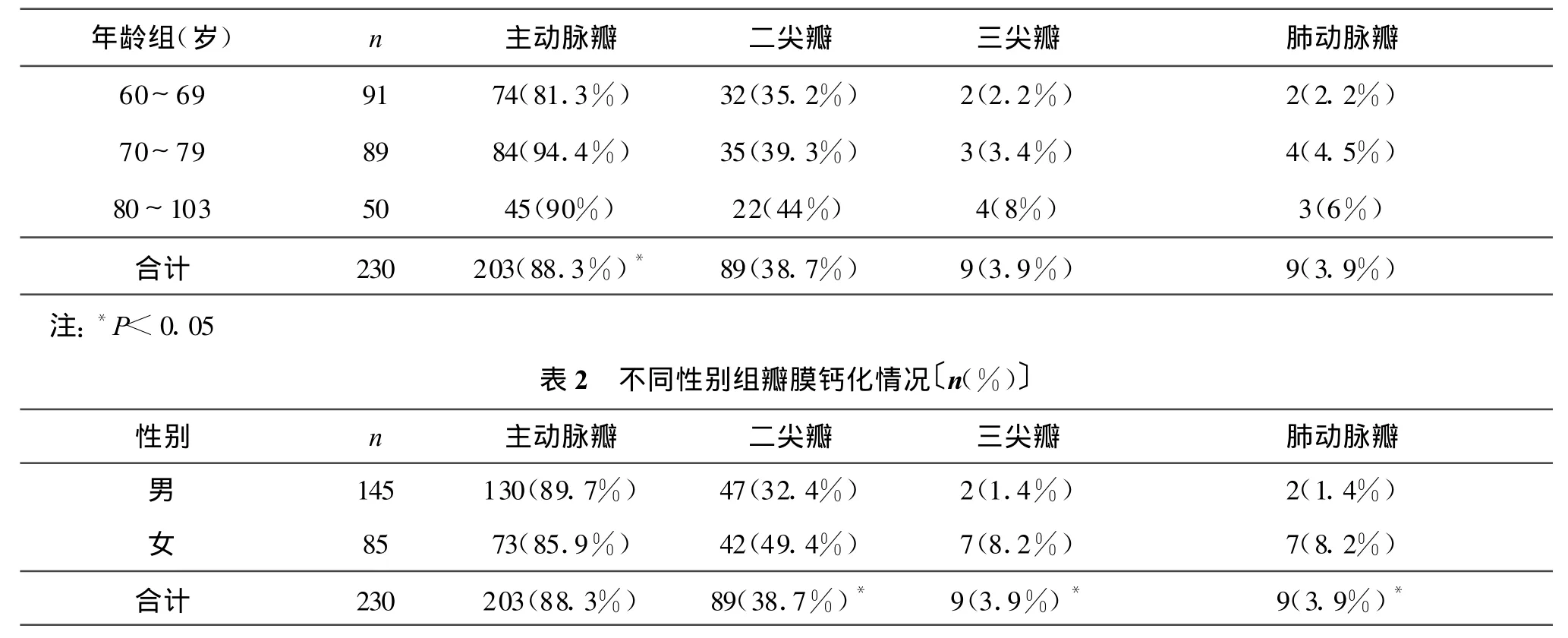
表1 不同年龄组瓣膜钙化情况〔n(%)〕
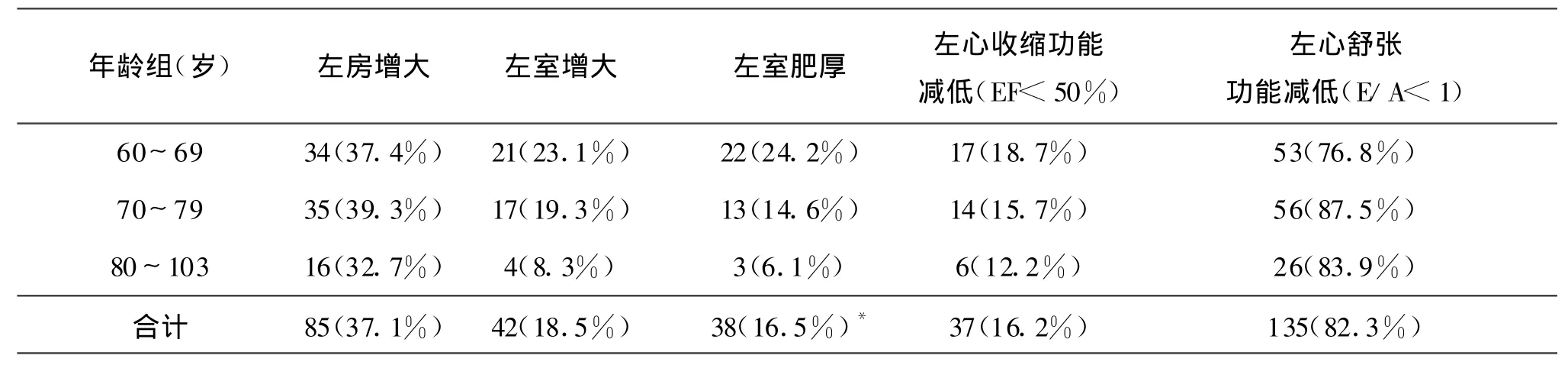
表3 不同年龄组左房、左室内径扩大和左室壁增厚情况〔n(%)〕
2.5 心脏形态及功能 不同年龄组心脏形态的改变情况见表3。心脏异常检出率依次为左心舒张功减低(82.3%)、左房增大(37.1%)、左室增大(18.5%)、左室肥厚(16.5%)和收缩功能减低(16.2%),其中左室肥厚检出率具有显著年龄差异(P<0.05),随增龄而减少。全体患者共检出左心扩大者96例,包括单纯左房扩大54例、左房和左室同时扩大31例、单纯左室扩大11例;其中合并左室舒张功能减低者40例,收缩功能减低者29例。
2.6 胸部X线检查 心脏扩大者56例(24.3%),主动脉弓钙化者165例(71.7%),冠状动脉钙化者5例(2.2%),未发现瓣膜钙化影。
2.7 心电图及动态心电图检查 共检出各类心律失常155例(67.4%),65.5%并存两种以上的心律失常,依次为各种期前收缩96例(41.7%)、心房颤动47例(20.4%)、房室传导阻滞37例(16.1%)、室上性心动过速 36例(15.7%)、束支阻滞 34例(14.8%)、心房扑动 33例(14.3%)、病窦综合症13例(5.7%)、室性心动过速 7例(3.0%),有19例安装了永久起搏器(8.3%)。多数患者心电图伴有ST-T改变,平均心率为(73±13)次/min,PR间期为(171±35)ms,QTc间期(423±35)ms,其中QTc间延长(>440 ms)55例,左心室肥大53例,PtfV1>0.04mm·s 23例。
2.8 生化指标 共检出血脂异常144例(62.6%),其中甘油三酯 ≥1.70 mmol/L者 77例(33.5%),总胆固醇 ≥5.18 mmol/L者 67例(29.1%),高密度脂蛋白<1.04 mmol/L者 61例(26.5%),低密度脂蛋白≥3.37 mmol/L者45例(19.6%)。血碱性磷酸酶平均为(78±33)U/L,血钙为(2.4±0.4)mmol/L,血磷为(1.2±0.5)mmol/L,均在正常范围内。
3 讨 论
CVHD是随增龄而发生、老年人特有的一种瓣膜病变。欧洲瓣膜疾病心脏调查[2]显示,CVHD约占全体主动脉瓣狭窄的81.9%,主动脉瓣反流50.3%,二尖瓣狭窄 12.5%,二尖瓣反流61.3%。国内刘丽等[3]所统计的北京地区军队老年人群CVHD患病率约为13.4%,并随年龄而增加,到80岁以上时已升至25.7%。目前对于CVHD确切发病机制尚不清楚,很可能是一种多因素参与、被动和主动交替出现的过程,其病理生理基础与动脉粥样硬化钙化相似,包含了基膜破裂、巨噬细胞和T淋巴细胞迁移、脂质渗透及钙盐沉积等过程[4]。临床研究也已证实二尖瓣环或主动脉瓣钙化与冠心病密切相关,CVHD的冠心病发病率更高、冠状动脉病变程度更重,并且可作为预测冠心病发病和病变程度的独立因素[5,6]。本组中,CVHD患者冠心病检出率高达60%,而高血压病、糖尿病检出率分别达到70%、28.7%,并且62.6%患者存在血脂异常,但血钙、磷和碱性磷酸酶水平等骨代谢指标却未见异常。高血压病、糖尿病和高脂血症均为动脉粥样硬化重要危险因素,也是CVHD易患因素[3]。高血压病时,瓣膜所受血流冲击力大,容易出现瓣膜损伤,诱导钙化和狭窄;而血糖、血脂升高则能明显增加患者血液黏稠度,加重全身和局部炎症反应,导致脂质沉积于瓣环、瓣膜内膜,诱发或加重钙化。
CVHD可引起瓣膜反流甚至狭窄,导致左心室肥厚、增大和功能异常。本组中,钙化主要累及主动脉瓣、二尖瓣,其中以主动脉瓣受累最常见,其次为主动脉瓣和二尖瓣同时受累,并未发现三尖瓣和肺动脉瓣单独受累。这可能与左心系统瓣膜所承受的机械应力更高有关,其中主动脉瓣所承受的冲击力、剪切力变化最大,也更易出现瓣膜表面受损、胶原纤维断裂,发生慢性炎症反应和钙盐沉积[7]。主动脉瓣叶以无冠瓣受累最多,可能与无冠窦内没有冠脉开口,无法分流应力,致使血液在无冠瓣与主动脉瓣环后缘连接处容易形成涡旋,损伤瓣叶。CHVD时,无论主动脉瓣还是二尖瓣钙化,多以关闭不全为主,本组钙化性主动脉狭窄发病率仅为12.3%,二尖瓣狭窄仅为2例。瓣膜关闭不全发生可能与钙化瓣膜缩短、瓣环僵硬或扩大等有关,其能导致左心容量负荷过重时左室明显扩张,甚至诱发左心衰竭,并且主动脉瓣反流时,由于减少舒张期冠脉供血不足,还能诱发心肌缺血。本组中,各类左心扩张、心肌肥厚和心功能异常并不少见,但由于多数患者合并高血压病、冠心病或慢性阻塞性肺病,在病因分析中很难明确仅与瓣膜钙化有关。
本组CVHD临床症状缺乏特异性,多与并发症及伴发疾病有关,但心脏听诊有助于早期识别,多数患者心尖部或主动脉瓣区可闻及收缩期杂音,少数出现舒张期杂音。X线检查时,71.7%患者检出主动脉弓钙化,少数合并有冠脉钙化,提示主动脉弓钙化有助于预测瓣膜钙化。Allison等[8]借助电子束CT曾观察过1242例无症状的非冠心病患者,发现胸、腹主动脉钙化与二尖瓣环、主动脉瓣环钙化显著相关,从而证实动脉粥样硬化性钙化与瓣膜钙化相关。另外,本组所检出的心律失常以快速性房性心律失常和缓慢性心律失常为主,这是因为CVHD患者常合并二尖瓣反流,致使左房压力增高、左房扩张,容易诱发房性心律失常。如本组心房颤动、心房扑动检出率分别为20.4%和14.3%。此外,钙化还能波及各级传导系统,诱发各种传导阻滞和束支阻滞等,如本组房室传导阻滞、束支阻滞检出率分别达到16.1%和14.8%。
目前临床上尚缺乏对CVHD的充分重视,NHLBI研究[9]已证实,无论社区还是整个人口,合并瓣膜疾病的校正后死亡风险均会显著升高,提示早期识别该病对于改善患者预后非常重要,而超声心动图已被认为是唯一可充分评估瓣膜疾病分布和发病的有效手段。借助超声心动图,能够鉴别风湿性、先天性或其他原因所致的瓣膜病变,判断瓣膜钙化的部位、大小,并能及时发现血流动力学、心脏功能的改变,因此是目前诊断评估CVHD的最灵敏、最可靠的检查。
[1]Wong MC,Clark DJ,Horrigan MC,et al.Advances in percutaneous treatment for adult valvular heart disease[J].Intern Med J,2009,39(7):465-474.
[2]Iung B,Baron G,Butchart EG,et al.A prospective survey of patients with valvular heart disease in Europe:The Euro Heart Survey on Valvular Heart Disease[J].Eur Heart J,2003,24(13):1231-1243.
[3]刘 丽,赵玉生,王士雯,等.北京地区军队老年人群退行性心脏瓣膜病流行病学研究[J].中华流行病学杂志,2006,26(10):836-839.
[4]Goldbarg SH,Elmariah S,Miller M A,etal.Insights into degenerative aortic valve disease[J].J Am Coll Cardiol,2007,50(13):1205-1213.
[5]Acarturk E,Bozkurt A,Cayli M,et al.Mitral annular calcification and aortic valve calcification may help in predicting significant coronary artery disease[J].Angiology,2003,54(5):561-567.
[6]Chu H,Chen J,Guo R.The association between cardiac calcification and coronary artery disease[J].Acta Cardiol,2009,64(4):531-535.
[7]王士雯,尹 彤,赵玉生.钙化性主动脉瓣膜狭窄的基础和临床研究进展[J].中华老年多器官疾病杂志,2004,3(2):305-308.
[8]Allison MA,Cheung P,Criqui MH,et al.Mitral and aortic annular calcification are highly associated with systemiccalcified atherosclerosis[J].Circulation,2006,113(6):861-866.
[9]Nkomo VT,Gardin JM,Skelton TN,et al.Burden of valvular heart diseases:a population-based study[J].Lancet,2006,368(9540):1005-1011.
