包装材料对医院制剂质量的影响
2010-06-09徐建东
徐建东
上海市皮肤病性病医院(200050)
国家食品药品监督管理局于2005年6月1日起实施的《医疗机构制剂配制管理办法》进一步加大了对医院制剂的质量要求和抽检力度。随着各大医院对自制制剂质量的重视,2006至2008年上海市药监局对全市各大医院制剂抽查的结果得出的结论是因检测偏差引起的制剂质量不合格比例明显下降,而因包装材料问题引起的制剂不合格比例却明显上升,本文就因包材对制剂质量产生影响的因素作一分析。
1 包装材料成分对自制制剂质量的影响
装材料成分为低密度聚乙烯,对于含油类液体制剂如樟脑薄荷脑滴鼻液、液状石蜡滴鼻液等制剂易发生渗漏现象,造成制剂外观不合格。
2 温度对存放于不同包装材料中樟脑薄荷脑滴鼻液质量的影响
2.1 标准液的制备
精密称取樟脑对照品适量,加液体石蜡溶解,并稀释成每1mL中约含樟脑10mg的溶液。
2.2 样品溶液的制备
精密量取本品3mL,置10mL量瓶中,加液体石蜡稀释至刻度,摇匀。
2.3 标准曲线的绘制
精密量取标准液0.5、1.0、2.0、3.0、4.0与5.0mL分别置10mL量瓶中,加液体石蜡稀释至刻度。摇匀,照分光光度法(《中国药典》2005年版,二部附录IV A)[1],以液体石蜡为空白,于292nm的波长处测定吸收度。求得回归方程为:△A=0.1599C—8.469×10-3,r=0.9991。结果表明,樟脑在0.5~5mg范围内,线性关系良好。
2.3.1 温度对储存于塑料瓶中樟脑薄荷脑滴鼻液质量的影响。结果见表1。
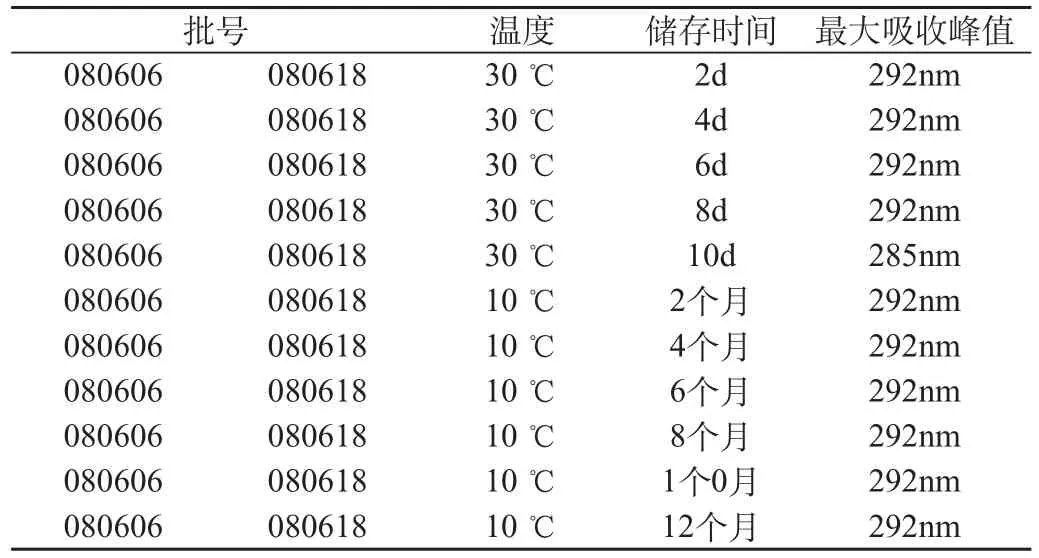
表1 温度对储存于塑料瓶中樟脑薄荷脑滴鼻液质量的影响
2.3.1.1 樟脑薄荷脑滴鼻液在高于30℃的环境下储存10d后,樟脑的最大吸收峰值由292nm偏移至285nm,该制剂中樟脑的有效成份发生变化,制剂由合格转变为不合格。
2.3.1.2 樟脑薄荷脑滴鼻液在低于10℃的环境中储藏2、4、6、10、12个月后,樟脑的最大吸收峰值不发生偏移,制剂质量稳定。
2.3.2 温度对储存于玻璃瓶中樟脑薄荷脑滴鼻液质量的影响。结果见表2。
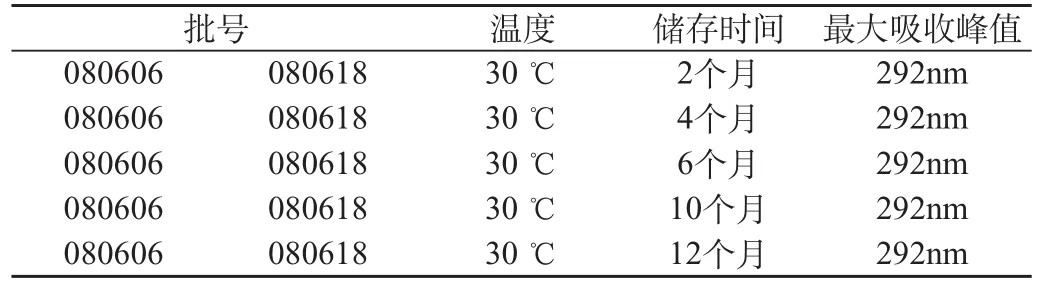
表2 温度对储存于玻璃瓶中樟脑薄荷脑滴鼻液质量的影响
樟脑薄荷脑滴鼻液存放于玻璃瓶中,储藏温度30℃,储藏2、4、6、10、12个月后,樟脑的最大吸收峰值不发生偏移,制剂质量稳定。
3 温湿度对包装材料微生物限度的影响
3.1 供试液的制备
取包材样品20个,每个样品中各加入pH 7.0无菌氯化钠-蛋白胨缓冲液(以下简称缓冲液)5mL,充分振摇后将洗液集中于已消毒瓶中,再取缓冲液5mL,清洗一次,收集洗液。
3.2 微生物限度检测
参照中国药典2005年版 附录Ⅺ J微生物限度检查法检查。结果见表3。
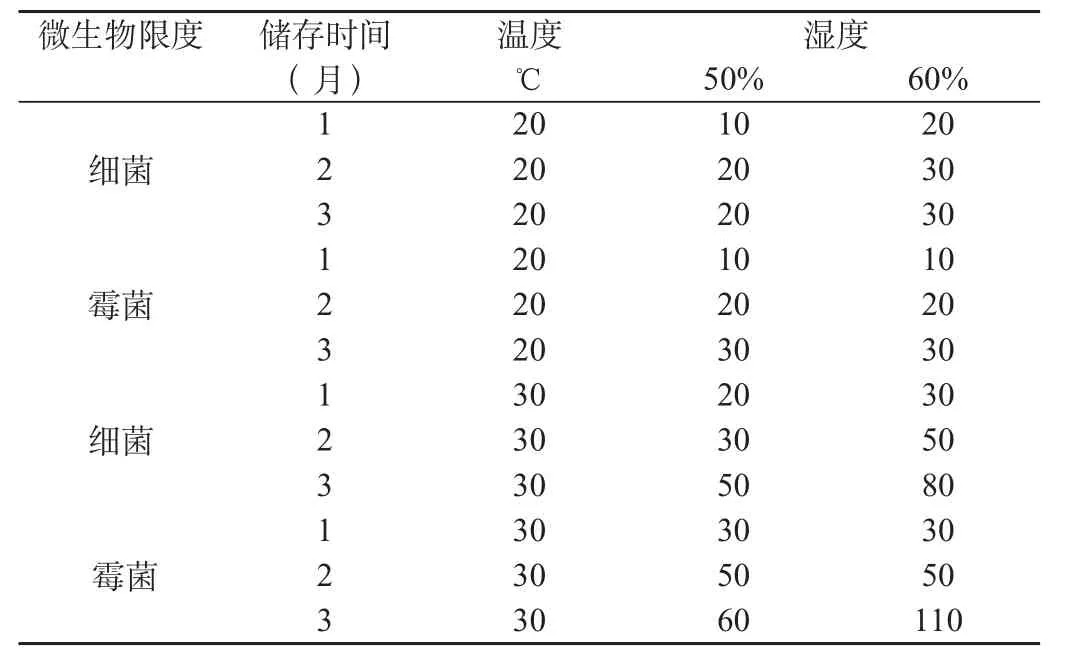
表3 微生物限度检测表
4 讨 论
发生制剂渗漏现象是由于包材致密性不够,建议更换其他成分的包材。
包装材料在不同的储存温度对制剂质量的影响很大,因温度造成的制剂不稳定可通过稳定性试验选择适宜的制剂储存温度。
储存于玻璃瓶中樟脑薄荷脑滴鼻液的质量不受温度和储存时间的影响。
温度对储存于塑料瓶中樟脑薄荷脑滴鼻液的质量影响很大,温度30℃,10d后樟脑最大吸收峰值发生偏移;温度低于10℃樟脑最大吸收峰值不发生偏移。
由于包材成分与制剂有效成分发生反应是在储存一段时间后发生,所以一定要加强医院自制制剂的留样观察。为了避免包装材料微生物限度不合格造成制剂质量不合格,包材应存放于洁净、通风、温度低于30℃,湿度不超过60%的环境,定期检测包材微生物限量,确保制剂质量。
[1]国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:附录93-101.
