高速逆流色谱法纯化丹酚酸B工艺研究
2010-06-05王继勇,何浏,袁晓
中药丹参[1]的化学成分主要分为两类:脂溶性二萜醌类和水溶性酚酸类[2]。丹酚酸B(Salvianolic acid B)是丹参主要的水溶性成分,具有明显的抗氧化[3]、放松血管[4]、保肝护肝[5]的作用,其结构式见图1。
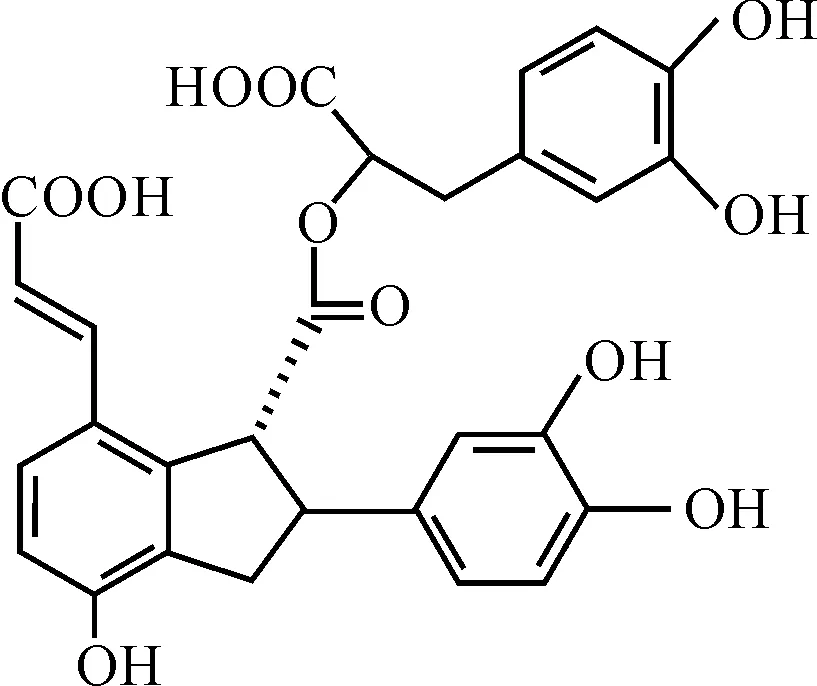
图1 丹酚酸B的结构式
高速逆流色谱法是由Ito[6]于20世纪80年代研发的一种新型液液分配技术。该技术无需固体载体,消除了样品的不可逆吸附,且具有分离度高、重现性好、分离量大等优势,广泛应用于天然植物的分离[7]。作者针对丹酚酸B极性大的特点,运用高速逆流色谱法对其进行了分离纯化。
1 实验
1.1 材料、试剂和仪器
丹参购于武汉百姓大药房,经中科院武汉植物园李建强鉴定为丹参根茎。
所用试剂均为分析纯,天津富宇精细化工有限公司;双蒸水,自制。
FastChromeTM分析型高速逆流色谱仪、CXTH-3000色谱工作站、CF-30恒流泵,江阴逆流科技有限公司; 分离柱管直径1.70 mm,柱体积26.0 mL,进样环1.0 mL;UV-3000型紫外检测器,北京创新通恒科技有限公司;日立液相色谱仪(Hitachi Pump L-2130,Hitachi Autosampler L-2200,Hitachi Column Oven L-2300,Hitachi Diode Array Detector L-2455);D-2000 Elite 工作站。
HPLC色谱条件:色谱柱:Fortis C18(250 mm×4.6 mm,5 μm),流动相:A为甲醇∶乙酸乙酯=4∶1(体积比),B为0.2%甲酸水溶液,A∶B=40∶60(体积比);流速1 mL·min-1,温度28℃,检测波长280 nm,进样量50 μL。
1.2 丹酚酸B部位的制备
取丹参切片100 g,粉碎,过200目筛,用70%乙醇溶液超声提取至无色。合并回收液,于60℃真空回收,制得粗浸膏。将粗浸膏过大孔树脂柱,流动相为甲醇-0.2%甲酸水溶液,共收集7段,其中第2段为丹酚酸B部位,用于后续实验。
1.3 高速逆流溶剂系统选择
按一定的比例配制溶剂系统,充分振荡,测定稳定时间,取相同体积的上下相溶液,加入一定量的样品,充分振荡混合,系统稳定后,分别取上下层溶液用HPLC进行含量分析,测定K值。
1.4 纯化工艺条件的确定
影响高速逆流系统分离效果的主要参数为流动相的流速、仪器的转速以及分离的温度。以保留率和稳定时间为考核指标,通过单因素实验确定最佳参数。
2 结果与讨论
2.1 溶剂系统的确定
溶剂系统的正确选择是实验成功的关键因素,合适的两相系统应该遵循以下原则[8]:
(1)具有一定的固定相保留率,一般溶剂的保留率应大于30%;
(2)两相在剧烈振动后,分层稳定时间应小于30 s;
(3)目标产物的K值应该在0.5与2之间;
(4)为了节约溶剂,要求上下两相有相近的体积。
根据各种溶剂的粘度、密度、极性等因素,测定了一系列溶剂系统的上下相体积比、稳定时间及K值,结果见表1。

表1 不同溶剂系统比较
由表1可知,石油醚-乙酸乙酯-甲醇-水-甲酸(1.0∶6.0∶1.5∶8.0∶0.1)的K值较适合丹酚酸B的分离,因此选择此溶剂系统为分离的最佳系统。
2.2 纯化工艺条件的优化(表2)
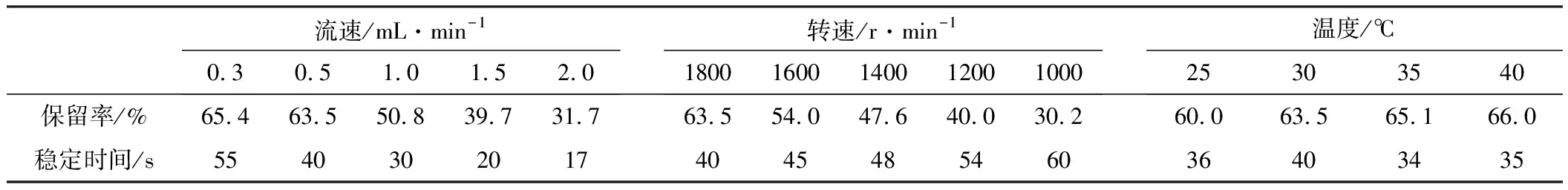
表2 工艺条件对保留率和稳定时间的影响
从表2可知,在转速与温度(仪器转速为1800 r·min-1、温度为30℃)一定的条件下,流动相流速越大,保留率越低,稳定时间越短。在流动相流速与温度(流动相流速为0.5 mL·min-1,温度为30℃)一定的情况下,转速越低,保留率越小,稳定时间越长。在转速与流动相流速(仪器转速为1800 r·min-1、流动相流速为0.5 mL·min-1)一定的情况下,温度越高,保留率越高,但对稳定时间几乎没有影响。
综合考虑保留率以及稳定时间,确定最佳工艺条件为:转速1800 r·min-1,流动相流速1.0 mL·min-1,温度30℃。
2.3 丹酚酸B的分离纯化及HPLC分析
将丹酚酸B部位进行HPLC分析,色谱图见图2a。由图2a可知第24 min峰为丹酚酸B,且为最大峰,表明此部位中含多种丹酚酸及鞣质,丹酚酸B含量最高。
运用高速逆流色谱对丹酚酸B部位进行分离,分离色谱见图3,第48 min峰为丹酚酸B,收集丹酚酸B,冷冻干燥。用HPLC分析,其色谱图见图2b。由图2b可知,第24 min峰为丹酚酸B,根据面积归一法计算丹酚酸B的纯度为98.3%。
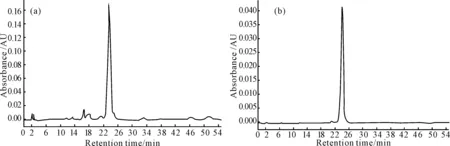
图2 丹酚酸B部位(a)和纯化后丹酚酸B(b)HPLC分析
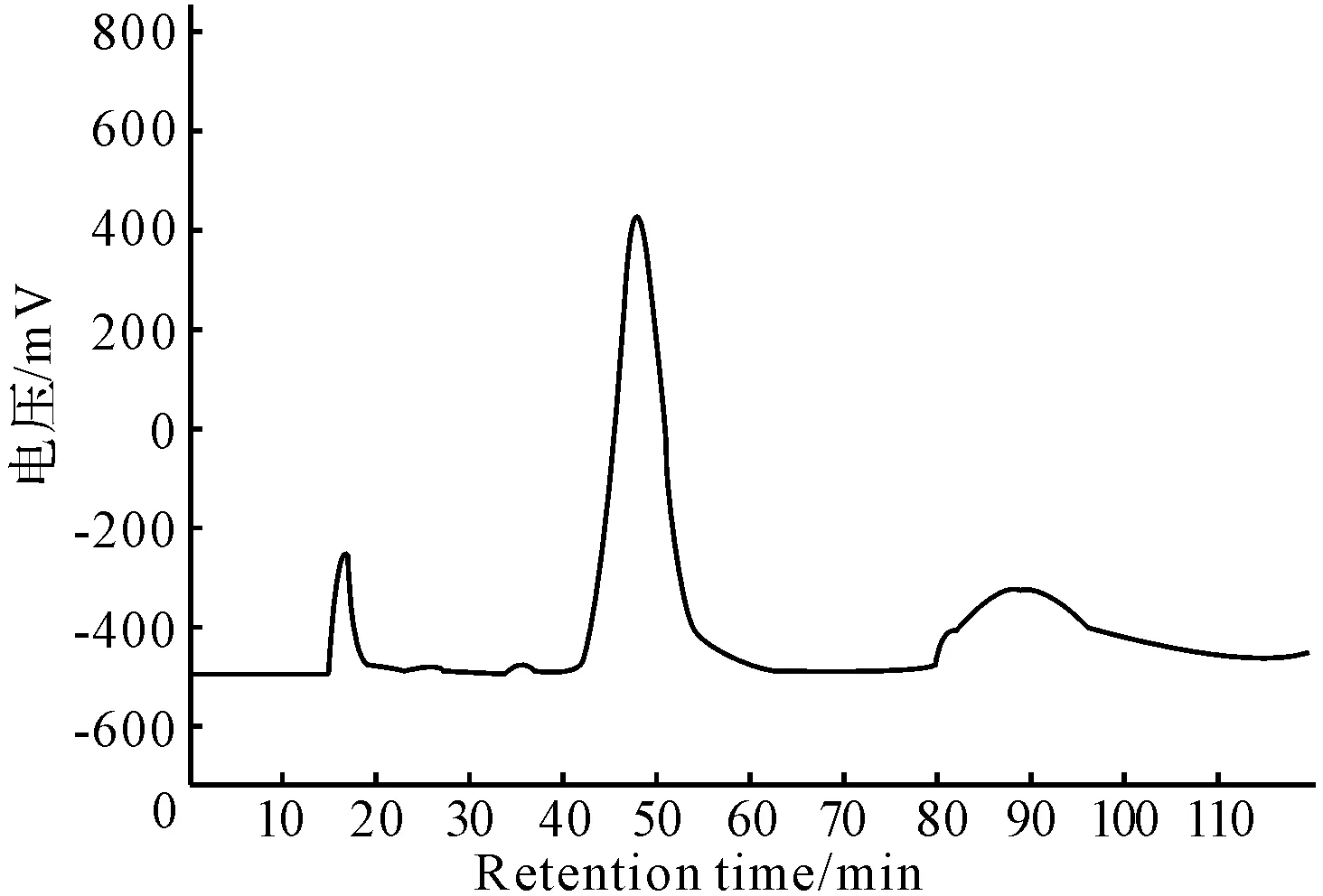
图3 丹酚酸B高速逆流分离色谱图
3 结论
运用高速逆流色谱法分离了丹参的活性成分丹酚酸B,其纯度达到98.3%,表明运用高速逆流色谱法能有效纯化丹酚酸B,且该方法与传统柱层析方法相比,具有不可逆吸附、无样品损失、成本低、方便、快捷等优点,可用于丹酚酸B的制备。
参考文献:
[1] 王举涛,彭代银,刘金旗,等.不同产地丹参中丹参酮ⅡA的含量比较[J].中国实验方剂学杂志,2008,14(3):4-5.
[2] 余世春,琚小龙,段广勋.丹参的化学成分和药理活性研究概况(综述)[J].安徽卫生职业技术学院学报,2002,(2):43-47.
[3] Liu C S,Chen N H,Zheng J T.Protection of PC12 cells from hydrogen peroxide-induced cytotoxicity by salvianolic acid B,a new compound isolated from RadixSalviaemiltiorrhizae[J].Phytomedicine,2007,14(7-8):492-497.
[4] Lam Francis F Y,Yeung John H K,Kwan Yiu W,et al.Salvianolic acid B,an aqueous component of danshen (Salviamiltiorrhiza),relaxes rat coronary artery by inhibition of calcium channels[J].European Journal of Pharmacology,2006,553(1-3):240-245.
[5] Lin Y L,Wu C H,Luo M H,et al.Invitroprotective effects of salvianolic acid B on primary hepatocytes and hepatic stellate cells[J].Journal of Ethnopharmacology,2006,105(1-2):215-222.
[6] Ito Y.Countercurrent Chromatography Theory & Practice[M].NewYork:Marcel Dekker Inc,1988:252-360.
[7] 戴德舜,王义明,罗国安.高速逆流色谱研究进展[J].分析化学,2001,29(5):586-591.
[8] Marston A,Hostettmann K.Developments in the appliacation of counter-current chromatography to plant analysis[J].J Chromatogr A,2006,1112(1-2):181-194.
