注射用头孢米诺钠与更昔洛韦的配伍稳定性考察
2010-06-02郑厚林陈阳建
郑厚林,陈阳建
(1.浙江省宁波市医疗中心李惠利医院,浙江 宁波 315040;2.浙江医药高等专科学校,浙江 宁波 315100)
头孢米诺钠(cefminox)为头霉素衍生物,由半合成法制取,其作用性质与第3代头孢菌素相近,对大肠杆菌、链球菌、克雷伯杆菌、流感嗜血杆菌、拟杆菌等有抗菌作用。更昔洛韦(ganciclovir)是核苷类抗病毒药,其抗病毒作用与阿昔洛韦相似。临床有时将两药联合用于治疗细菌和病毒的混合感染,但其配伍稳定性尚未见文献报道。为了给临床合理用药提供依据,笔者考察了两者的配伍稳定性,报道如下。
1 仪器与试药
UV-2401 PC型紫外-可见分光光度计(日本岛津);pHS-3C型精密pH计(上海雷磁仪器厂);HH恒温水浴箱(江苏省金坛市中大仪器厂);GWJ-3型微粒检测仪(天津大学精密仪器厂)。头孢米诺钠对照品(中国药品生物制品检定所,批号为130508-200301);注射用头孢米诺钠(山东鲁抗医药股份有限公司,批号为090607,规格为1.0 g/瓶);更昔洛韦对照品(贵州迪大科技有限责任公司,批号为100380-200901);注射用更昔洛韦(上海新先锋药业有限公司,批号为20081107,规格为250 mg/瓶);0.9%氯化钠注射液(上海百特医疗用品有限公司,批号为S0907103,规格为250 mL∶2.25 g)。
2 方法与结果
2.1 含量测定
2.1.1 测定波长选择
分别以0.9%氯化钠注射液配制质量浓度为30 μg/mL的头孢米诺钠溶液和10 μg/mL的更昔洛韦溶液以及混合溶液,以0.9%氯化钠注射液为空白,于200~400 nm波长范围内扫描,紫外扫描结果见图1。可见,头孢米诺钠和更昔洛韦分别在273 nm和252 nm波长处有最大吸收,与文献报道基本一致[1-2]。因两种药物的紫外吸收相互干扰,故选用双波长等吸收法测定含量。确定头孢米诺钠的测定波长为273 nm,参比波长为241 nm;更昔洛韦的测定波长为252 nm,参比波长为287 nm。

图1 紫外吸收光谱图
2.1.2 标准曲线绘制
精密称取头孢米诺钠对照品5.0 mg,置50 mL量瓶中,以0.9%氯化钠注射液溶解并稀释至刻度,得质量浓度为100 μg/mL的对照品溶液。用0.9%氯化钠注射液将上述对照品溶液稀释成质量浓度为5.0~30.0 μg/mL的系列对照品溶液。分别在273 nm和241 nm波长处测定其吸光度,计算两者吸光度的差值(ΔA=A273-A241),并对质量浓度进行线性回归,得回归方程 C=141.34 ΔA+0.037,r=0.999 3(n=6)。结果表明,头孢米诺钠质量浓度在5.0~30.0 μg/mL范围内与吸光度线性关系良好。精密称取更昔洛韦对照品2.5 mg,置50 mL量瓶中,以0.9%氯化钠注射液溶解并稀释至刻度,得质量浓度为50 μg/mL的对照品溶液。用0.9%氯化钠注射液稀释成质量浓度为2.0~12.0 μg/mL的系列对照品溶液。分别在252 nm和287 nm波长处测定其吸光度,计算两者吸光度的差值(ΔA=A252-A287),并对质量浓度进行线性回归,得回归方程 C=20.19 A-0.062,r=0.999 8(n=6)。结果表明,更昔洛韦质量浓度在2.0~12.0 μg/mL范围内与吸光度线性关系良好。
2.1.3 回收率试验
精密量取头孢米诺钠对照品溶液(100 μg/mL)和更昔洛韦对照品溶液(50 μg/mL)适量,用0.9%氯化钠注射液配制头孢米诺钠和更昔洛韦质量浓度分别为10.0 μg/mL和 5.0 μg/mL,15.0 μg/mL 和 7.5 μg/mL,20.0 μg/mL 和 10.0 μg/mL 的混合液,按2.1.2项下操作,分别在选定波长处测定吸光度,并将所得数据代入回归方程后计算回收率。结果见表1。
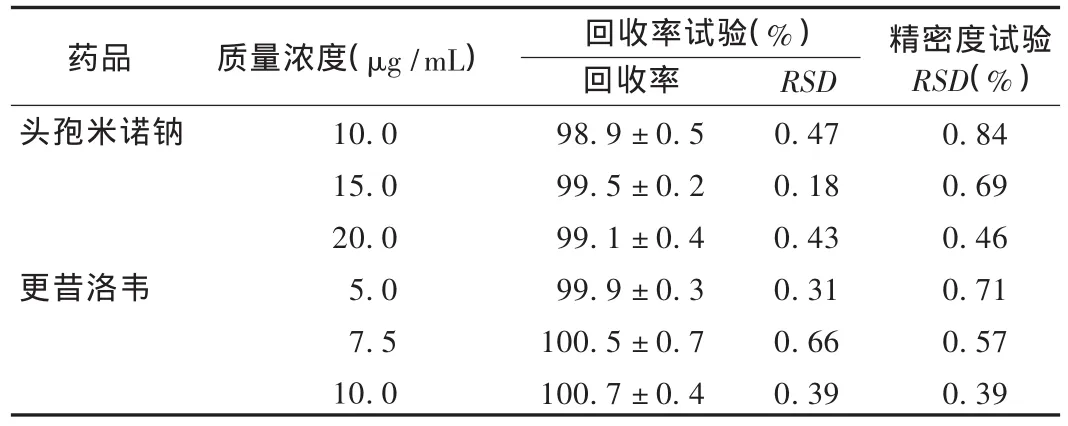
表1 头孢米诺钠和更昔洛韦的回收率(n=5)
2.1.4 精密度试验
按照2.1.3项下方法配制高、中、低3种质量浓度的混合液并按照2.1.2项下方法分别在选定波长处测定吸光度,每种混合液分别测定5次,将所得数据代入回归方程计算。结果见表1,表明该方法精密度较高。
2.1.5 重复性试验
精密量取100 μg/mL的头孢米诺钠溶液和50 μg/mL的更昔洛韦溶液适量,平行配制含头孢米诺钠和更昔洛韦分别为15.0 μg/mL和7.5 μg/mL的混合液6份;按照2.1.2项下操作分别在选定波长处测定吸光度,将所得数据代入回归方程计算。结果头孢米诺钠、更昔洛韦的 RSD分别为0.54%和0.37%(n=6),表明该方法误差较小,重复性良好。
2.2 配伍液稳定性考察
2.2.1 配伍液制备
模拟临床用药方案,取注射用头孢米诺钠1瓶(1.0 g/瓶)和注射用更昔洛韦2瓶(250 mg/瓶),溶于250 mL的0.9%氯化钠注射液中得到两者的配伍液。将配伍液分为2份,分别于25℃和37℃条件下放置,同时用0.9%氯化钠注射液配制等质量浓度的头孢米诺钠和更昔洛韦对照品溶液。
2.2.2 稳定性试验
外观性状:分别取氯化钠注射液5 mL稀释注射用头孢米诺钠和注射用更昔洛韦。头孢米诺钠样品溶液为微黄色、澄清,更昔洛韦样品溶液为无色澄明。两药分别用氯化钠稀释、混合后,混合液呈微黄色,在放置过程中颜色无明显变化,无气体产生,置锥形管高速离心后无可见沉淀、结晶。
pH和微粒变化:分别取氯化钠注射液5 mL稀释注射用头孢米诺钠1.0 g和注射用更昔洛韦250 mg。头孢米诺钠样品溶液在25℃和37℃时的pH分别为6.12和6.09,更昔洛韦样品溶液在25℃和37℃时的pH分别为11.13和11.17。两药配伍后立即测定的 pH 为 8.91,分别于 10 min 和 0.5,1,2,4,6,8 h 时测定配伍液在不同温度下的pH及不溶性微粒。结果表明,配伍液pH在8 h内较为稳定,25℃平均pH为8.86±0.03,37℃平均pH为8.89±0.04;各时刻测得的不溶性微粒数量无明显变化。
主药含量:分别于 0,1,2,4,6,8 h 时精密量取配伍液适量,用0.9%氯化钠注射液稀释至适当质量浓度,再以0.9%氯化钠注射液为空白,在选定波长处测定吸光度,将所得数据代入回归方程后计算各药的含量,并以0 h时的测得值为标示量。结果见表2。

表2 配伍液中头孢米诺钠与更昔洛韦含量的变化
吸收曲线:在测定含量的同时,以0.9%氯化钠注射液为空白对照,对稀释后的配伍液在200~400 nm波长范围扫描。结果显示在不同时间内配伍液的吸光度无明显变化,吸收峰峰形、峰位均无明显改变。配伍液在8 h时的紫外吸收光谱图见图2。
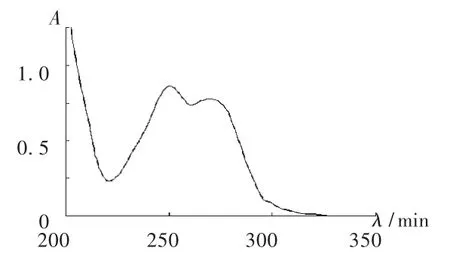
图2 配伍液在8 h时的紫外吸收光谱图
3 讨论
已有很多文献报道更昔洛韦与某些抗菌药物配伍的稳定性[3-6],但尚未见与头孢米诺钠配伍的稳定性报道。头孢米诺钠与更昔洛韦的紫外吸收光谱相互重叠,在含量测定时会相互干扰,因此采用双波长等吸收法以消除干扰[6-7]。结果表明,采用该方法测定含量时,样品不需要做任何处理,且操作简单。本试验结果表明,在25℃和37℃条件下,注射用头孢米诺钠与更昔洛韦配伍液在8 h内的外观、pH和主药含量均无显著变化,且紫外吸收曲线也没有明显变化。因此,两种药物混合后性质稳定,可在临床上配伍使用。
[2]熊 丽.紫外分光光度法测定更昔洛韦氯化钠注射液中更昔洛韦的含量[J].中国医药导报,2009,6(31):40-41.
[3]潘 浩,欧阳山丹,庄丽盆.注射用更昔洛韦与6种注射液的配伍稳定性的观察[J].海峡药学,2007,19(6):25-26.
[4]郭志锦.注射用更昔洛韦与14种药物配伍的稳定性研究[J].福建医药杂志,2008,30(5):74-75.
[5]梁陈方.头孢米诺钠与氨甲苯酸的配伍稳定性考察[J].中国药业,2007,16(2):30-31.
[6]黄 晨,诸林俏.头孢米诺钠与利巴韦林配伍稳定性考察[J].中国药业,2008,17(12):27.
[7]杨继章,刘瑞琴,徐秀娟,等.注射用加替沙星与注射用更昔洛韦配伍的稳定性考察[J].中国医院药学杂志,2008,28(21):1 881-1 883.
