SPE-GC/MS法检测水体中五氯酚残留
2010-01-11孙雅峰潘文碧井晶项丽蓉
孙雅峰 潘文碧 井晶 项丽蓉
(温州市工业科学研究院,浙江 温州 325028)
五氯酚及其钠盐具有杀虫、杀菌和除草等作用,曾被广泛用作皮革和木材的防腐剂、农作物的除草剂和杀虫剂。由于五氯酚具有致癌、致畸、致突变的潜在毒性,已被我国列为水中优先控制的污染物之一。温州市是全国最大的制革基地之一,皮革厂数量众多,由于早期的皮革加工中大量使用五氯酚等高毒性化工原料,工业废水直排入河,造成了温州市局部水体的污染;并且,PCP在自然环境中降解缓慢,会对环境造成长期的影响。因此,有必要对温州市水体中的五氯酚残留现状做一个调查。
分析工作者们对水中PCP的检测已作了很多研究[1-4]。据文献报道,GC和GC/MS已经广泛用于PCP的分析,但是前处理的过程中常需进行多次液液萃取[1,2],操作较烦琐、费时。本文先用乙酸酐对水样进行衍生,后采用SPE法纯化,GC/MS法检测,建立了一种较便捷快速的PCP测定方法。并将建立的方法应用于温州地区水体中PCP的残留分析。
1 实验部分
1.1 仪器与试剂
HP6890/5973 GC/MS气相色谱/质谱联用仪,美国HP公司;HP5MS色谱柱(30mm×25mm,0.25μm),美国安捷伦公司;12管SPE真空固相萃取装置,美国Agilent公司;MTN-2800W型自动快速浓缩仪,天津美特塞恩斯有限公司;AP-01P型真空泵,天津美特塞恩斯有限公司;12管SPE真空固相萃取装置,美国Agilent公司;C18固相萃取柱(6mL,500mg),美国安捷伦公司;Oasis HLB柱(6mL,0.2g),Waters公司;PCP标准品,GSB05-1850-2008,100μg/mL,农业部环境保护科研检测所;二氯甲烷、丙酮、正己烷、甲醇为色谱纯;其它试剂均为分析纯;超纯水用Milli-Q系统制取。
1.2 水样的采集
采样时间为2010年6月。采样点包括温州市3个主要水源,A水库、B水库和C水库,每个水库设置l~3个采样点;分别在D河Ⅰ段和Ⅱ段、E河、F江、G江、H湿地分别设置l~3个采样点;饮用自来水样采自温州市鹿城区。水样以干净褐色玻璃瓶采集。
1.3 水样前处理
取水样100mL,经0.45μm滤膜过滤,调pH至中性,加2.0mL乙酸酐,摇床振摇1h衍生;将容量为6mL的C18柱安装到固相萃取装置上,用10mL甲醇和10mL超纯水先后对C18柱进行活化,将水样以2mL/min流速流过上述装置,氮气吹干;控制流速为0.4mL/min,用10mL二氯甲烷进行洗脱,收集洗脱液、氮气吹至少于1mL,用二氯甲烷定容至1mL,待分析。
1.4 检测方法
色谱条件:初始柱温60℃,保持2min,以10℃/min的温度梯度升至250℃,保持5min;进样口温度200℃;电子捕获检测器(ECD)温度320℃;载气为纯度>99.999%的高纯氦气,流量1.0mL/min,进样量1.0μL。
质谱条件:离子源温度230℃;接口温度270℃;离子能量70eV;溶剂延时5min;扫描范围50~500amu,全扫描,扫描间隔0.2s。
2 结果与讨论
2.1 衍生化的讨论
随着GC/MS的普及,PCP的GC/MS法检测已有较多的报道,文献[3-6]采用不通过衍生化直接进行GC/MS检测,本文对比了PCP直接进样和PCP衍生化后再进样的方法,其色谱图显示未衍生化的情况下PCP峰严重拖尾,影响了定量分析的准确性。这是由于PCP易吸附于毛细管柱的固定相上,在进行GC/MS测定时,易产生拖尾[7]。为了准确定量样品中的PCP,本文使用乙酸酐将水样衍生化后进行分析。
2.2 水样纯化方法的选择
根据GB 8972-1988[1],水样须经两次液液萃取来达到纯化的目的,范苓等[2]将方法进行简化,只需进行一次萃取,但是这类液液萃取的方法操作费时,并需使用大量溶剂,萃取的过程中有效物质大量流失,作者也对这两种方法进行了实验,当PCP加入量为50μg/L时,两种方法的回收率分别为85.1%和91.6%。固相萃取(SPE)技术具有溶剂使用量少、高效快速、能减少背景干扰、提高回收率的优点。使用本文1.3的方法,利用SPE法纯化水样,PCP的回收率为91.9%,与液液萃取法得到的回收率结果差别不大。但是考虑快速和操作方便的原因,本文选择SPE法来对衍生化后的水样进行纯化。
在固相萃取柱的选择上,我们对比了两种常用的固相萃取住:C18柱和HLB柱(亲水亲脂平衡柱,Hydrophilic-Lipophilic Balance),在相同条件下,使用HLB柱时,PCP回收率仅为56.2%,因此,本实验选择C18柱对样品进行富集。
选择洗脱剂首先应考虑其对固相的适应性和对样品的溶解度,要保证对分析物的完全洗脱。文献中常用的洗脱剂有二氯甲烷、丙酮、正己烷、甲醇等[3-6],本实验将这几种洗脱剂进行比较,回收率结果如表1所示。其中,二氯甲烷对PCP的回收率较高,因此,选择二氯甲烷做为洗脱剂。

表1 洗脱剂的比较
2.3 GC/MS分析条件的确定
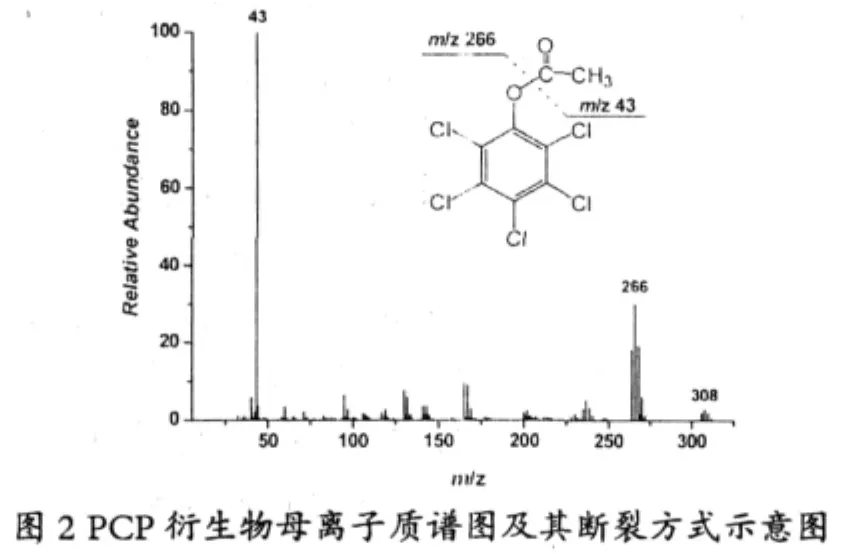
五氯酚衍生物五氯苯乙酸酯的总离子流色谱图见图1。质谱图及断裂方式如图2所示,可推断组分碎片离子:五氯苯乙酸酯除了极少量的母离子(m/z 308)之外,其主要碎片离子为m/z 266,m/z 43,这两个离子峰,该离子峰主要来自于COCH3基团断裂后的峰和COCH3离子碎片峰;在实际样品测试时,采用全扫描,根据保留时间和特征离子峰m/z 308,m/z 266,m/z 43进行定性分析。

2.4 方法线性与检出限
分别取一定量100μg/mL标准贮备液,在10mL 0.2mol/L K2CO3介质中用0.5mL乙酸酐衍生化后,加入10mL正己烷萃取衍生化产物五氯苯乙酸酯,最后浓缩定容至1.0mL,得浓度为0.4、2、10、50、100、500、1000、2000、5000、10000μg/L的五氯苯乙酸酯系列标准溶液。将这组溶液分别进样进行GC/MS测定,每个浓度水平的样品平行进3针,根据10个浓度水平绘制标准工作曲线,以浓度为横坐标、峰面积为纵坐标,得线性方程为Y=391794X-15278,相关系数R2=0.9997。表明在0.4~10000μg/L范围内,PCP浓度与色谱峰面积有很好的线性关系。水样100mL时,得PCP检出限为0.003μg/L,定量限为0.010μg/L。说明本方法适用于痕量PCP的定量分析。
2.5 精密度与加标回收试验
向饮用水样中分别加入浓度为5、50、500μg/L的五氯酚标准溶液,分别进行3次加标回收测试,方法的加标回收率为81%~95%,相对标准偏差(RSD)≤3.0%。结果见表2。
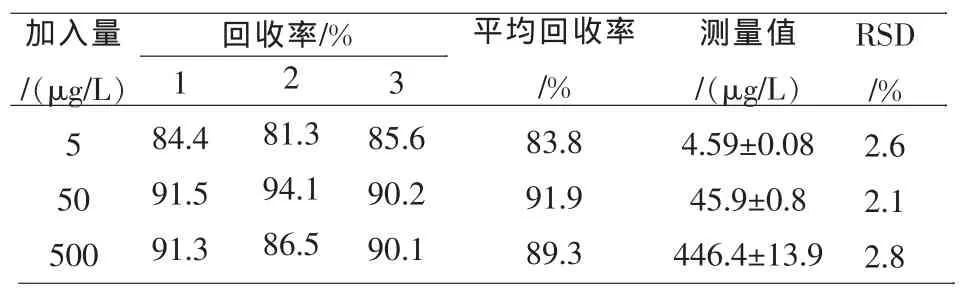
表2 五氯酚精密度、加标回收率的测定(n=3)
2.6 实际水样测定
采用上述检测方法对温州10处水体水样进行分析,检出结果见表3。从结果中可以看出,除市区自来水及A、C两水库外,均有检出少量的五氯酚残留,最高残留检出量为0.074μg/L,远低于国家生活饮用水卫生标准GB 5749-2006的限定值0.009mg/L[8]。
五氯酚作为农药曾被广泛应用于温州市的农业生产中,且温州市的皮革厂、造纸及纸制品厂、化学原料及化学制品厂等也曾大量使用PCP,长期的工业废水排放对温州局部水环境也造成了一定程度的污染。当前,PCP的使用与排放虽已受到较严格控制,但是,由于长时间大范围使用,水体中的残留量累增,且五氯酚能在生物体内蓄积,并通过食物链对人体造成危害,因此有必要进一步严格控制温州市水体中的五氯酚污染。

表3 温州市水体中五氯酚残留检测结果
3 结论
本文通过对前人方法的一些改进,确定了水中PCP的测定方法,方法首先使用乙酸酐对水样进行衍生化,再采用SPE-GC/MS联用技术对PCP衍生物五氯苯乙酸酯进行检测,实现了水体中五氯酚的定性定量分析,并得到了较高的回收率。该方法定性定量准确,检测简单快速,能够满足水质监控的需要。
[1]GB 8972-1988.水质—五氯酚的测定—气相色谱法[S].
[2]范苓,夏豪刚.气相色谱/质谱法测定水中五氯酚[J].环境监测管理与技术,2001,13(1):33-34.
[3]任雪冬,吕蓉,刘成雁,等.水中11种酚类化合物的固相萃取/气相色谱-质谱/选择离子法测定[J].分析测试学报,2008,27(5):501-504.
[4]马云云,李红莉,时杰,等.C18-固相萃取/气相色谱法检测水中氯酚类[J].中国环境监测,2009,25(4):46-48.
[5]M R Lee,Y C Yeh,W S Hsiang,et al.Solid-phase microextraction and gas chromatography-mass spectrometry for determining chlorophenols from landfill leaches and soil[J].Journal of Chromatography A,1998,806(2):317-324.
[6]Ribeim A,Neves M H,Almeida M F,et al.Directdeterm -ination of ehlomphenols in landfill leachates by sohd-phase microextraction gaschromatography massspectrometry[J].Joumal of Chromatogrophy A,2002,975(2):267-274.
[7]孙磊,蒋新,周健民,等.红壤中痕量五氯酚的气相色谱法测定[J].分析化学,2003,31(6):716-719.
[8]GB 5746-2006.生活饮用水卫生标准[S].
