人脐带间充质干细胞的分离培养及其与胶原支架材料的相容性
2009-04-11刁垠泽马庆军
王 琦 刁垠泽 马庆军
·论著·
人脐带间充质干细胞的分离培养及其与胶原支架材料的相容性
王 琦 刁垠泽 马庆军
目的探讨人脐带间充质干细胞(Mesenchymal stem cells,MSCs)体外分离、培养的方法,观察其与胶原蛋白支架的相容性,为进一步研究提供依据。方法利用组织体外培养法分离人脐带MSCs,流式细胞学分析细胞表型,组织化学观察细胞分化能力;将细胞静态接种于胶原蛋白支架上,观察细胞在材料中的形态、粘附情况和增殖特点。结果直接贴壁法分离的细胞表型均一,体外具有成骨和成脂肪能力;细胞在支架上有较好的粘附铺展,培养2周后,MSCs占据支架总体积的80%,细胞分布较均匀。结论组织块培养法可获得高纯度的人脐带MSCs,细胞在体外与胶原蛋白有较好的组织相容性。
脐带间充质干细胞胶原蛋白生物支架相容性
组织工程细胞-支架复合物至少包括两个重要组成部分,即活细胞和支架材料,其中活细胞是产生新组织的决定性成分,是构建组织工程复合体的关键因素,因此寻找再生能力强的种子细胞和适合细胞生存的生物材料便成为组织工程研究的核心内容[1]。本研究以人脐带源性间充质干细胞为种子细胞,观察其在牛胶原蛋白支架上的贴附、生长和分化情况,证明两者可以形成细胞-支架复合物。
1 材料与方法
1.1 材料
人脐带间充质干细胞分离自产妇脐带,Ⅱ型胶原蛋白购买自北京贝菱公司,是将18个月龄的健康牛跟腱通过酶解获得,DMEM培养基采用市售产品。
1.2 方法
1.2.1 人脐带间充质干细胞(Human umbilical cord mesenchymal stem cells,hUC-MSCs)的培养
将脐带剪切成4~5 cm长的小段,挤净血管内血液,用眼科剪沿血管将包裹着血管的Wharton胶剪下,于小培养皿内进一步剪碎。将组织小块收集于50 mL离心管内,每次加入5倍以上体积的PBS,反复清洗2~3次,室温下160 g离心8 min。清洗后的组织小块种植于100 mm培养皿,加入含10%FBS的a-MEM培养基,在37℃、饱和温度、5%CO2培养箱内培养。隔2日更换培养基,细胞达到80%汇合时更换新鲜培养液,次日去除培养液后以37℃预热的PBS轻柔冲洗细胞,弃去PBS后加入适量胰酶-EDTA,光镜下观察细胞,当胞质回缩、胞体变圆时弃去胰酶,以含FBS的培养基轻柔吹打细胞使之脱落,将细胞悬液离心清洗两次,计数,依细胞数量接种于新的培养瓶。
1.2.2 细胞表面标志鉴定
取第4代生长状态良好细胞,消化并计数,用含2%胎牛血清的冷FBS重悬细胞,制备成单细胞悬液,调整细胞浓度为1×106cells/mL,以每管2×105个细胞分装,分别加入以下抗体(按说明书推荐用量):小鼠抗人CD29-FITC,CD34-FITC,CD45-FITC,CD71-FITC,CD90-FITC,CD117-FITC;CD80-PE,CD86-PE,CD105-PE,HLA-A、B、C-PE,CD73-PE;CD14-PE,CD44-PE,HLA-DP、DQ、DR-PE。分别以小鼠IgG1-FITC、小鼠IgG1-PE、小鼠IgG2a-PE作为同型对照,4℃避光孵育30 min。用PBS洗涤2次,每管加入200 μL流式细胞仪固定液,轻柔吹打成单细胞悬液,上机检测。
1.3 体外分化实验
按文献[2]报道方法进行MSCs体外成骨和成脂肪能力鉴定,NBT-BCIP染色显示碱性磷酸酶活性,油红染色显示细胞内脂肪滴。
1.4 支架与细胞共培养
将胶原蛋白支架材料置入24孔培养板中,每孔各一块,取消化后体外培养的第6代细胞制成单细胞悬液,细胞密度2×106cells/mL,每孔接种2 mL,并浸没支架,次日更换培养液,每日使用相差显微镜观察细胞与生物材料附着及生长等情况。
1.5 组织化学分析
植入2周后,取出标本,以10%中性福尔马林固定,制备石腊切片,HE染色,观察组织在支架材料内的生长情况。
2 结果
2.1 细胞生长情况
接种后7~12 d可见细胞从组织块爬出,呈成纤维细胞样,约2周时细胞达到80%汇合,可进行传代,传代后2~3 h贴壁,4~6 d长满,细胞汇合成单层细胞,生长旺盛(图1)。
2.2 hUC-MSCs的培养、鉴定
第4代细胞的流式分析表明,培养的MSCs样细胞表达CD29,CD73,CD105,CD166,HLA-A、B、C(MHC-Ⅰ);不表达CD31(内皮细胞抗原),CD34(造血干细胞抗原),CD45(白细胞共同抗原),和HLA-DR(MHC-II)。
进一步研究表明,细胞经诱导后高表达碱性磷酸酶活性,细胞内出现脂滴。证明细胞具备成骨和成脂肪能力,提示所得贴壁细胞为MSCs(图2)。
2.3 相差显微镜镜下结果
脐带间充质干细胞与支架共培养24 h,在倒置显微镜下大部分细胞呈梭形、多角形、不规则形等,黏附于胶原蛋白细胞支架上,胶原蛋白与细胞有良好的相容性,在胶原蛋白的边缘可见明显的细胞长入,细胞对支架材料有良好的趋向性(图3)。
2.4 苏木精-伊红染色结果
在混合培养中支架与细胞相容性良好,细胞在材料中粘附良好,呈棱形和多角形生长。细胞与支架材料有趋向性,在支架材料的边缘明显可见细胞长入,胶原蛋白的多孔结构非常有利于细胞长入。在胶原蛋白纤维上有细胞密集区,细胞核呈椭圆形,染淡蓝色,胞质染淡红色,细胞生长于网架纤维之间,外形饱满,具有良好的生长形态,在细胞与纤维之间以及细胞与细胞之间均有较多突起相互交连(图4)。
图1 传代培养2 d后细胞生长状况

图2 脐带MSCs经诱导后碱性磷酸酶活性高(左);经脂肪诱导后细胞浆内出现脂滴(右)

图3 脐带间充质干细胞与支架共培养2周后细胞生长状况
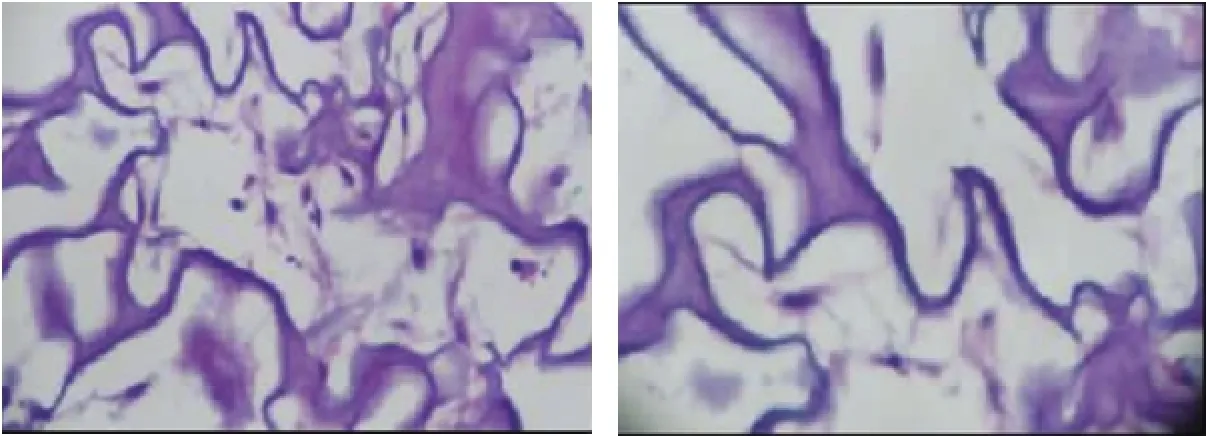
图4 支架与细胞共培养苏木精-伊红染色(左:培养2周时间;右:培养3周时间)
3 讨论
MSCs是骨组织工程的理想种子细胞,骨髓是目前MSCs的主要来源[3]。然而由于其细胞数量和增殖分化能力随年龄增长而显著下降,移植物不便在体外预先定制,异体移植中的伦理争议以及病毒传染等问题又限制了其临床应用[4]。在前期实验中已证实,脐带来源间充质干细胞体外诱导条件下可以分别向骨、软骨、脂肪组织分化,在体内具有成骨能力,可以为骨组织工程提供新的种子细胞来源。本研究从人类脐带中分离、培养MSCs,其细胞免疫表型与骨髓源性的MSCs相似,只表达HLA-Ⅰ类分子,不表达HLA-Ⅱ类分子,也不表达共刺激分子。体外培养发现,未分化的MSCs可以抑制同类基因的增殖反应。有人将人类脐带基质分离的MSCs直接注入Hemi Parkinson模型鼠的脑内,未发现免疫排斥反应,并且部分缓解了该模型的典型症状,这表明UC-MSC有免疫逃避能力,如果MSCs能够避免同种异体移植障碍,其临床应用前景广阔[3]。
单纯细胞移植由于缺乏附着点和空间结构支持而呈漂浮状态,无良好的移植微环境将不利于细胞存活和发挥正常功能。因此在损伤部位桥接组织工程支架材料受到了广泛关注,可作为移植治疗的载体及移植后的生长支架,对病灶起支撑填充作用,待细胞分化增殖填充后又可自行降解。采用组织工程方法构建器官来修复或替代损伤组织、器官是具有广阔前景的新途径[2]。
理想的载体材料应该具有良好的组织相容性、生物降解性、生物工程活性等[1]。生物材料的生物相容性包括生物安全性和生物功能性。对生物材料相容性研究有很多方法,其中常用的有体内直接植入法和体外复合细胞培养法两种。体内直接植入法由于受多种体内环境因素的影响,较难准确反映生物材料与组织细胞的相容性。而体外复合细胞培养可以直接观察细胞与生物材料复合生长的情况,较前者更为敏感、客观[4],是近年来研究生物材料相容性的主要方法。因此,本实验选用胶原蛋白-硫酸肝素支架与MSCs在体外复合培养,结果发现两种生物材料对细胞的生长无明显不良影响。通过形态学观察,发现MSCs可以在胶原蛋白支架中逐渐贴附,还能进一步增殖、分化。随着培养时间的延长,细胞长入孔隙内,说明支架有很好的细胞亲和性,支架孔径适合细胞粘附生长,可见胶原蛋白支架与MSCs具有很好的生物相容性。
胶原蛋白海绵是以牛跟腱为原材料,通过酶解,纯化抽取高纯Ⅱ型胶原,再根据连贯网络技术制成,纯度高,生物相容性优异。胶原海绵呈网状结构能提供组织生长支架[5],且其保持了蛋白质的三维螺旋结构,因而具有生物活性。本实验结果示,胶原蛋白生物材料与干细胞具有良好的生物相容性,胶原蛋白支架有望作为组织工程载体材料应用于临床。
1汪洋,王友.间充质干细胞在关节软骨缺损修复中的应用[J].组织工程与重建外科杂志,2008,4:231-233.
2王恒湘,边素艳,陈金龙,等.间充质干细胞不抑制体内T淋巴细胞的增殖[J].组织工程与重建外科杂志,2006,2:248-250.
3王恒湘,郭子宽.间充质干细胞在组织再生应用中的诸多问题[J].组织工程与重建外科杂志,2008,4:241-245.
4Lavik E,Langer R.Tissue engineering:current state and perspectives [J].Appl Microbiol Biotechnol,2004,65:1-8.
5武继民,李荣,王岩.胶原海绵作为止血和创面下敷料的临床试验[J].生物医学工程与临床杂志,2003,7:152-154. (收稿日期:2008年12月21日;修回日期:2009年1月14日)
Isolation of Mesenchymal Stem Cells Derived from Human Umbilical Cord and Their Compatibility with Collagen Scaffolds
WANG Qi,DIAO Yinze,MA Qingjun.
Department of Orthopedics,Third Hospital of Beijing University,Beijing 100036,China.Corresponding author:MA Qingjun.
ObjectiveTo search optional biomaterials for mesenchymal stem cells(MSCs)based tissue construction.The compatibility of human umbilical MSCs with collagen scaffolds was investigated in vitro.MethodsHuman umbilical MSCs were isolated by direct explant culture,and the phenotypic and differentiation characteristics were analyzed by flow cytometric technique and histological staining respectively.MSCs were seeded onto the collagen scaffolds and the morphological,adhensive and proliferation features were observed.ResultsThe cells were homogenous phenotype and occupied the ability of osteogenesis and adipogenesis in vitro.The cells were adhered and spread into the scaffolds thoroughly.The cells covered around 80%of the total volume of the scaffold after two weeks.ConclusionHuman umbilical MSCs could be readily isolated and harvested by explant-culture method.Collagen scaffold may be served as an optional biomaterial for three-dimension culture of MSCs.
Umbilical cord mesenchymal stem cells;Collagen;Scaffold;Compatibility
Q813.1+1
A
1673-0364(2009)-01-0001-03
10.3969/j.issn.1673-0364.2009.01.001
国家自然科学基金(30571870)。
100036北京市北京大学附属第三医院骨科。
马庆军。
