基于高效液相色谱法检测鲫肌肉中5种氟喹诺酮类药物
2025-03-01刘文鼎丁国栋钟佳慧




摘要:为检测鲫肌肉中5种氟喹诺酮类(FQs)药物(诺氟沙星、环丙沙星、恩诺沙星、噁喹酸、氟甲喹)的残留量,建立了一种高效液相色谱检测方法。本方法使用T3色谱柱,流动相为01%的甲酸水溶液和乙腈,采用梯度洗脱法,利用荧光检测器检测。结果表明5种氟喹诺酮类药物在001~200 μg/mL药物浓度条件下有良好线性关系(r2gt;0999);5种药物的检出限为006~013 μg/kg;定量限为018~038 μg/kg;药物回收率为9227%~11476%,相对标准偏差(RSD)为141%~850%。结果表明方法准确、灵敏、稳定,满足氟喹诺酮类药物的检测要求,可为水产品中FQs的检测和研究提供技术参考。
关键词:鲫;氟喹诺酮;高效液相色谱
中图分类号:TS2547文献标识码:A
作为人工合成的新型抗菌药物,氟喹诺酮类(Fluoroquinolones,FQs)药物具有抗菌作用强、抗菌谱广、高效、低毒、半衰期较长、用药次数少等特点,目前被广泛应用于水产养殖业[1-3]。中国是渔业大国,水产养殖水域广阔,水产品种类丰富,水产品产量持续上升[4]。然而,随着FQs在水生生物养殖中的广泛应用,水产品体内药物残留情况也愈发严重,这对人类生命健康构成了一定的风险[5]。因此,对水产品开展FQs药物残留检测,对严控水产品质量和保障人民食品安全具有重要意义。目前水产品药物残留检测方法主要有色谱法、免疫分析法、毛细管电泳法、电化学传感器法和光谱法等[6-7],这些方法各有特点,适用于不同要求和目的的检测项目。色谱法中的高效液相色谱法(HPLC)因其具有强大的分离能力和极高的灵敏度,是一种药物检测的经典方法。
我国于2021年发布了关于液相色谱法测定水产品中氟喹诺酮类药物残留量的标准(GB 316563—2021)[8],本研究以《GB 316563—2021》为基础,通过改变色谱柱类型、流动相等进行试验,用荧光检测器的高效液相色谱仪梯度洗脱检测,测定水产品中FQs残留,旨在拓展和优化当前已有的检测方法,提高检测精度和效率,为后续水产品中FQs类药物的研究和检测奠定基础。
1 材料与方法
11 材料与仪器
供试样本:鲫,来自江西省水产科学研究所。
药品:诺氟沙星、环丙沙星、恩诺沙星、噁喹酸、氟甲喹5种药物标准品均为Stanford Analytical Chemical Inc生产。其中诺氟沙星、环丙沙星和氟甲喹纯度均为99%,恩诺沙星和噁喹酸纯度均为98%。
试剂:甲醇(Honeywell,GR)、乙腈(Honeywell,GR)、正己烷(Honeywell,GR)、甲酸(Honeywell,GR)、洗脱液(氨水+甲醇,体积比为1∶3);酸化乙腈溶液:取乙腈250 mL,加盐酸溶液2 mL,充分混匀;乙腈饱和正己烷溶液:取正己烷200 mL于250 mL分液漏斗中,加适量乙腈后剧烈振荡,待分配平衡后,弃乙腈层即得。
仪器:液相色谱仪(Agilent 8890)、分析天平(EX125DZH)、氮吹仪(HSC-24B)、高速离心机(TG10K)、固定式混匀仪(MX-F)和旋蒸仪(RE100-S)。
12 方法
121 标准曲线
标准储备液(100 μg/mL):称取环丙沙星和恩诺沙星各001 g(精确至00001 g,下同),分别用色谱纯级甲醇溶解,定容至100 mL棕色容量瓶中,配置成100 μg/mL的母液;取诺氟沙星001 g,用01 mol/L盐酸溶液10 mL使其溶解,用乙腈稀释定容至100 mL棕色容量瓶中,配置成100 μg/mL的母液;取噁喹酸和氟甲喹各001 g,用01 mol/L氢氧化钠溶液10 mL使其溶解,分别用乙腈稀释定容至100 mL棕色容量瓶中,配置成100 μg/mL的母液。以上储备液均4℃冷藏保存,有效期3个月。
标准工作液(10 μg/mL):量取5种标准储备液各1 mL,分别置于10 mL棕色容量瓶中,用01%的甲酸溶液稀释至刻度,配制成10 μg/mL 5种药物的标准工作液。
标准曲线制备:分别准确吸取一定量的诺氟沙星、环丙沙星、恩诺沙星、噁喹酸、氟甲喹标准工作液于6个容量瓶中,用01%的甲酸溶液稀释成浓度为001、005、010、050、100、200 μg/mL的标准溶液,每个容量瓶中5种药物的浓度保持一致。以药物浓度为横坐标,峰面积为纵坐标,绘制标准曲线。
122 检出限和定量限
检出限:根据仪器的信噪比(I/N)来计算方法的检出限,计算公式为:
123 样品前处理
取鲫背部肌肉5 g(准确至±002 g),加酸化乙腈溶液20 mL、无水硫酸钠10 g,高速均质2 min,3000 r/min离心5 min,取上清液至分液漏斗,用酸化乙腈溶液20 mL重复提取2次后合并上清液。加乙腈饱和正己烷溶液60 mL,振荡20 min后静置,取下层乙腈至梨形瓶,40℃旋转蒸发至干。加磷酸盐缓冲液4 mL,超声振荡1 min,静置30 s,溶液转移至15 mL离心管。再重复提取残余物2次,溶液转移至同一离心管,合并3次残余物溶解液,3000 r/min离心5 min,取上清液。取上清液过活化后的C18固相萃取柱,用3 mL水淋洗,抽干后加洗脱液5 mL,使用氮吹仪在50℃下吹干,加1 mL 01%的甲酸溶液溶解,过022 μm微孔滤膜后备用。
124 回收率和精密度
取5 g(准确至±002 g)鲫肌肉样品4份,其中1份为空白检测样,3份为测试样。向每份测试样中加入诺氟沙星、恩诺沙星、噁喹酸和氟甲喹标准工作液,使诺氟沙星、恩诺沙星、噁喹酸和氟甲喹在每份测试样中的浓度分别为6、12、100 μg/kg;向测试样中加入环丙沙星标准工作液,使环丙沙星在每份测试样中的浓度分别为5、10、100 μg/kg。按照“123”前处理方法处理空白检测样和测试样后上机检测。
每份样品平行测定6次,计算样品回收率,其计算公式为:
2 结果与分析
21 色谱分离
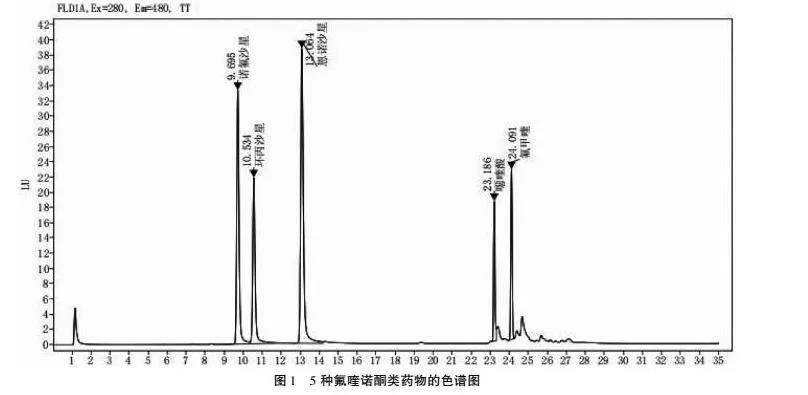
诺氟沙星、环丙沙星、恩诺沙星、噁喹酸和氟甲喹在本色谱条件下的出峰时间分别为:9695、10534、13064、23186和24091 min,具体见图1,结果表明,5种氟喹诺酮类药物可以获得良好的分离和峰型,并且样品中其余杂峰对主峰基本无干扰。
22 标准曲线
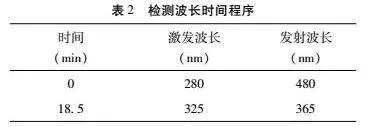
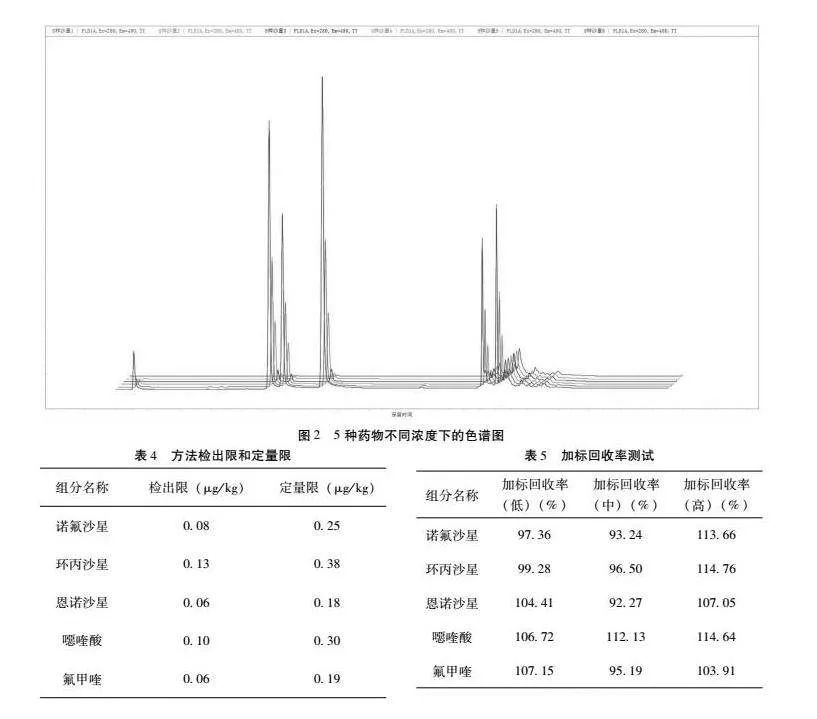
以药物浓度为横坐标(x),峰面积为纵坐标(y),得出5种氟喹诺酮类药物的标准曲线,诺氟沙星、环丙沙星、恩诺沙星、噁喹酸、氟甲喹的回归方程和线性相关系数见表3,5种药物浓度和峰面积在001~200 μg/mL呈现出线性关系(r2gt;0999)。不同药物浓度下色谱图如图2所示。
23 检出限和定量限
当进样量为10 μL,浓度为001 μg/mL时,诺氟沙星、环丙沙星、恩诺沙星、噁喹酸和氟甲喹的信噪比(S/N)分别为726、476、988、609和931。检出限和定量限结果如表4所示,诺氟沙星、环丙沙星、恩诺沙星、噁喹酸和氟甲喹检出限分别为008、013、006、010和006 μg/kg,定量限分别为025、038、018、030和019 μg/kg。
24 回收率和精密度
环丙沙星在5、10、100 μg/kg添加水平下的加标回收率分别为9650%~11476%;诺氟沙星在6、12、100 μg/kg添加水平下的加标回收率分别为9324%~11366%;恩诺沙星在6、12、100 μg/kg添加水平下的加标回收率分别为9227%~10705%;噁喹酸在6、12、100 μg/kg添加水平下的加标回收率分别为10672%~11464%;氟甲喹在6、12、100 μg/kg添加水平下的加标回收率分别为9519%~10715%,具体见表5。诺氟沙星、环丙沙星、恩诺沙星、噁喹酸和氟甲喹的相对标准偏差RSD分别为141%、486%、850%、141%和421%,具体见表6。结果表明回收率稳定,精密度可满足检测需要。
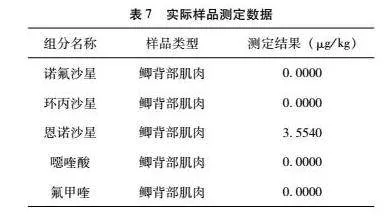
25 样品测定结果
本实验的水产品样品测定结果见表7,鲫背部肌肉中未检测出诺氟沙星、环丙沙星、噁喹酸和氟甲喹,恩诺沙星检测结果为35540 μg/kg。
3 讨论
不同的流动相对药物分离效果有着直接影响,本研究采用01%的甲酸水溶液和乙腈作为流动相,5种氟喹诺酮类药物分离效果较好。冯涛等[9]以pH=30的甲酸水溶液(002%)和乙腈作为流动相,环丙沙星、达氟沙星、恩诺沙星和沙拉沙星等4种氟喹诺酮类药物有着较好的分离度。兰承兴等[10]采用四丁基溴化铵和乙腈作为流动相,结果表明4种氟喹诺酮类药物的方法回收率和分离效果较好。这说明检测过程中pH值、流动相种类及其比例不是固定不变的,适当的调整和多次试验才能优化药物分离效果,后续研究可以考虑通过调整以上色谱条件,摸索出可分离更多种FQs药物、用时更短的色谱方法。
本研究利用T3色谱柱进行检测,与C18色谱柱相比,T3色谱柱具有更宽的pH值适用范围,具备应对复杂、多组分样品分离的能力,而本研究中流动相为01%甲酸溶液,选择T3色谱柱也能较大程度降低对色谱柱的损害。T3色谱柱已经被应用于多种化学药物残留检测领域,比如测定畜禽肉及内脏中的新生霉素、莫匹罗素、丰加霉素和茴香霉素[11],化妆品中葡糖酸、葡糖酸内酯和乳糖酸[12],保健品中的脂溶性维生素[13]等药物。
本研究选用T3色谱柱,以甲酸和乙腈为流动相对鲫背部肌肉中的5种FQs药物进行测定,分离效果好,检测灵敏度高,基线平稳,且流动相配制简单,适用于实际工作中水产品中FQs物质的检测。
参考文献
[1]周青青,杨清麟,李月,等. 新型氟喹诺酮衍生物对水产致病菌及其生物被膜的抑制作用研究[J].微生物学报,2023,63(8):3041-3053.
[2]李贞金,张洪昌,胡双庆,等. 2种氟喹诺酮类抗生素在水产养殖区沉积物上的吸附和解吸行为研究[J].生态毒理学报,2023,18(2):434-448.
[3]杨芳,马开立,杨帆. 达氟沙星在水产养殖中的研究进展[J].水产养殖,2023,44(5):74-77.
[4]农业农村部渔业渔政管理局,全国水产技术推广总站,中国水产学会. 2024中国渔业统计年鉴[M].北京:中国农业出版社,2024.
[5]许磊. 简述动物源食品中氟喹诺酮类药物残留的危害及检测方法[J].四川农业科技,2022(9):92-94.
[6]邓建朝,赵阳,贾博凡,等. 水产品中药物残留前处理及检测方法研究进展[J/OL].食品与发酵工业,1-10[2024-10-15]. https://doi.org/10.13995/j.cnki.11-1802/ts.038696.
[7]黄欣桐,王李宝,黎慧,等. 水产喹诺酮类药物使用与检测方法研究进展[J].水产养殖,2023,44(3):41-47.
[8]中华人民共和国农业农村部,中华人民共和国国家卫生健康委员会,国家市场监督管理总局. 食品安全国家标准 水产品中诺氟沙星、环丙沙星、恩诺沙星、氧氟沙星、噁喹酸、氟甲喹残留量的测定 高效液相色谱法:GB 31656.3—2021[S]. 北京:中国农业出版社,2021.
[9]冯涛,邬玲玲. 高效液相荧光法测定养殖水产中四种氟喹诺酮类药物残留[J].山西化工,2019,39(6):33-34+38.
[10]兰承兴,田雪莲,周开拓,等. 优化高效液相色谱法对水产品中4种氟喹诺酮类药物残留的检测[J].贵州畜牧兽医,2018,42(2):25-29.
[11]申雷,柳溪,羊银,等. Captiva EMR-Lipid技术结合液相色谱-串联质谱法测定畜禽肉及内脏中4种抗生素残留[J].食品安全质量检测学报,2024,15(11):220-229.
[12]张丽媛,程巧鸳,陈岑,等. 高效液相色谱法测定化妆品中3种α-羟基酸及其酯[J].日用化学工业,2024,54(1):102-106.
[13]吴琴,余家胜,李瑞,等. 超高效液相色谱-串联质谱法同时测定复杂基质保健食品中7种脂溶性维生素营养补充剂的含量[J].理化检验(化学分册),2024,60(2):187-193.
