特瑞普利单抗联合紫杉醇治疗转移性或复发性三阴性乳腺癌的成本-效果分析
2025-02-15闫文英陶心悦冯冰


关键词特瑞普利单抗;三阴性乳腺癌;成本-效果分析;药物经济学;分区生存模型
乳腺癌是女性高发恶性肿瘤之一,近年来其发病率增长快速并且逐渐呈现年轻化趋势,已代替肺癌成为全球女性第一大癌症[1]。三阴性乳腺癌(triple-negativebreastcancer,TNBC)患者约占乳腺癌人群的15%~20%,具有侵袭性高、预后差、易局部复发和远处转移、生存率低等特点[2]。长期以来,TNBC患者只能选择手术、放疗和化疗等常规治疗方案,这些方案虽然有一定的效果,但是对TNBC患者来说疗效仍不佳。
近年来,免疫治疗药物的出现及其应用为多种肿瘤的治疗提供了新的治疗方法[3]。免疫检查点抑制剂是一类针对肿瘤的免疫治疗药物,其主要作用机制是通过阻断一类被称为免疫检查点的蛋白质,恢复免疫系统对肿瘤细胞的杀伤能力,从而起到治疗肿瘤的作用[4]。TORCHLIGHT试验是一项随机、双盲的3期临床试验,该试验评估了特瑞普利单抗或安慰剂联合紫杉醇(白蛋白结合型)治疗转移性或复发性TNBC的疗效和安全性。该研究最新公布的结果显示,与安慰剂联合紫杉醇(白蛋白结合型)相比,特瑞普利单抗联合紫杉醇(白蛋白结合型)的中位无进展生存期(progression-freesurvival,PFS)[8.4个月vs.6.9个月,风险比(HR)=0.773,95%置信区间(CI)(0.602,0.994)]和中位总生存期(overallsurvival,OS)[33.1个月vs.23.5个月,HR=0.691,95%CI(0.513,0.932)]均显著改善,且两组间≥3级的治疗相关不良反应发生率相似,安全性可控[5],表明该方案临床获益显著。
特瑞普利单抗作为国内首个获批上市的国产程序性死亡受体1(programmeddeath-1,PD-1)单抗于2020年12月被纳入我国医保目录,广泛应用于多个瘤种的治疗。2024年4月,特瑞普利单抗联合紫杉醇(白蛋白结合型)方案被《中国晚期乳腺癌规范诊疗指南(2024版)》推荐作为晚期TNBC的解救治疗方案;当年6月,特瑞普利单抗联合紫杉醇(白蛋白结合型)治疗程序性死亡受体配体1(programmeddeath-ligand1,PD-L1)阳性[联合阳性分数(combinedpositivescore,CPS)≥1]的初治转移或复发转移性TNBC的适应证成功获批;2025年1月,该适应证又被2024年版国家医保目录收录。考虑到TNBC患者长期以来的用药方案较为单一,而最新的TORCHLIGHT试验也已证实特瑞普利单抗联合紫杉醇(白蛋白结合型)在治疗中带来的良好获益,因此本研究基于TORCHLIGHT试验,利用三状态分区生存模型,从我国卫生体系角度出发,对特瑞普利单抗联合紫杉醇(白蛋白结合型)治疗转移性或复发性TNBC进行成本-效果分析,以期为临床用药提供参考。
1 资料与方法
1.1 目标人群
目标人群的入选标准与治疗措施与TORCHLIGHT试验(NCT04085276和NCT03777579)一致。受试人群的主要纳入标准为经组织学证实的TNBC患者、根据TNM临床分类法首诊为肿瘤Ⅳ期或不适合进行手术治疗的局部晚期TNBC以及一线化疗失败的患者;其他纳入标准包括:至少有1个基于实体瘤疗效评价标准(ResponseEvaluationCriteriainSolidTumors,RECIST)v.1.1的可测量病灶,美国东部肿瘤协作组体力状态评分(EasternCooperativeOncologyGroupperformancestatus,ECOGPS)为0或1分,器官功能正常。主要排除标准包括:有抗PD-1/PD-L1/PD-L2/细胞毒性T淋巴细胞相关抗原4(cytotoxicTlymphocyte-associatedantigen-4,CTLA-4)治疗史,存在活动性或未经治疗的脑转移和活动性自身免疫性疾病,或有需要全身治疗的自身免疫性疾病病史。TORCHLIGHT试验入组患者共531例,其中特瑞普利单抗组353例、对照组178例。特瑞普利单抗组患者的中位年龄为53.0岁,对照组患者的中位年龄为54.5岁。入组患者中,处于M0期的人数占比为6.2%,处于M1期的人数占比为93.8%。
1.2 干预措施
两组患者均以21d为1个用药周期,所有患者均在每周期的第1天静脉滴注特瑞普利单抗注射液240mg[上海君实生物工程有限公司,国药准字S20191003,规格:80mg(2mL)/瓶]或安慰剂,每周期的第1天和第8天静脉滴注紫杉醇(白蛋白结合型)125mg/m2。假设所有患者均接受本研究方案治疗直至疾病进展(progressivedisease,PD)或出现不可耐受的不良事件,之后患者接受后续治疗方案直至死亡。由于该研究并未公开后续治疗方案,根据中国临床肿瘤学会《乳腺癌诊疗指南(2023)》[6],本研究假设所有患者均选择吉西他滨联合顺铂作为二线治疗方案,用药周期为28d,在每周期的第1天和第8天静脉滴注吉西他滨1000mg/m2,在每周期的第2天静脉滴注顺铂75mg/m2。
1.3 模型结构
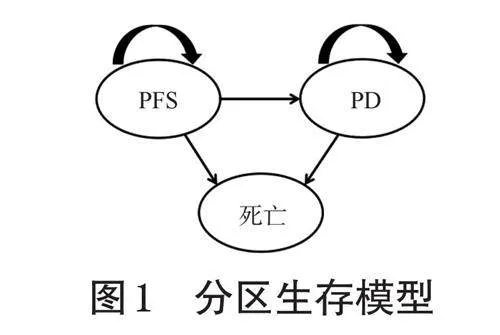
分区生存模型是一种经济学模型,该模型通常基于临床试验报告的PFS曲线和OS曲线,将患者的健康状态划分为PFS、PD和死亡3个状态。生存曲线中的曲线下面积可用于估计效果和成本[7]。假设所有患者进入模型时均处于PFS状态,模型循环周期设为21d,与给药周期保持一致。考虑到TNBC患者的5年预后较差,转移性复发概率高,且晚期TNBC的3年总生存率仅为22%~36%[8],所以本研究设置模型模拟时限为10年。假设患者在每个周期中只能处于1种健康状态并接受相应的治疗,且PD状态以后的患者不能返回上一级健康状态。各周期中各健康状态下的患者人数由生存曲线计算得出,分区生存模型结构见图1。采用成本-效果分析法来分析两种方案的经济性,以质量调整生命年(quality-adjustedlifeyear,QALY)作为模型产出指标,通过计算增量成本-效果比(incrementalcost-effectiveratio,ICER)并与本研究设定的意愿支付(willingness-topay,WTP)阈值比较,以判断方案的经济性。本研究采用5%的年贴现率对成本及健康产出数据进行贴现处理[9];以3倍我国2023年人均国内生产总值(grossdomesticproduct,GDP)作为WTP阈值,即268074元/QALY。
1.4 生存分析
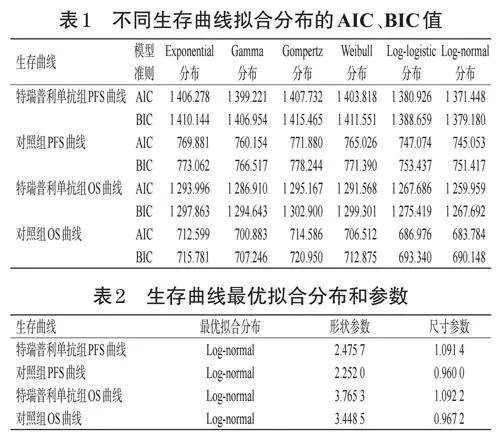
本研究首先利用GetData2.26软件从生存曲线中取点,然后利用R语言的生存分析数据包对患者个体水平数据进行重构,再对生存曲线进行相应的参数分布拟合,包括Exponential、Weibull、Gamma、Gompertz、Loglogistic和Log-normal分布等。最优拟合结果根据赤池信息准则(Akaikeinformationcriterion,AIC)和贝叶斯信息准则(Bayesianinformationcriterion,BIC)判断,再根据分布参数计算患者的长期生存函数。不同生存曲线拟合分布的AIC、BIC值见表1,最优拟合分布和参数见表2。
1.5 成本和效用数据
本研究从我国卫生体系角度出发,故只考虑直接医疗成本,包括药品成本、药品管理成本、疾病管理成本及不良反应处理成本。根据《中国居民营养与慢性病状况报告(2020)》,我国女性平均身高为158cm,平均体重为59kg,算得我国女性平均体表面积为1.62m2[10],本研究据此计算药物的治疗成本。药品成本为药智网2021-2024年全国各省市药品挂网与中标价格的中位值,药品管理成本包含门诊费、静脉输液费;疾病管理成本包括护理费、床位费、肿瘤影像学检查费和实验室检查费。根据TORCHLIGHT试验的不良反应统计结果,本研究仅考虑≥3级且发生率>20%的不良反应。考虑到患者治疗过程中发生不良反应时,医生会进行换药处理,故本研究中不良反应处理成本仅计入1次。药品不良反应发生率来自TORCHLIGHT试验,药品管理成本和不良反应处理成本均来源于已发表文献[11―15],PFS、PD状态的效用值和不良反应的负效用值来自文献[14―15]。模型参数及分布见表3。
1.6 敏感性分析
本研究采用单因素敏感性分析和概率敏感性分析,以验证模型结果的稳健性。单因素敏感性分析用于评估单个变量对结果指标ICER影响的大小,结果采用旋风图表示[16]。概率敏感性分析考虑了各模型参数变化对结果的影响,先对不同的参数按预先设置的特定分布进行计算,再通过1000次蒙特卡罗模拟迭代,获得成本-效果散点图和成本-效果可接受曲线。用于敏感性分析的参数的变化范围和分布类型见表3。
2 结果
2.1 基础分析结果
基础分析结果显示,在本研究模拟时限内,相较于安慰剂+紫杉醇(白蛋白结合型)方案,特瑞普利单抗+紫杉醇(白蛋白结合型)方案的增量效果为0.568QALYs,增量成本为100207.59元,ICER为176347.17元/QALY,低于本研究设定的WTP阈值(268074元/QALY),所以特瑞普利单抗+紫杉醇(白蛋白结合型)对比安慰剂+紫杉醇(白蛋白结合型)方案治疗转移性或复发性TNBC具有经济性。结果见表4。
2.2 敏感性分析结果
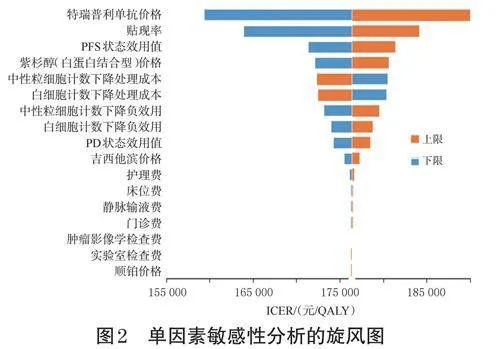
单因素敏感性分析结果见图2。由图2可知,特瑞普利单抗注射液价格、贴现率、PFS状态效用值以及紫杉醇(白蛋白结合型)价格对结果影响较大,其他参数如PD状态效用值、二线治疗药物成本、护理费、床位费等对结果的影响较小。所有参数的变化并未使结果发生翻转,表明基础分析结果较为稳健。
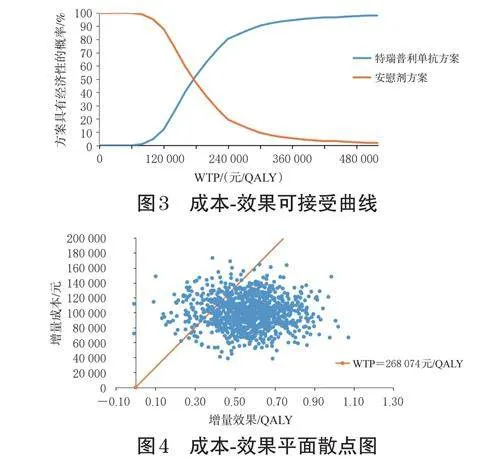
概率敏感性分析通过1000次蒙特卡罗模拟,得到特瑞普利单抗+紫杉醇(白蛋白结合型)方案对比安慰剂+紫杉醇(白蛋白结合型)方案的成本-效果可接受曲线和成本-效果散点图,分析结果分别见图3、图4。如图3所示,在3倍人均GDP的WTP阈值水平下,特瑞普利单抗+紫杉醇(白蛋白结合型)方案具有经济性的概率为85.5%,且该概率随着WTP阈值的增加而逐渐升高:当WTP阈值降至180000元/QALY时,该方案具有经济性的概率仍超过50%。概率敏感性分析结果也提示基础分析结果稳定,表明模型稳定性良好。
3 讨论
TNBC恶性程度高、预后差、总体治疗手段有限。近年来免疫治疗的巨大成功对TNBC的治疗具有重大意义[17]。特瑞普利单抗的关键性临床研究TORCHLIGHT试验,是国内首个在晚期TNBC免疫治疗领域取得阳性结果的3期临床试验[5]。本研究利用该研究数据,结合相关文献及国内医疗资源现状,对特瑞普利单抗联合紫杉醇(白蛋白结合型)治疗转移性或复发性TNBC的经济性进行了分析。PD-L1单抗类药物经国谈后已大幅降价,特瑞普利单抗的价格降幅超过60%。本研究结果显示,与安慰剂联合紫杉醇(白蛋白结合型)相比,特瑞普利单抗联合紫杉醇(白蛋白结合型)方案虽然成本更高,但获得的效果更好,表明特瑞普利单抗给患者带来了更多的临床获益,在以3倍我国2023年人均GDP为WTP阈值时,特瑞普利单抗联合紫杉醇(白蛋白结合型)方案更具经济性。单因素敏感性分析显示,特瑞普利单抗价格是影响ICER的重要因素。现如今特瑞普利单抗联合紫杉醇(白蛋白结合型)治疗转移性或复发性TNBC的适应证已在我国获批,并已被纳入医保目录,TNBC患者的治疗负担将进一步减轻。
除此之外,资料显示,在TORCHLIGHT试验未公开最终数据时,便已有英文文献研究了特瑞普利单抗联合紫杉醇(白蛋白结合型)方案治疗转移性或复发性TNBC的经济性[18]。由于该文献发表时间较早,缺少试验的不良反应具体数据以及处理成本,针对其不足,本文选取最新的药品价格以及不良反应处理成本进行分析,使得研究结果更符合当前决策环境。但本研究尚存在不足之处:(1)本研究通过参数法外推生存曲线可能会增加模型的不确定性。(2)本研究仅纳入了3级及以上且发生率较高的不良反应,可能会与实际结果存在部分差异。(3)本研究假设患者在PD后使用吉西他滨加顺铂的方案进行二线治疗,但在真实诊疗环境中,二线治疗方案可能因患者个体差异而不同。不过单因素敏感性分析结果显示,不良反应处理成本及二线治疗成本对本研究方案的经济性影响甚微,因此本研究结果依然具有稳健性。
综上所述,在以3倍我国2023年人均GDP作为WTP阈值的前提下,相比于安慰剂联合紫杉醇(白蛋白结合型)方案,特瑞普利单抗联合紫杉醇(白蛋白结合型)方案治疗转移性或复发性TNBC具有经济性,是TNBC患者的良好选择。
