孟河医派大黄煨制工艺优化及炮制后化学成分含量变化研究
2025-01-15薛江林刘雨欣钟佩刘产明陆兔林李林颜晓静朱月琴华丰黄玮





关键词煨大黄;大黄;层次分析;熵权法;正交实验;成分变化规律;孟河医派
大黄为蓼科植物掌叶大黄RheumpalmatumL.、唐古特大黄Rheum.tanguticumMaxim.exBalf.或药用大黄RheumofficinaleBaill.的干燥根及根茎,具有泻下攻积、清热泻火、凉血解毒、逐瘀通经、利湿退黄的功效[1]。生大黄苦寒之性甚强,泻下作用峻烈,久服易引起腹痛、恶心等胃肠道反应[2],临床常以炮制品入药。煨大黄是孟河医派的特色饮片,大黄经煨制后,泻下作用减弱,且活血化瘀、消肿止痛作用增强,可治疗各类伤症[3―5],而有缓性增效的作用。
传统大黄的煨制方法多以湿纸裹后埋入热火灰中进行加热,由于火候温度不可控,导致煨大黄的质量控制较为困难。现代煨大黄研究常以烘箱作为加热源,采用恒温方式进行加热[6],但烘箱中水分蒸发速率过快,与传统煨制方法存在一定差异。此外,历版《中国药典》以及各地方炮制规范均未收录煨大黄,因此煨大黄的相关炮制方法以及工艺参数尚不明确。基于此,本研究以外观性状评分以及5-羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)、没食子酸、番泻苷A+番泻苷B、游离蒽醌、结合蒽醌的含量为评价指标,采用主观评价的层次分析(analytichierarchyprocess,AHP)法和客观评价的熵权法结合正交实验[7],优选大黄最优煨制工艺,同时采用高效液相色谱(HPLC)法对大黄煨制前后的5种蒽醌类成分(芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚)、5种蒽醌苷类成分(芦荟大黄素苷、大黄酸苷、大黄素苷、大黄酚苷和大黄素甲醚苷)、2种番泻苷类成分(番泻苷A和番泻苷B)以及没食子酸和5-HMF的含量进行对比分析,以期为大黄煨制工艺研究及煨制后化学成分变化规律的阐明提供参考依据。
1 材料
1.1 主要仪器
本研究所用主要仪器有Aglient1260Ⅱ型高效液相色谱仪(美国Aglient公司),XSR105DU型十万分之一分析天平、ME204型万分之一分析天平(瑞士Mettler-Toledo公司),IQ7003型Milli-Q纯水仪(美国Millipore公司),R201C型旋转蒸发仪(巩义市英峪高科仪器厂),DZG-6090型减压干燥仪(上海培因实验仪器有限公司)。
1.2 主要药品与试剂
大黄饮片(批号231024,产地甘肃)购自苏州市天灵中药饮片有限公司,经南京中医药大学常州附属医院药学部主任中药师刘产明鉴定为蓼科植物掌叶大黄R.palmatumL.的干燥根和根茎。对照品没食子酸、5-HMF、番泻苷A、番泻苷B、芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚(批号分别为B20851、B21832、B20380、B20381、B20772、B20245、B20240、B20238、B20242,纯度均大于97%)均购自上海源叶生物科技有限公司;甲醇、碳酸氢钠、氯仿、磷酸均为分析纯;甲醇、四氢呋喃为色谱纯;水为纯化水。草木灰采自农家土灶,粗草纸购自常州市天宁区农贸市场。
2 方法与结果
2.1 大黄煨制方法
取大黄饮片80g,用湿纸包裹后,放置一定时间,再埋入热火灰中,然后一并置于烤箱中,先以大火(250~300℃)煨制一定时间后转文火(120~160℃)煨制,炮制一定时间后取出打开,放凉,即得煨大黄样品。
2.2 没食子酸和5-HMF的含量测定方法建立
2.2.1 混合对照品溶液的制备
精密称取没食子酸对照品14.30mg、5-HMF对照品14.60mg,加50%甲醇定容于不同10mL容量瓶中,配制成含没食子酸1.43mg/mL、5-HMF1.46mg/mL的对照品储备液;分别精密吸取没食子酸、5-HMF对照品储备液3.20、0.28mL,混合,加50%甲醇制成没食子酸和5-HMF质量浓度分别为457.60、40.88μg/mL的混合对照品溶液。
2.2.2 供试品溶液的制备
取生大黄(或煨大黄)粉末0.3g(过四号筛),精密称定,置具塞锥形瓶中,精密加入50%甲醇25mL,密塞,称定质量;超声(功率500W,频率40kHz,下同)提取30min,放冷,再称定质量;以50%甲醇补足减失质量,摇匀,滤过,取续滤液过0.22μm微孔滤膜,即得。
2.2.3 色谱条件、系统适用性试验与方法学考察
本实验色谱条件参考文献[8]设置,以AgilentZorbaxODSC18(250mm×4.6mm,5μm)为色谱柱,以甲醇-0.1%磷酸溶液(V/V,8∶92)为流动相进行等度洗脱,流速为0.8mL/min;柱温为25℃,检测波长为273nm,进样量为10μL,洗脱时间为18min。分别吸取空白对照溶液(50%甲醇)和“2.2.1”“2.2.2”项下混合对照品溶液、煨大黄供试品溶液适量进样测定,记录色谱图。结果显示,各成分分离度均大于1.5,理论板数按没食子酸峰计均不低于10000,空白对照溶液对测定无干扰,具体见图1(空白对照溶液图略)。参考2020年版《中国药典》(三部)9101分析方法验证指导原则[9]进行方法学考察。结果显示,没食子酸和5-HMF的回归方程分别为Y=36.025X-120.490、Y=72.793X-2.000(r≥0.9992),线性范围分别为3.575~457.600、0.320~40.880μg/mL;精密度试验、重复性试验、稳定性试验(24h)的RSD均小于2.00%(n=6);平均加样回收率分别为103.3%、98.75%(RSD分别为0.44%、0.36%,n=6)。以上均符合指导原则相关要求。
2.3 番泻苷A和番泻苷B的含量测定方法建立
2.3.1 混合对照品溶液制备
精密称取番泻苷A对照品7.06mg和番泻苷B对照品8.59mg,加0.1%碳酸氢钠溶液定容于不同10mL容量瓶中,配制成含番泻苷A0.706mg/mL、番泻苷B0.859mg/mL的对照品储备液;分别精密吸取番泻苷A、番泻苷B对照品储备液1.40、0.60mL,混合,加0.1%碳酸氢钠溶液制成番泻苷A、番泻苷B质量浓度分别为98.84、51.54μg/mL的混合对照品溶液。
2.3.2 供试品溶液制备
取生大黄(或煨大黄)粉末约0.5g(过四号筛),精密称定,置于具塞锥形瓶中,加0.1%碳酸氢钠溶液25mL,称定质量;超声提取30min,取出放冷后补足减失质量,摇匀,滤过,取续滤液,过0.22μm微孔滤膜,即得。
2.3.3 色谱条件、系统适用性试验与方法学考察
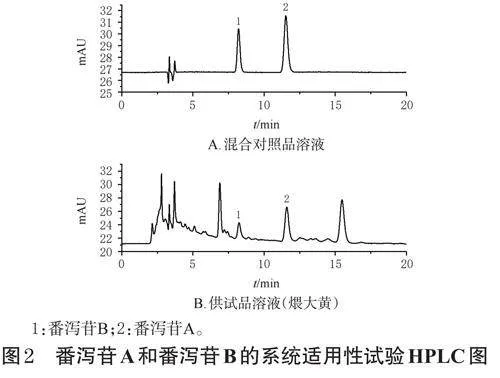
本实验色谱条件参考文献[10]设置。以AgilentZorbaxODSC18(250mm×4.6mm,5μm)为色谱柱,以四氢呋喃-水-乙酸(V/V/V,2∶80∶1.5)为流动相进行等度洗脱,检测波长为380nm,流速为0.8mL/min,柱温为30℃,进样量为10μL,洗脱时间为20min。分别吸取空白对照溶液(0.1%碳酸氢钠溶液)和“2.3.1”“2.3.2”项下混合对照品溶液和供试品溶液(煨大黄)适量进样测定,记录色谱图。结果显示,各成分分离度均大于1.5,理论板数按番泻苷B峰计均不低于7000,空白对照溶液对测定无干扰,具体见图2(空白对照溶液图略)。参考2020年版《中国药典》(三部)9101分析方法验证指导原则[9]进行方法学考察。结果显示,番泻苷A和番泻苷B的回归方程分别为Y=7.6407X-1.9066、Y=8.5195X-1.3115(r≥0.9999),线性范围分别为3.090~98.840、1.610~51.540μg/mL;精密度试验、重复性试验、稳定性试验(24h)的RSD均小于2.00%(n=6);平均加样回收率分别为99.11%、97.12%(RSD分别为1.79%、1.32%,n=6)。以上均符合指导原则相关要求。
2.4 游离蒽醌和结合蒽醌的含量测定方法建立
游离蒽醌和总蒽醌的含量均以芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚5种成分的总量计,结合蒽醌的含量以芦荟大黄素苷、大黄酸苷、大黄素苷、大黄酚苷和大黄素甲醚苷5种成分的总量计(但定量分析时,各蒽醌苷类成分含量以对应苷元含量计),其中结合蒽醌含量=总蒽醌含量-游离蒽醌含量。
2.4.1 混合对照品溶液的制备
精密称取芦荟大黄素对照品0.40mg、大黄酸对照品0.84mg、大黄素对照品0.52mg、大黄酚对照品1.84mg、大黄素甲醚对照品0.44mg,加甲醇定容至同一10mL容量瓶中,制成含芦荟大黄素0.040mg/mL、大黄酸0.084mg/mL、大黄素0.052mg/mL、大黄酚0.184mg/mL、大黄素甲醚0.044mg/mL的混合对照品溶液。
2.4.2 供试品溶液制备
(1)游离蒽醌供试品溶液的制备:取生大黄(或煨大黄)粉末约0.5g(过四号筛),精密称定,置于具塞锥形瓶中,精密加入甲醇25mL,称定质量;加热回流1h,放冷,再次称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,过0.22μm微孔滤膜,即得。(2)总蒽醌供试品溶液的制备:取生大黄(或煨大黄)粉末约0.15g(过四号筛),精密称定,置于具塞锥形瓶中,精密加入甲醇25mL,称定质量;加热回流1h,放冷,再次称定质量,用甲醇补足减失的质量,摇匀,滤过;精密量取续滤液5mL,置于烧瓶中,挥去溶剂,加8%盐酸溶液10mL,超声处理2min;再加三氯甲烷10mL,加热回流1h,放冷,置于分液漏斗中,再用少量三氯甲烷洗涤容器,洗涤液并入分液漏斗中,取三氯甲烷层;再用三氯甲烷提取3次,每次10mL,合并三氯甲烷液,减压回收溶剂至干;残渣加甲醇使溶解,转移至10mL容量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,过0.22μm微孔滤膜,即得。
2.4.3 色谱条件、系统适用性试验与方法学考察
本实验色谱条件参考文献[11]设置。以AgilentZorbaxODSC18(250mm×4.6mm,5μm)为色谱柱,以甲醇-0.1%磷酸溶液(V/V,85∶15)为流动相进行等度洗脱,检测波长为254nm,流速为1.0mL/min,柱温为30℃,进样量为10μL,洗脱时间为15min。分别吸取空白对照溶液(甲醇)和“2.4.1”“2.4.2”项下混合对照品溶液、煨大黄游离蒽醌和总蒽醌供试品溶液适量进样测定,记录色谱图。结果显示,各成分分离度均大于1.5,理论板数按大黄酸峰计均不低于9000,空白对照溶液对测定无干扰,具体见图3(空白对照溶液图略)。参考2020年版《中国药典》(三部)9101分析方法验证指导原则[9]进行方法学考察,结果显示,芦荟大黄素、大黄酸、大黄素、大黄酚和大黄素甲醚的回归方程分别为Y=44.288X+4.203、Y=28.356X+1.587、Y=27.553X+1.356、Y=39.703X+20.806、Y=32.660X+1.431(r≥0.9999),线性范围分别为0.020~0.480、0.042~1.008、0.026~0.624、0.092~2.208、0.022~0.528μg;精密度试验、游离蒽醌的重复性试验和稳定性试验(24h)、总蒽醌的重复性试验和稳定性试验(24h)的RSD均小于3.00%(n=6);游离蒽醌的平均加样回收率分别为97.35%、101.94%、100.89%、98.40%、99.50%(RSD分别为0.69%、3.05%、1.85%、0.66%、0.87%,n=6);总蒽醌的平均加样回收率分别为98.01%、100.97%、97.16%、98.59%、97.38%(RSD分别为1.02%、3.32%、2.28%、0.65%、1.27%,n=6)。以上均符合指导原则相关要求。
2.5 外观性状评价标准
笔者根据古籍中“大黄湿纸裹煨勿令焦”“大黄湿纸包,煨令香熟”“湿纸裹煨至纸焦”等相关描述,并参考相关文献的评分方法[6,11],对煨大黄的纸张性状、饮片气味、颜色以及质地进行评分,具体标准为:当饮片浓香、较硬、呈深棕黄色且纸焦时,记为3分;当饮片清香、较软、呈黄褐色且纸干时,记为2分;当饮片焦香、轻脆、呈焦褐色且纸湿时,记为1分。
2.6 AHP-熵权法计算煨大黄的综合评分
2.6.1 AHP确定权重rj
煨大黄作为古代应用普遍但现代已经失传的炮制品种,外观性状特征对其质量评价具有重要作用,因此在AHP中设置最高权重;游离蒽醌是2020年版《中国药典》中大黄质量评价的重要指标,也是大黄发挥活血化瘀作用的主要药效成分[12];结合蒽醌和番泻苷类是大黄及其炮制品发挥泻下作用的主要药效成分[13―14];没食子酸是大黄发挥收敛止血、抗炎作用的主要药效成分,且大黄煨制后该成分含量变化较大[15];5-HMF具有多种药理活性但有一定毒副作用[16],故在AHP中设置最低权重。最终确认各指标重要程度依次为外观形状评分>游离蒽醌含量=结合蒽醌含量>番泻苷A+番泻苷B含量>没食子酸含量>5-HMF含量,构建各指标的优先判断矩阵,并根据方根法计算各指标的rj,具体见表1。进一步对矩阵进行一致性检验发现,一致性参数λmax=6.072,一致性指标=0.014,一致性比率=0.011<0.1,表明矩阵合理有效,权重系数可靠。
2.6.2 熵权法确定权重wj
将测得数据代入相应公式计算,其中,正向指标代入Yij=(Xij-Xmin)/(Xmax-Xmin),负向指标代入Yij=(Xmax-Xij)/(Xmax-Xmin)中,式中,Yij为j指标下第i个数值的标准化值,Xij为第i次实验时第j个指标的测定值,Xmin为该组测定值中的最小值,Xmax为该组测定值中的最大值。将标准化数据矩阵(Yij)转化为概率矩阵(Pij),Pij=Yij/Σi=1nYij;再求各指标信息熵(Hj),Hj=-kΣi=1nPijlnPij,k=1/lnn(n为样本量);然后采用熵权法计算各指标权重wj,wj=(1-Hj)/Σj=1m(1-H)j。
2.6.3 综合评分的计算方法
用AHP法得到的rj、熵权法得到的wj,计算综合权重(Fj),Fj=rjwj/Σj=1mrjwj。结果显示,外观性状评分和5-HMF、没食子酸、番泻苷A+番泻苷B、游离蒽醌、结合蒽醌含量的Fj分别为0.235、0.115、0.068、0.182、0.156、0.244,然后计算综合评分(M),M=0.235×100×外观性状评分/外观性状评分最大值+0.115×100×5-HMF含量/5-HMF含量最大值+0.068×100×没食子酸含量/没食子酸含量最大值+0.182×100×(番泻苷A+番泻苷B)含量最小值/(番泻苷A+番泻苷B)含量+0.156×100×游离蒽醌含量/游离蒽醌含量最大值+0.244×100×结合蒽醌含量最小值/结合蒽醌含量。
2.7 大黄煨制工艺的优选
结合本研究前期预实验,选取文火温度、煨制时间、纸张层数、纸裹时间为考察因素,以外观性状评分以及没食子酸、5-HMF、番泻苷A+番泻苷B、结合蒽醌、游离蒽醌含量为评价指标,采用AHP-熵权法计算综合评分M,再根据正交实验优选大黄煨制工艺。
2.7.1 正交实验设计与结果
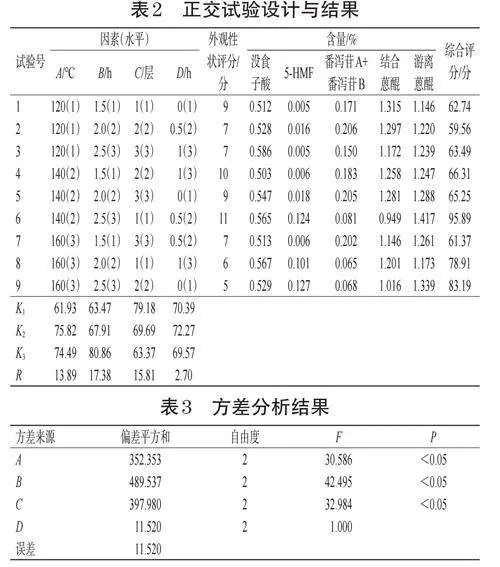
根据预实验中不同煨大黄饮片的外观性状筛选出部分适宜条件:固定大火温度加热时间为20min,文火温度(A)取120、140、160℃3个水平,煨制时间(B)取1.5、2、2.5h3个水平,纸张层数(C)取1、2、3层3个水平,纸裹时间(D)取0、0.5、1h3个水平,进行4因素3水平的L(934)正交实验。具体方案与结果见表2,方差分析结果见表3。
由表2、表3可知,各因素影响大小顺序为B>C>A>D,且因素A、B、C对煨大黄质量均有显著影响,因此最终确定最优的工艺为A2B3C1D2,即每80g大黄用1层湿纸包裹0.5h,大火煨制20min后转文火140℃煨制,总煨制时间2.5h。
2.7.2 验证实验
按“2.7.1”项下最优工艺制备煨大黄样品,进行3次验证实验。结果显示,3次验证实验的综合评分均值为94.10,RSD小于1.0%,表明优化工艺稳定、可行。验证实验结果见表4。
2.8 大黄煨制后化学成分变化研究
取生大黄饮片及“2.7.1”项下按最优工艺制备煨大黄饮片适量,按“2.2”~“2.4”项下方法测定其中5种蒽醌类成分、5种蒽醌苷类成分、2种番泻苷类成分以及没食子酸和5-HMF的含量(平行测定3次),并分析含量变化情况[含量变化=(炮制后成分含量-炮制前成分含量)/炮制前成分含量×100%]。结果显示,大黄煨制后5种蒽醌苷类成分和2种番泻苷类成分的含量均大幅降低,而5种游离蒽醌类成分和没食子酸含量均不同程度升高,且新生成了5-HMF,表明煨制过程会导致大黄化学成分发生转化。结果见表5。
3 讨论
《通俗文》记载的“热灰谓之煻煨”,是将药物包裹后置于炭火或柴火的余烬中缓慢加热至一定程度的炮制方法。孟河医派古籍中也以“热火灰煨”或“煻火煨”描述煨法。这种煨制方法工艺繁琐,条件不易控制,且有安全隐患,不适于现代生产。本课题组前期比较了目前主流的湿纸裹煨法、湿纸裹后烘箱直接加热法以及热沙煨制法[6,17],发现这些方法煨制的大黄与古籍中煨大黄的性状记载均有较大差异,因此本研究选择保温保湿性能较好的热火灰,用烤箱代替火源,并模拟古法炮制真实的温度变化,采取先大火加热后文火加热的方式进行煨制,并在此基础上对大黄的煨制工艺进行优化,结果显示,大黄的最优煨制工艺为:每80g大黄用1层湿纸包裹0.5h,大火煨制20min后转文火140℃煨制,总煨制时间2.5h。
大黄煨制后5种蒽醌类成分、5种蒽醌苷类成分、2种番泻苷类成分以及没食子酸和5-HMF的含量均发生明显变化,其中蒽醌苷类和番泻苷类成分含量大幅降低,而游离蒽醌含量升高,这可能是由于大黄煨制过程中,番泻苷类成分结构被破坏,蒽醌苷类成分受热易分解为相应的苷元;没食子酸含量的升高可能是大黄中缩合鞣质与可水解鞣质的化学键在高温下断裂形成了单体成分没食子酸[18]。5-HMF是大黄中糖类成分发生焦糖化反应的产物,一定程度上可以反映炮制程度和产品质量,且具有抗氧化、改善血液流变学等药理活性[8,16]。研究表明,蒽醌类成分中的糖苷键可以保护苷元不被小肠水解吸收以顺利进入结肠,刺激肠道而致泻[19];番泻苷A可通过调控肠道菌群和水通道蛋白表达发挥泻下作用[20];大黄素、芦荟大黄素、大黄素甲醚等可作用于内皮型一氧化氮合酶等关键靶点,发挥活血化瘀作用[12];没食子酸对角叉菜胶诱导的急性炎症大鼠具有良好的抗炎消肿止痛作用[21]。由此表明,大黄煨制过程中,蒽醌苷类和番泻苷类成分的分解和破坏可能是煨大黄苦寒泻下作用减轻的主要原因,而没食子酸和游离蒽醌含量的升高可能是煨大黄发挥活血化瘀作用的物质基础,这也与煨大黄在孟河医派中的临床应用一致。
综上所述,本研究成功优化了大黄的煨制工艺,并分析了大黄煨制后的化学成分含量变化,可为大黄煨制工艺的深入研究及煨制过程中化学成分变化规律的阐明奠定基础。
