黄铁矿在组氨酸、赖氨酸、精氨酸中的电化学氧化机理研究
2024-10-30薛旭东张炎






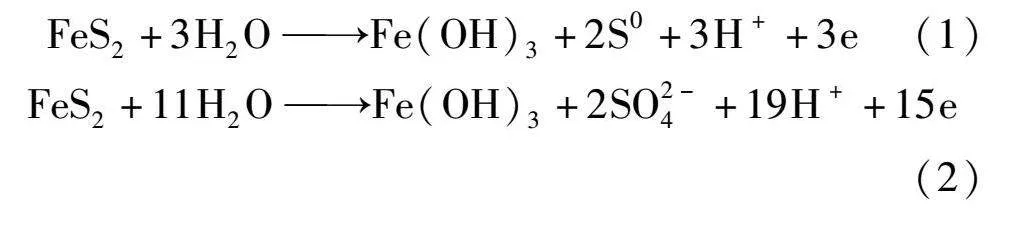









摘要:黄铁矿开采冶炼过程中会产生尾矿废渣,暴露的金属硫化物被氧化后产生的酸性矿山废水污染等环境问题突出。研究黄铁矿的氧化机理,对抑制或阻止酸性矿山废水产生具有重要意义。采用碱性氨基酸作为电解质研究黄铁矿的电化学氧化机理,利用OCP、CV、Tafel极化曲线、LSV、EIS等电化学方法对黄铁矿表面的电化学行为进行测量,验证了黄铁矿在碱性氨基酸体系中氧化的可行性,黄铁矿在3种碱性氨基酸中氧化机理一致,最终发现,黄铁矿在电解质溶液中的氧化速率为赖氨酸>精氨酸>组氨酸。
关键词:黄铁矿;组氨酸;赖氨酸;精氨酸;氧化机理;电化学氧化
中图分类号:TD98文章编号:1001-1277(2024)10-0084-07
文献标志码:Adoi:10.11792/hj20241014
引言
黄铁矿是一种含硫矿石,化学式为FeS2,常与其他矿石共生,尤其是黄铜矿、闪锌矿和黝铜矿等硫化物矿石[1]。黄铁矿中含有微量的钴、镍、铜、金、硒等元素,含量较高时可以在提取硫过程中综合回收和利用。在矿山开采冶炼过程引发的环境问题中,酸性矿山废水是目前最受关注的矿山污染问题之一,它会污染水体、土壤等,影响生物多样性,从而危及人类健康[2]。目前,矿山普遍认为黄铁矿是酸性矿山废水的主要来源。因此,黄铁矿的开采和利用也面临着越来越大的挑战。矿山企业开始寻求更加环保、节能的开采和利用方法,同时也在努力减少黄铁矿的浪费和污染。
当黄铁矿表面暴露在空气中时,会与氧气和水分子发生反应,这个过程被称为黄铁矿的表面电化学氧化,该过程中黄铁矿中的Fe(Ⅱ)被氧化成Fe(Ⅲ),并且在水分子存在条件下发生酸化。HOLMES等[3]研究结果显示,黄铁矿具有半导体特性,其氧化实质上是一种电化学过程[4]。电化学可间接反映金属硫化物氧化过程,被广泛用于研究黄铁矿氧化的动力学和机理。BIEGLER等[5]采用阳极极化法研究黄铁矿在酸性条件下的氧化,发现黄铁矿半导体结构对其阳极氧化动力学无影响,氧化产物为Fe3+、S0和 SO2,研究认为S0是电化学惰性物质,并不是形成SO2的中间物质,升高电压无法将其氧化为SO2-4。然而,KELSALL等[6]认为,黄铁矿半导体结构限制了其氧化速率,且在高电位下氧化形成SO2-4,阳极电压升高,黄铁矿价带产生的空穴氧化性变强,导致吸附于电极表面的H2O解离为OH-和H+,OH-吸附于矿物表面,形成中间体FeS2(OH)3,后脱去H形成FeS2O[7]3。
针对黄铁矿表面电化学氧化,前人已经进行了大量的研究。然而,黄铁矿在氨基酸溶液中的电化学氧化机理研究还较少。因此,基于对黄铁矿的开发利用和对生态环境的保护,本文选取具有矿物浸出效果的氨基酸作为电解质,探究黄铁矿在3种碱性氨基酸溶液中的电化学行为。利用电化学方法,如开路电位(OCP)、线性扫描伏安(LSV)、循环伏安(CV)、交流阻抗(EIS)、Tafel极化曲线等电化学分析技术研究块状黄铁矿电极分别在组氨酸、赖氨酸、精氨酸体系中的电化学行为,从动力学和热力学的角度揭示黄铁矿的氧化机理。通过上述电化学数据得到黄铁矿的氧化过程和氧化速率,并结合等效电路数据获取黄铁矿的氧化动力学模型。通过对这些数据的分析,了解黄铁矿在碱性氨基酸中的氧化机理,旨在揭示黄铁矿电化学氧化在碱性氨基酸体系中的应用潜力,同时也可进一步完善黄铁矿的氧化理论,为相关领域的研究和应用提供基础数据和参考依据。
1试验材料与方法
1.1黄铁矿电极
试验所用黄铁矿为从中国地质博物馆购买eb0aa619122df23445129447d0231c8c3f98b53a464ccbee25b4cc6f703b81b2的高纯度立方单晶黄铁矿样品,将其切割为π cm×0.5 cm×0.25 cm的块状后作为工作电极,使用面积为1 cm2的电极抛光面作为工作电极的表面。在每次进行电化学试验之前,工作电极的表面用700目金刚砂纸抛光,以得到新的电极表面。用去离子水清洗工作电极表面除去杂质后,用高纯氮气吹干。
1.2电化学测试
电化学测试试验条件为常温,50 mL玻璃烧杯作为电化学反应电解池,将纯度分别为99 %、98 %、98 %的组氨酸、精氨酸和赖氨酸分别加入到超纯水中,制得10 mmol/L、20 mmol/L和30 mmol/L的电解质溶液。电化学测试采用三电极体系,分别是工作电极(黄铁矿电极)、辅助电极(铂电极15 mm×10 mm×0.2 mm)和参比电极(饱和甘汞电极)。所有电化学测量都是在CHI660e电化学工作站上进行,溶液均用超纯水制备,超纯水由自动双重纯水蒸馏器SZ-93制取。本文采用的电化学测试技术主要为开路电位、循环伏安测试、Tafel极化曲线、线性扫描伏安和电化学阻抗。
2结果与讨论
2.1开路电位
开路电位是指电流密度为零时的电极电位,也就是不带负载时工作电位和参比电极之间的电位差,其稳定的过程是一个电路稳定的过程。开路电位反映了电极的腐蚀几率,也可以为后续的电化学测试提供参数。黄铁矿电极在浓度分别为10 mmol/L、20 mmol/L、30 mmol/L的不同氨基酸体系中的开路电位-时间曲线分别见图1~3。由图1~3可知:黄铁矿在不同氨基酸体系中的开路电位在300 s后趋于稳定,且600 s内开路电位的变化均小于0.005 V。此结果表明,测试过程中的电化学测试系统比较稳定,碱性氨基酸体系满足电化学测量条件。
2024年第10期/第45卷矿业工程矿业工程黄金
2.2循环伏安曲线
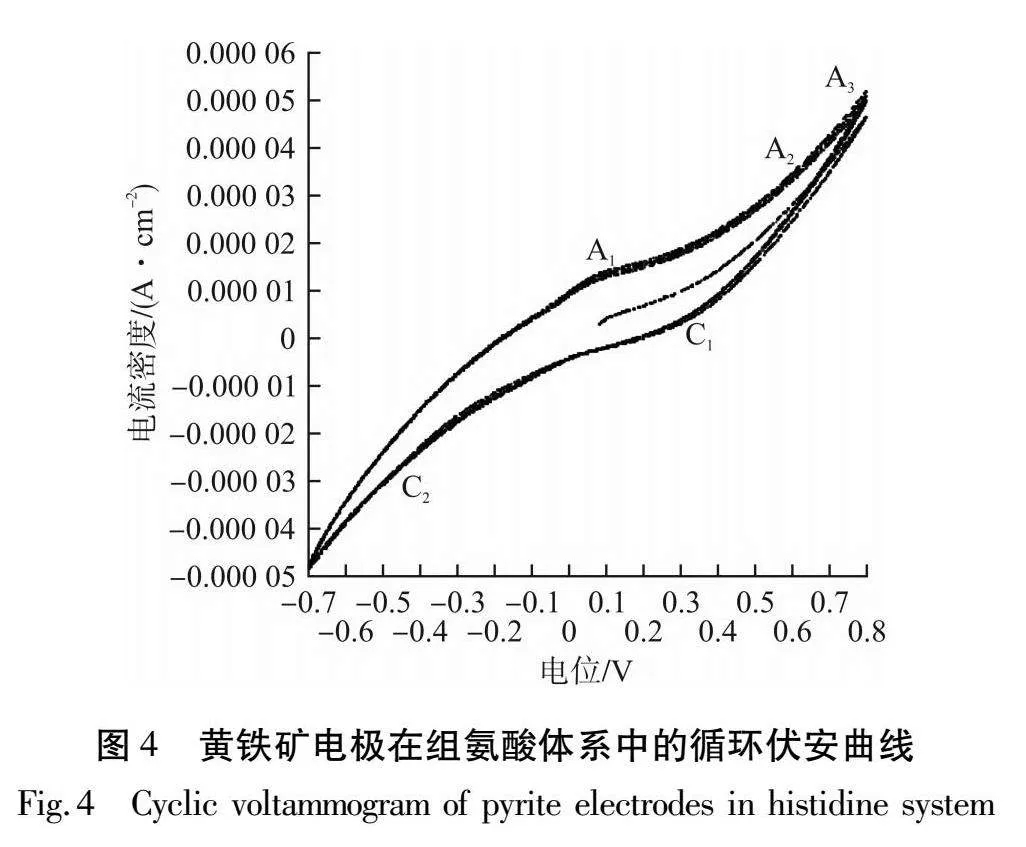
黄铁矿电极在组氨酸体系中的循环伏安曲线见图4。测量循环伏安曲线主要是为了提供黄铁矿溶解的相关信息。从开路电位开始扫描,初始电位为-0.7 V,初始扫描方向为正向,扫描速率为50 mV/s。每一种氨基酸体系中的循环伏安曲线扫描7个循环。由图4可知:在组氨酸体系中,7条循环伏安曲线几乎重合,说明测试结果具有良好的重现性。阳极峰标记为A1、A2、A3,阴极峰标记为C1、C2。测试结果和前人研究结果吻合,但峰的位置和高度有所差异,可能是黄铁矿样品和电解质的组成成分差异所导致的[8]。
高电位峰A2、A3都属于黄铁矿的氧化。A2峰位于0.6 V,与Fe(OH)3和硫元素S0的形成有关,见式(1);在0.8 V时出现A3峰,黄铁矿和S0在此高电位下反应,剧烈氧化生成SO2-4和Fe(OH)[9]3,见式(2)、式(3)。
FeS2+3H2OFe(OH)3+2S0+3H++3e(1)
FeS2+11H2OFe(OH)3+2SO2-4+19H++15e(2)
S0 +4H2OSO2-4+8H++6e(3)
电位正向扫描至最高电位0.8 V后,变为负向扫描,在扫描过程中出现2个还原峰C1、C2,C1峰在0.2 ~ 0.4 V,这是因为在阳极形成的Fe(OH)3被还原成了Fe2+,见式(4)。在-0.4~-0.2 V出现了还原峰C2,C2峰对应的反应可能是黄铁矿表面的2个反应,一个是FeS2被还原成FeS 和H2S,见式(5);另一个是黄铁矿表面的S0被还原[10],见式(6)。
Fe(OH)3+3H++eFe2++3H2O(4)
FeS2+2H++2eFeS+H2S(5)
S0+2H++2eH2S(6)
当电位在-0.7~ 0.1 V,出现了一个微弱的氧化峰A1,该峰为H2S氧化成S0,是式(6)的逆反应。由于H2S微溶于水,容易从电极表面脱离进入到溶液中,从而导致H2S在电极表面的含量很低。
黄铁矿电极在精氨酸体系中的循环伏安曲线见图5。由图5可知:在精氨酸体系中,循环伏安曲线的测量参数与组氨酸体系中一致,并且7个循环的曲线几乎重合,说明在精氨酸体系中测试结果具有良好的重现性。
在精氨酸体系中,氧化峰与还原峰的位置与组氨酸体系中大致相同,黄铁矿在这2个碱性氨基酸体系中发生的氧化还原反应是一致的,但在精氨酸体系中,在0.6 V左右并没有出现氧化峰,与在组氨酸体系中相比,在0.6 ~ 0.8 V,精氨酸体系的电流密度更低一些,猜测这是出峰不明显的原因。
黄铁矿电极在赖氨酸体系中的循环伏安曲线见图6。由图6可知:在赖氨酸体系中,循环伏安曲线的测量参数与在组氨酸体系中一致,并且7个循环的曲线几乎重合,说明在赖氨酸体系中测试结果也具有良好的重现性。同时,黄铁矿电极的循环伏安曲线出峰位置也与组氨酸体系、精氨酸体系中的大致相同,说明在这3种氨基酸体系中黄铁矿电极发生的氧化还原反应是一致的。但是,相较于赖氨酸体系,组氨酸体系和精氨酸体系中还原峰C2的位置更负,说明还原峰C2对应的反应在赖氨酸体系中更易发生。
彭樱[9]采用电化学方法研究了pH对黄铁矿氧化的影响,在酸性或碱性条件下,氧化还原电流密度比中性条件下更高,电化学氧化还原反应也更强。在中性条件下形成致密且无孔的S0和羟基氧化铁(FeOOH)会抑制黄铁矿氧化,但在碱性条件下形成的Fe(OH)3是疏松多孔的,因此,铁氧化物对黄铁矿氧化的抑制作用弱于中性条件[11-12]。与中性条件相比,在碱性条件下,更多S0能转化为可溶性硫氧(SO)物种(如SO3和 S2O2-3),从而导致其氧化作用较中性条件下更强。在赖氨酸体系中,氧化还原峰相对于组氨酸体系和精氨酸体系中更为突出,原因可能是赖氨酸溶液的碱性较另外2种氨基酸溶液更强。
黄铁矿电极在浓度为10 mmol/L、20 mmol/L和30 mmol/L的组氨酸体系、精氨酸体系、赖氨酸体系中的循环伏安曲线见图7。由图7可知:氨基酸浓度改变后,在碱性氨基酸体系中CV曲线的出峰位置并没有改变,认为黄铁矿电极在碱性氨基酸体系中碱性氨基酸的浓度影响不大。
2.3Tafel极化曲线
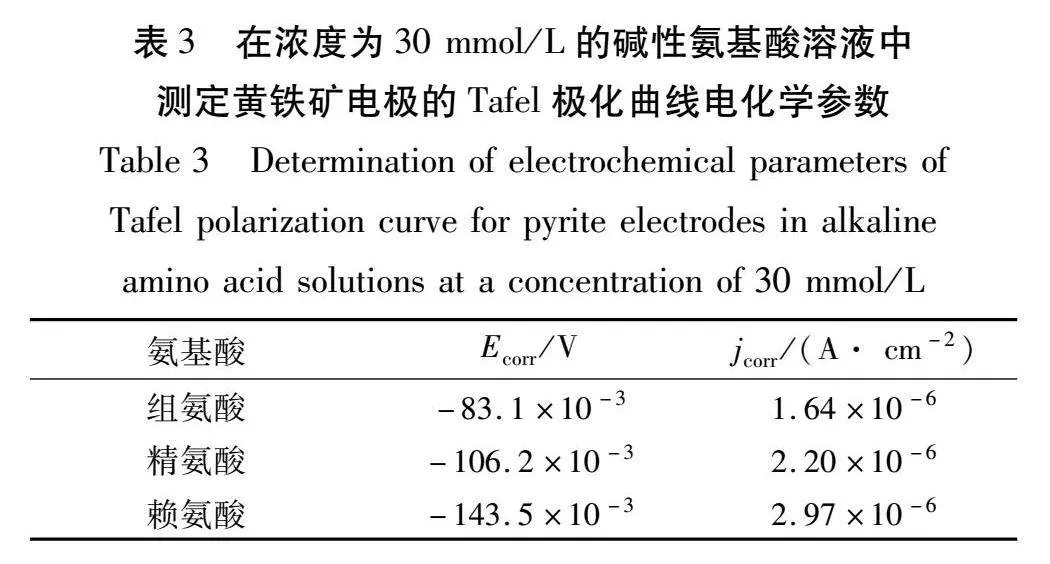
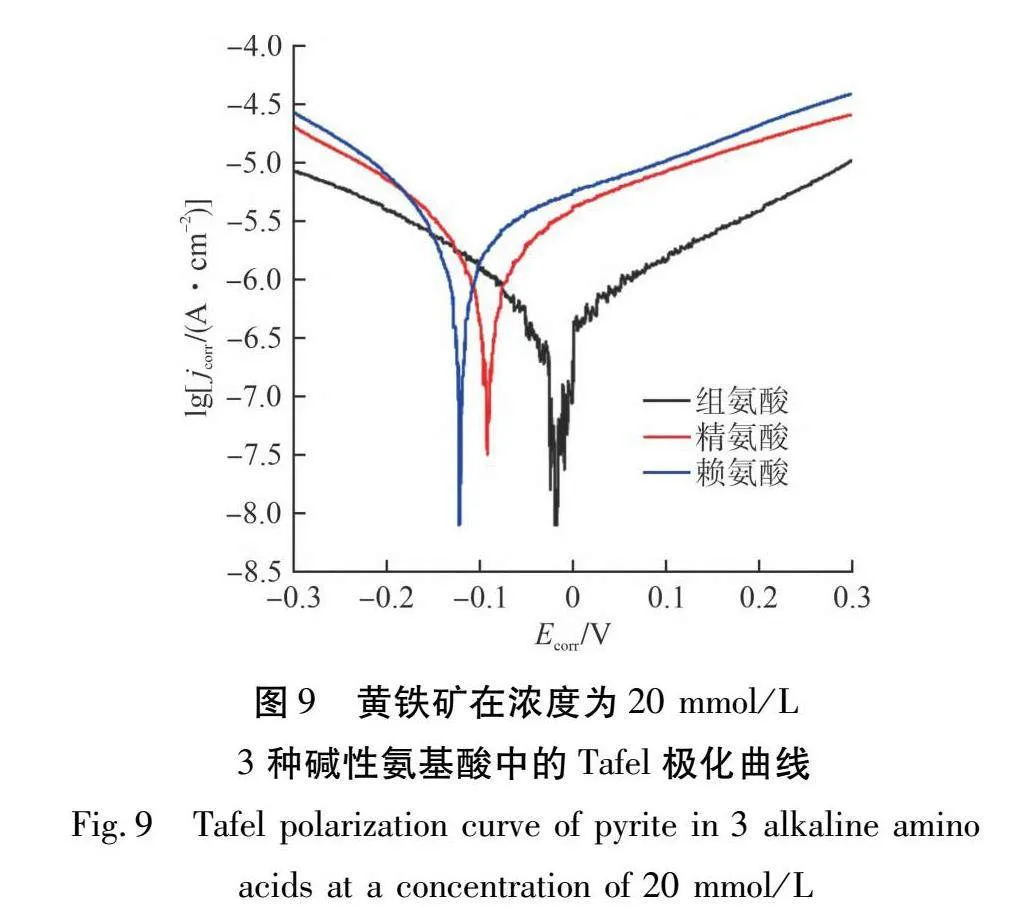
利用Tafel极化曲线可以分析黄铁矿在碱性氨基酸体系中动力学和热力学的稳定性。在Tafel极化曲线中可以得到腐蚀电位(Ecorr)和腐蚀电流密度(jcorr)等电化学参数,这些参数可以反映电极表面发生反应的速率和趋势。黄铁矿电极分别在浓度为10 mmol/L、20 mmol/L和30 mmol/L不同碱性氨基酸电解质溶液中的Tafel极化曲线见图8~10,试验电位为-0.3~0.3 V,扫描速率为10 mV/s,扫描段数为1段。
由图8~10可知:3种氨基酸体系中黄铁矿的Tafel极化曲线相似,说明黄铁矿分别在不同浓度的组氨酸、精氨酸和赖氨酸体系中具有相同的电化学相互作用机制,这些结果与CV测试结果一致。在不同浓度的碱性氨基酸体系中,黄铁矿的Tafel极化曲线电化学参数见表1~3。由表1~3可知:组氨酸、精氨酸到赖氨酸的腐蚀电位逐渐减小,而腐蚀电流密度呈相反的趋势。
这些参数在赖氨酸体系中达到最小或最大。从热力学的角度来看,腐蚀电位更负说明碱性氨基酸体系中黄铁矿表面的反应更有利,但这并不等同于有更快的反应速率。需要注意的是,Ecorr小于开路电位,原因是电极极化在Tafel扫描的过程中改变了电极表面的状态[13]。从动力学的角度来看,腐蚀电流密度越大,黄铁矿的反应速率越快[14]。结果表明,在3种碱性氨基酸电解质溶液中赖氨酸是最利于黄铁矿浸出的。
2.4线性扫描伏安曲线
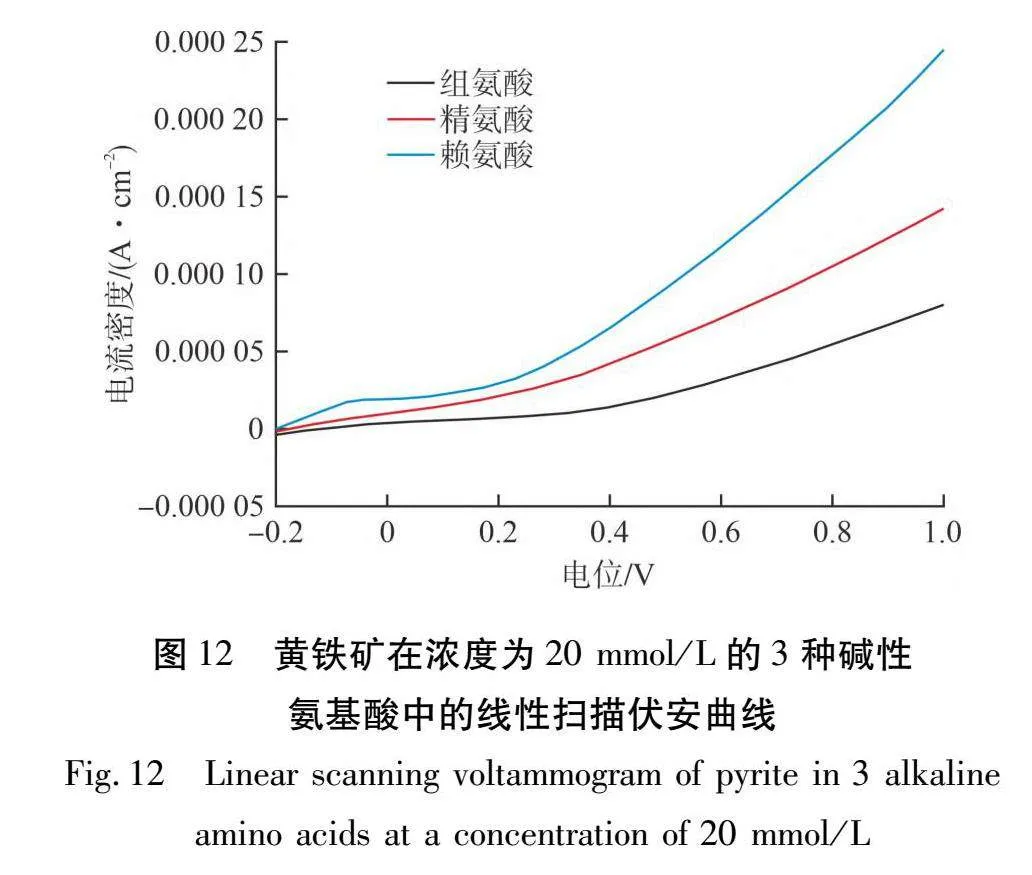
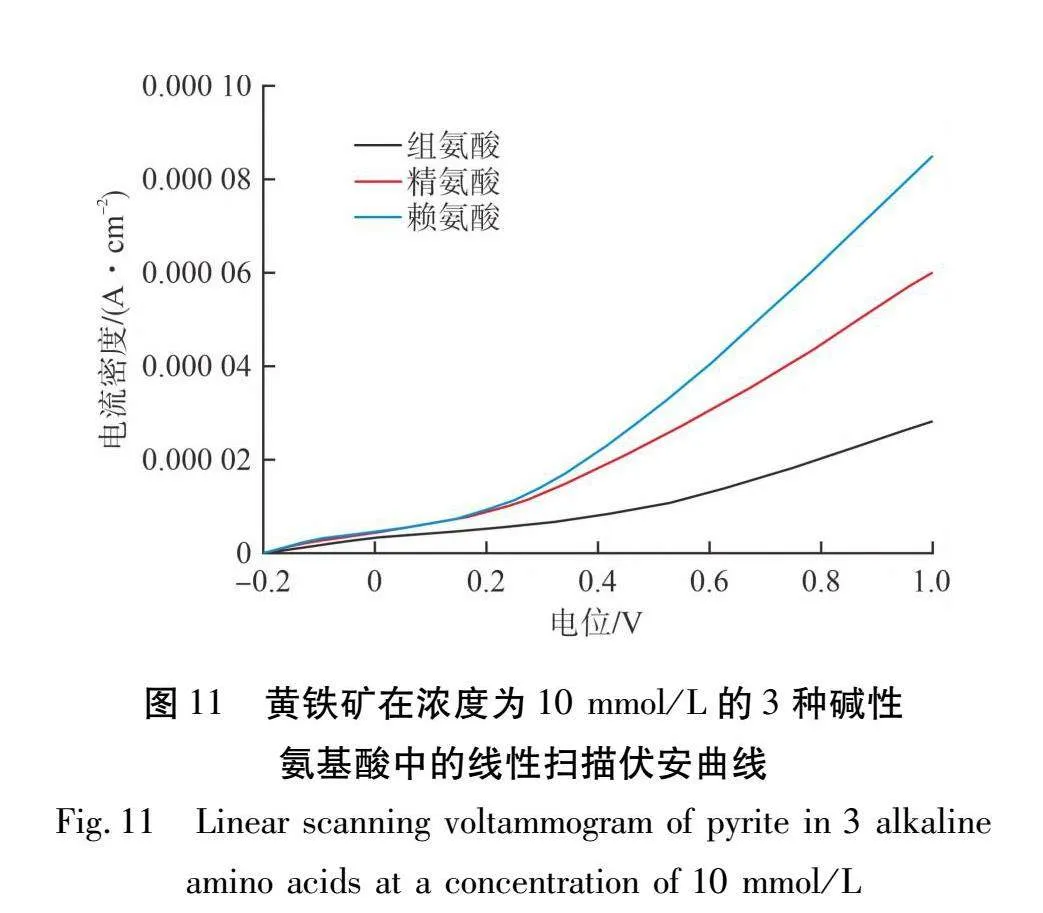
黄铁矿电极分别在浓度为10 mmol/L、20 mmol/L和30 mmol/L的碱性氨基酸中测得的线性扫描伏安曲线见图11~13。线性扫描伏安曲线可以用来评估黄铁矿的电催化活性。线性扫描伏安曲线的测试电位为-0.2 ~1.0 V,测试速率为2 mV/s。
由图11~13可知:黄铁矿电极在3种氨基酸体系中的LSV曲线都呈先平缓然后上升的趋势。LSV曲线的活化区和钝化区的分界并不明显,在-0.2 ~0 V时,LSV曲线比较平缓,在这个区域可能产生了S0或Fe(OH)3,并沉积在电极表面,让电极表面从活化区向钝化区转化。在钝化区电流密度变化不大,原因是单质S0的形成阻碍了黄铁矿表面继续发生反应。 BRYSON等[15-16]研究发现,黄铁矿表面在钝化区没有明显变化。而在过钝化区,随着电位的增大,电流密度也快速上升,说明在较高电压下黄铁矿更容易氧化,也意味着钝化层被溶解或进一步氧化。
2.5交流阻抗
对矿物进行EIS测量可以了解更多有关于矿物/溶液界面的信息,如黄铁矿表面的物理信息和黄铁矿氧化过程中的化学动力学等。在0.2 V、0.4 V、0.6 V下黄铁矿电极分别在3种碱性氨基酸中测得的奈奎斯特曲线,以及采用Rs(C(RctW))电路进行拟合后的等效电路图见图14、图15。在Rs(C(RctW))电路中,Rs表示该电路中溶液的电阻,C表示表面层—电极界面的双层电容,Rct表示电荷转移电阻,W表示Warburg扩散电阻。由图14可知:在3种体系中,不同电压下的光谱在高频和中频中显示出一个不完整的半圆,在低频区中显示出典型的Warburg阻抗特征。
通过等效电路拟合获得的阻抗参数值见表4。由表4可知:采用拟合电路获得的数值与实际值之间得到较低的χ2值,说明拟合的等效电路得到的数值与实际数值非常接近。Rct可以反映出电极表面的反应速率[15-16]。拟合结果说明,利用等效电路拟合的曲线与实际曲线有较高的吻合度,因此采用的拟合电路能够较为准确反映试验过程中黄铁矿的动力学过程。在0.2 V、0.4 V、0.6 V电位下,赖氨酸体系的Rct值均是最小的,说明黄铁矿在赖氨酸体系中氧化速率是最快的,这与前期研究结果一致。
3结论
本文以黄铁矿电极为研究对象,通过采用开路电位、循环伏安、Tafel极化曲线、线性扫描伏安和交流阻抗等电化学测试方法,对黄铁矿在不同浓度的3种碱性氨基酸下的电化学氧化产物及氧化速率进行了比较和研究,得到了以下结论:
1)通过CV测试,观察到CV曲线的峰位置在各个条件下基本一致。说明3种不同的碱性氨基酸体系与黄铁矿电极的反应机理是一致的,并且氨基酸电解质浓度对反应机制的影响不明显。
2)LSV测试结果显示,在碱性氨基酸体系中,随着施加电压的增加,黄铁矿电极的电流密度呈递增趋势。这说明在较高电压条件下,黄铁矿电极更容易发生氧化反应,产生较大的电流响应。
3)Tafel极化曲线和EIS测试数据表明,赖氨酸体系中黄铁矿电极的氧化速率最快,精氨酸体系次之,而组氨酸体系中的氧化速率最慢。
[参 考 文 献]
[1]刘云.黄铁矿氧化机理及表面钝化行为的电化学研究[D].广州:华南理工大学,2011.
[2]杨志婷,字富庭,张炎,等.酸性矿山废水中表面钝化技术的研究进展[J].有色金属工程,2023,13(7):147-157.
[3]HOLMES P R,CRUNDWELL F K.The kinetics of the oxidation of pyrite by ferric ions and dissolved oxygen:An electrochemical study[J].Geochimica et Cosmochimica Acta,2000,64(2):263-274.
[4]LIU Y,DANG Z,LU G N,et al.Utilization of electrochemical spectroscopy for monitoring pyrite oxidation in the presence and absence of Acidithiobacillus ferrooxidans[J].Minerals Engineering,2011,24(8):833-838.
[5]BIEGLER T,SWIFT D A.Anodic behaviour of pyrite inPLVQOISCPLT6IPCFHtJrtg== acid solutions[J].Electrochimica Acta,1979,24(4):415-420.
[6]KELSALL G H,YIN Q,VAUGHAN D J,et al.Electrochemical oxidation of pyrite(FeS2) in aqueous electrolytes[J].Journal of Electroanalytical Chemistry,1999,471(2):116-125.
[7]涂志红.黄铁矿氧化过程中硫形态转化及其表面氧化电化学研究[D].广州:华南理工大学,2017.
[8]ZHANG Y,CHEN Z,ZI F T,et al.New insights into the oxidation mechanism of pyrite in copper-containing sulfuric acid:An electrochemical,AFM,Raman spectroscopy and XPS investigation[J].Journal of the Electrochem Society,2021,168(6):061502.
[9]彭樱.黄铁矿典型晶面氧化机理研究[D].武汉:武汉理工大学,2021.
[10]CHANDRA A P,GERSON A R.The mechanisms of pyrite oxidation and leaching:A fundamental perspective[J].Surface Science Reports,2010,65(9):293-315.
[11]ELISABET A,ANN E B.Electrochemical reaction mechanisms at pyrite in acidic perchlorate solutions[J].Journal of the Electrochemical Society,2019,144(4):1 281-1 286.
[12]CALDEIRA C L,CIMINELLI V S T,DIAS A,et al.Pyrite oxidation in alkaline solutions:Nature of the product layer[J].International Journal of Mineral Processing,2003,72(1/2/3/4):373-386.
[13]CONSTANTIN C A,PAUL C.Oxidative dissolution of pyrite in acidic media[J].Journal of Applied Electrochemistry,2013,43(7):659-666.
[14]唐家华,毛王彬,李栢庄,等.金电极在硫代硫酸盐溶液中的电化学氧化机理研究[J].黄金,2022,43(8):55-59.
[15]BRYSON L J,CRUNDWELL F K.The anodic dissolution of pyrite(FeS2) in hydrochloric acid solutions[J].Hydrometallurgy,2014,143:42-53.
[16]YIN Q,KELSALL G H,VAUGHAN D J,et al.Rotating Ring(Pt)-Disc(FeS2) electrode behavior in hydrochloric solutions[J].Journal of Colloid & Interface Science,1999,210(2):375.
Electrochemical oxidation mechanism of pyrite in histidine,lysine,and arginine
Xue Xudong1,Zhang Yan2
(1.Xi,an Innovation College of Yan,an University; 2.Faculty of Science,Kunming University of Science and Technology)
OTjEgi4LipgPkvrBiUN5SGj4c6MWGeOWxlcClDpui0k=STeXSkC0ncUaYeGIHZ7nwwwTFYACSdolFNl+ktnT5V8=Abstract:During pyrite mining,tailings and waste residues are generated,and the oxidation of exposed metal sulfides leads to significant environmental issues such as acid mine drainage pollution.Studying the oxidation mechanism of pyrite is crucial for inhibiting or preventing the formation of acid mine drainage.Alkaline amino acids were used as electrolytes to explore the electrochemical oxidation mechanism of pyrite.Through electrochemical methods such as OCP,CV,Tafel polarization curve,LSV,and EIS,the electrochemical behavior of pyrite surfaces was measured,confirming the feasibility of pyrite oxidation in an alkaline amino acid system.The oxidation mechanisms of pyrite were consistent across the 3 alkaline amino acids,with the oxidation rate of pyrite following the order:lysine>arginine>histidine.
Keywords:pyrite;histidine;lysine;arginine;oxidation mechanism;electrochemical oxidation
