化学反应机理的考查
2024-10-29白燕英
电化学是高考化学试题中必考的知识点,化学反应机理从微观探析角度考查物质间反应的实质,将电化学原理与化学反应机理结合起来设计问题,能更好地考查学生宏观辨识与微观探析的化学核心素养.
1 对原电池与化学反应机理的考查
该类试题先将原电池电极附近化学反应的微观过程展示出来,然后根据反应机理图提供的信息,设计诸如电极类型的判断,电极反应方程式的书写或正误判断,电极产物成分、质量的确定,电极附近电解液pH 的变化,电路中转移电子的数目等一系列问题.
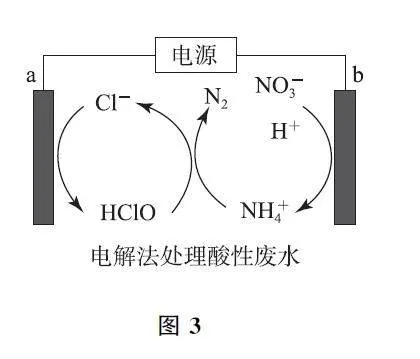
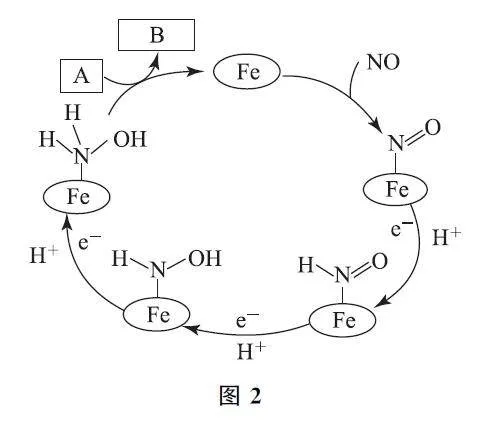
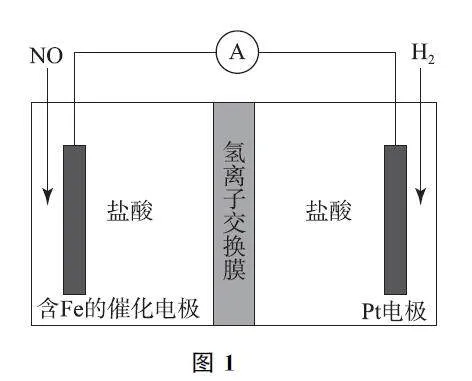
例1 与NH4Cl化学性质类似的盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂.工业上可利用电化学原理制取,其主要制备原理如图1所示.其中含Fe的催化电极反应机理如图2所示.图3是用图1所示电池电解处理含有Cl- 、NO- 3 的酸性废水的装置.下列说法错误的是( ).
A.图1电池工作时,Pt电极是负极
B.图2中,若A 为H+ ,则B为NH3OH+
C.电池工作时,每消耗3.36L H2 (标准状况下),左室溶液质量增加3g
D.电极b接电源负极,处理1molNO- 3 ,废水中放电的Cl- 为2.5mol
解析 由图1装置无外接电源可确定该装置是原电池.在含Fe的催化电极上,氮元素的化合价由NO 中的+2价转化为盐酸羟胺(NH3OHCl)中的-1价,即NO 发生得电子的还原反应,故含铁电极为正极,Pt电极是负极,选项A 说法正确.由使用原电池的目的是制备盐酸羟胺可知,图2中生成B物质的变化可表示为FeNH2OH+A →B+Fe,结合质量守恒及盐酸羟胺与NH4Cl性质相似可确定A 为H+ ,B为NH3OH+ ,选项B说法正确.Pt电极上H2 失去电子发生氧化反应:H2 -2e- =2H+ ,消耗3.36L H2(标准状况下为0.15mol)共转移0.3mol电子,则必有0.3molH+ 由右室流向左室,同时由NO 变成盐酸羟胺,由关系式NO~NH3OHCl~3e- 可知,参加反应的NO 为0.1mol,故左室增加的质量为0.1molNO 和0.3molH+ 质量之和,其质量为3.3g,选项C说法错误.由图3中信息可知,NO- 3 在b电极上转化为NH4+ 时发生的是得电子的还原反应,故b电极为阴极,阴极是与电源负极相连的电极,NO- 3 最终变成了N2,根据化合价的变化可推出处理1molNO- 3 共转移5 mol电子,而1 molCl- 转化为HClO 转移2mol电子,因此当电路转移5mol电子时,2.5 molCl- 参加反应,选项D说法正确.答案为C.
点评 解答涉及循环转化机理图的试题时,首先要明确最终的生成物(箭头指向且在“圈外”的物质)和反应物(图2中B 是生成物,A、NO 是反应物);反应物中组成元素的化合价的升降情况(图2中NO →NH3OHCl时氮元素化合价降低);再根据化合价的升降情况及原电池工作时电极发生的反应,确定相应的电极种类,最后对各选项或问题进行具体分析.
2 对电解池与化学反应机理的考查
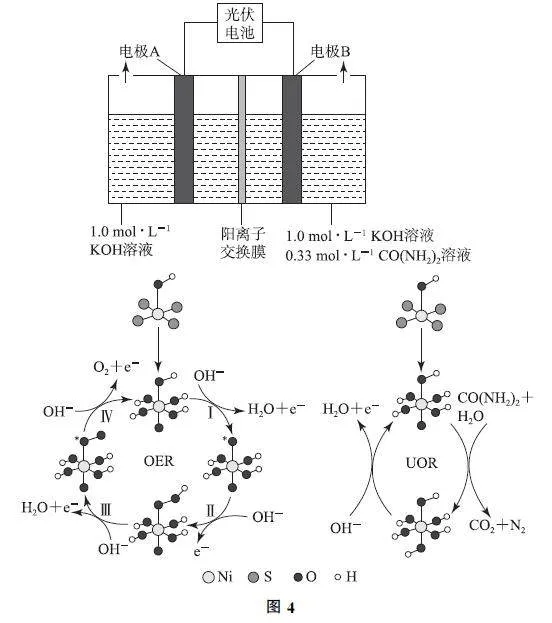
例2 以非晶态Ni(Ⅲ)基硫化物为催化剂,能有效催化OER(析氧反应)和UOR(尿素氧化反应),从而降低电解水制氢过程中的能耗,其工作原理和反应机理如图4所示.
下列说法正确的是( ).
A.UOR的电化学反应总过程为CO(NH2)2-6e- +6OH- =CO2↑+N2↑+5H2O
B.电解过程中,电极A 附近溶液的pH 不变
C.OER分4步进行,其中没有非极性键的形成或断裂
D.若将光伏电池换成铅蓄电池,电极A 应连接铅蓄电池的PbO2 电极
解析 该装置是电解池,尿素在电极B放电转化为CO2、N2,氮元素由-3价升高至0价,发生的是失电子的氧化反应,选项A 正确.电极A 为阴极,电极反应式为2H2O+2e- =2OH- +H2↑,故电极A附近溶液的pH 增大,选项B错误.观察OER 流程图知,过程Ⅱ中有O—O 非极性键的形成,选项C错误.铅蓄电池的负极材料是Pb,电解池的阴极应与电源的负极相连接,选项D错误.答案为A.
点评 该题的突破口是电极B上相关物质的元素变化,氮元素化合价升高,从而确定电极B是阳极;其次是题干中“电解水制氢”,确定A 电极上有H2 生成,进一步确定电极A 附近溶液的pH 是否会发生变化;此外还需要熟记铅蓄电池电极材料是Pb而不是PbO2.
3 电化学原理与反应机理在实际生产中的应用
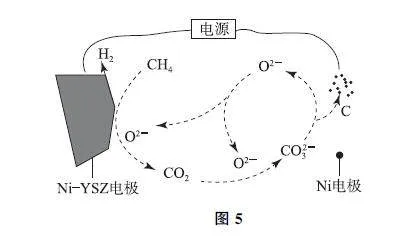
例3 含碳化合物的合成与转化具有重要的研究价值和现实意义.我国科学家报道了机理如图5所示的电化学过程.
(1)Ni电极反应式为________.
(2)理论上,每有1molCO2 与O2- 结合,电路中转移电子数为________(N A 为阿伏加德罗常数的值),总反应方程式为________.
解析 (1)CO23- 在Ni电极放电转化为C与O2- ,发生的是得电子的还原反应,电极反应式为CO23-+4e-=C+3O2-.(2)由图中信息知,1molCO2 与1molO2- 结合可生成1molCO23-,由(1)的分析知,每消耗1molCO23- 就会有4mol电子转移,故每生成1molCO23- 也会有4mol电子转移.CH4、O2- 在NiGYSZ 电极转化为CO2,电极反应式为CH4+2O2- -4e- =CO2+2H2,生成的CO2 与 O2- 结合生成CO23-,故理论上,生成1molCO2 转移电子数为4N A.由流程图知,初始反应物为CH4,最终产物为H2、C,故总反应为CH4=电解=C+2H2.
总之,解答电化学中化学反应机理类试题时要明确电化学的目的,通过分析反应机理,判断物质的变化,进而判断原电池的正负极或电解池的阴阳极,通过反应机理示意图中物质的变化情况,结合不同电化学装置的工作原理,进一步分析具体的问题.
(完)
