问“题”哪得清如许 唯有“教材”活水来
2024-10-29陈常菊




教材是对课程标准的具体化,是教学的依据,体现了新课程理念,突出了对化学学科核心素养的要求,是命题的依据.近几年,化学试题逐渐朝着紧扣教材、强化学生核心素养的方向发展.教材不仅是高考命题的资源依据,同时渗透着命题改革方向的信息.笔者选取近几年的高考试题,以人教版(2020年版)选择性必修1教材(以下简称教材)为例,阐释与电化学有关的高考试题与教材的密切关系,以期引起大家的关注与深思.
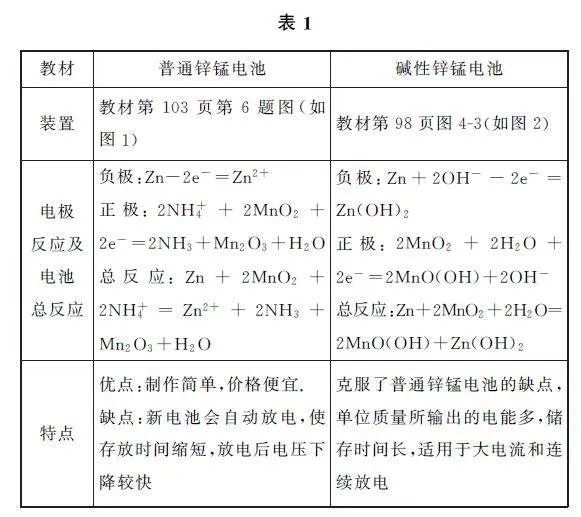
1 锌锰电池与教材主干知识的关联
相关装置及电极反应如表1所示.
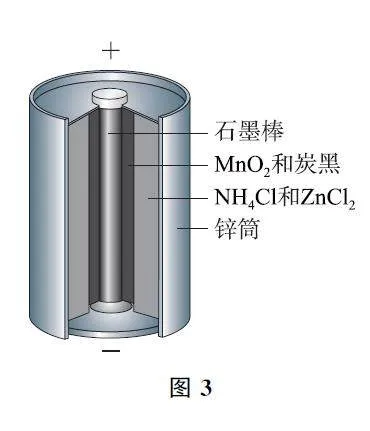
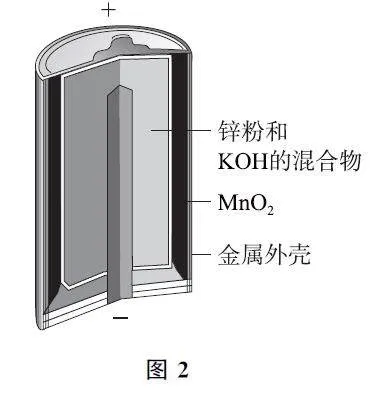
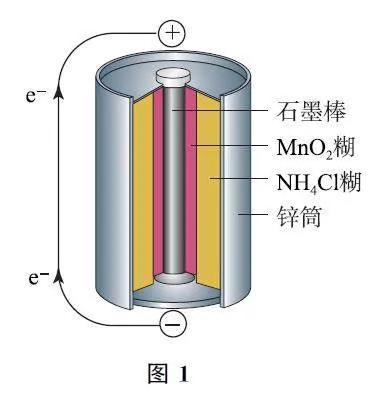
例1 (2024年北京卷)酸性锌锰干电池的构造示意图如图3所示.关于该电池及其工作原理,下列说法正确的是( )
A.石墨作电池的负极材料
B.电池工作时,NH4+向负极方向移动
C.MnO2 发生氧化反应
D.锌筒发生的电极反应为Zn-2e- =Zn2+
答案 D.
【考题溯源】本题与教材知识高度吻合,只要了解表1的两极反应原理和方程式的书写,本题可解.
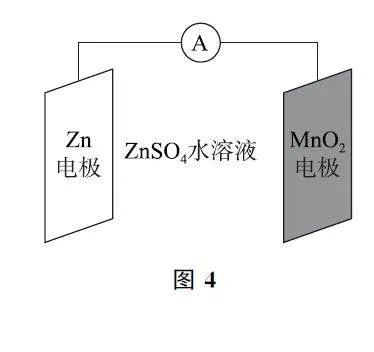
例2 (2024年全国甲卷) 科学家使用δGMnO2 研制了一种MnO2GZn 可充电电池(如图4).电池工作一段时间后,MnO2 电极上检测到MnOOH 和少量ZnMn2O4.下列叙述正确的是( ).
A.充电时,Zn2+ 向阳极方向迁移
B.充电时,会发生反应Zn+2MnO2=ZnMn2O4
C.放电时,正极反应有MnO2 + H2O+e- =MnOOH+OH-
D.放电时,Zn电极质量减少0.65g,MnO2 电极生成了0.020molMnOOH
答案 C.
【考题溯源】本题在教材一次电池的基础上深化成二次电池进行考查,体现了思维的进阶和高考命题超越教材的命题理念.充电时该装置为电解池,电解池中阳离子向阴极迁移,选项A 不正确.放电时,负极的电极反应为Zn-2e- =Zn2+ ,则充电时阴极反应为Zn2+ +2e- =Zn,选项B 不正确.放电时MnO2 电极为正极,正极上检测到MnOOH 和少量ZnMn2O4,则正极上主要发生的电极反应是MnO2+H2O+e- =MnOOH+OH- ,选项C 正确.放电时,Zn电极质量减少0.65g(物质的量为0.010 mol),电路中转移0.020mol电子,由正极反应可知,若正极上只有MnOOH 生成,则MnOOH 的物质的量为0.020mol,但是正极上还有ZnMn2O4 生成,因此,MnOOH 的物质的量小于0.020mol,选项D不正确.答案为C.
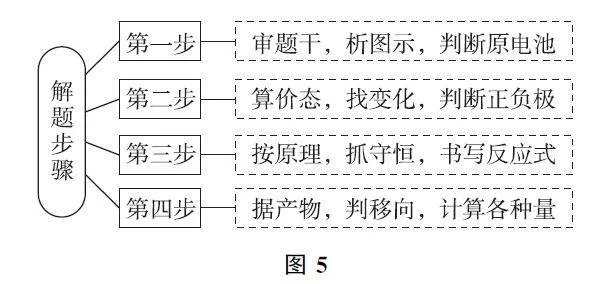
【思维模型】解答有关化学电源PEmqvKkTOKKWdrgWbrzBOJc8HsQMOLhSPlE/xJDag+8=电极反应式书写试题的思维流程,如图5所示.
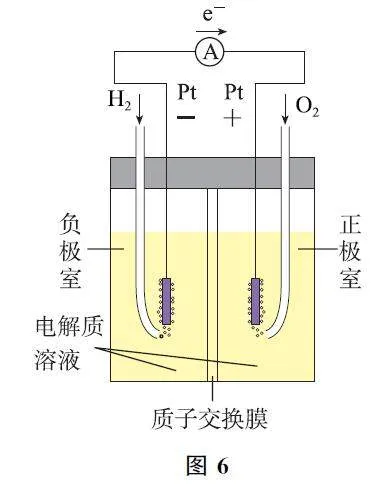
2 燃料电池与电解池的互逆原理
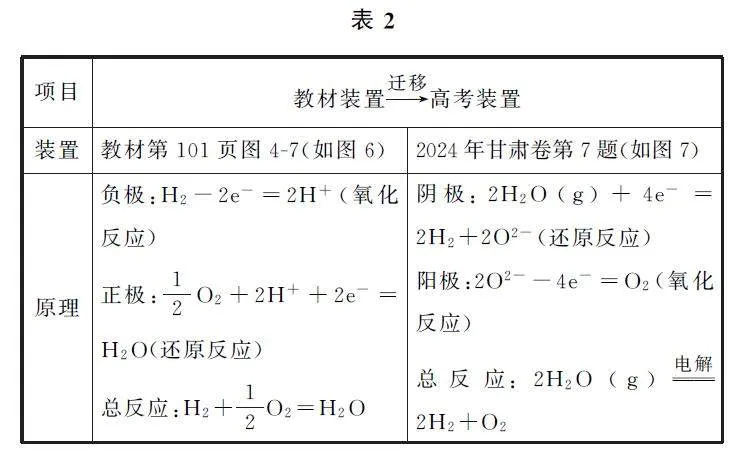
教材及高考试题的装置和反应原理如表2所示.
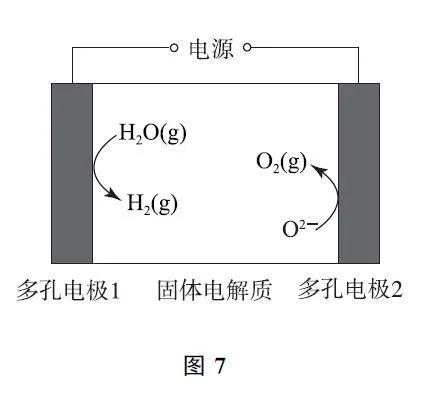
例3 (2024年甘肃卷)某固体电解池工作原理如图7所示,下列说法错误的是( ).
A.电极1的多孔结构能增大与水蒸气的接触面积
B.电极2是阴极,发生还原反应:O2+4e- =2O2-
C.工作时O2- 从多孔电极1迁移到多孔电极2
D.理论上电源提供2mole- 能分解1molH2O
答案 B.
【考题溯源】由图7可知多孔电极1上H2O(g)发生得电子的还原反应转化成H2(g),多孔电极1为阴极,电极反应为2H2O+4e- =2H2+2O2- ,多孔电极2为阳极,发生氧化反应:2O2- -4e- =O2,选项B错误.根据电解总反应为2H2O(g)电解=2H2+O2 和电子守恒可知,选项D正确.
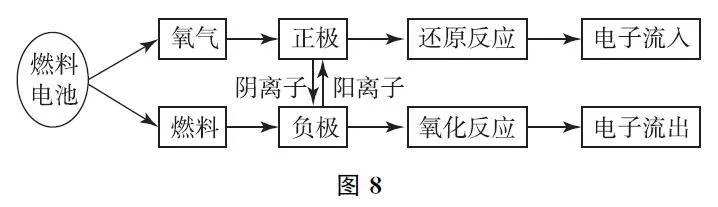
【思维模型】如图8所示.
1)注意介质是电解质溶液还是熔融盐或氧化物.
2)通入负极的物质为燃料,通入正极的物质为氧气(或其他氧化剂).
3)通过介质中离子的移动方向,可判断电池的正负极,同时考虑该离子是否参与靠近一极的电极反应.
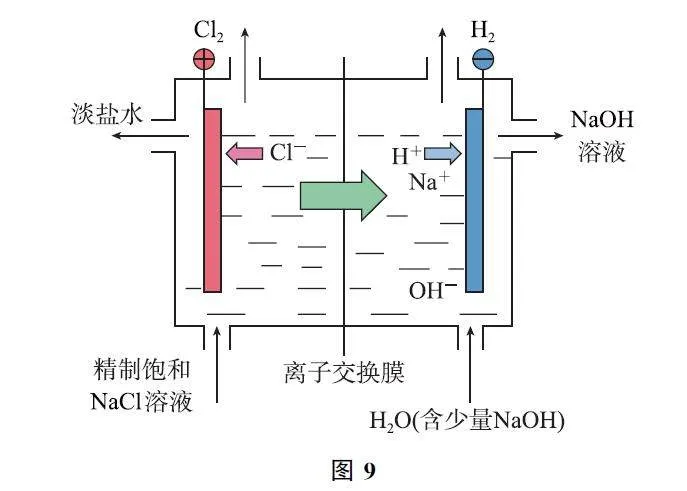
3 电解饱和食盐水装置的迁移应用
电解饱和食盐水装置的迁移应用如表3所示.
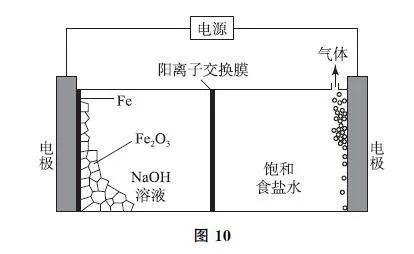
例4 (2024年广东卷)一种基于氯碱工艺的新型电解池(如图10),可用于湿法冶铁的研究.电解过程中,下列说法不正确的是( ).
A.阳极反应:2Cl- -2e- =Cl2↑
B.阴极区溶液中OH- 浓度逐渐升高
C.理论上每消耗1molFe2O3,阳极室溶液减少213g
D.理论上每消耗1molFe2O3,阴极室物质最多增加138g
答案 C.
【考题溯源】由图10可知,右侧电极Cl- 放电产生Cl2,为阳极,选项A 说法正确.左侧电极为阴极,发生还原反应,Fe2O3 在碱性条件下转化为Fe,电极反应为Fe2O3+6e- +3H2O=2Fe+6OH- ,选项B说法正确(该选项知识可根据电解池装置中的标识物判断).中间为阳离子交换膜,Na+ 由阳极向阴极移动.理论上每消耗1 molFe2O3,转移6 mol电子,产生3molCl2,同时有6molNa+ 由阳极转移至阴极,则阳极室溶液减少3×71g+6×23g=351g,阴极室物质最多增加6×23g=138g,选项C说法错误,选项D说法正确.答案为C.
【思维模型】电化学计算常用方法如图11所示.
4 电化学防护的迁移应用
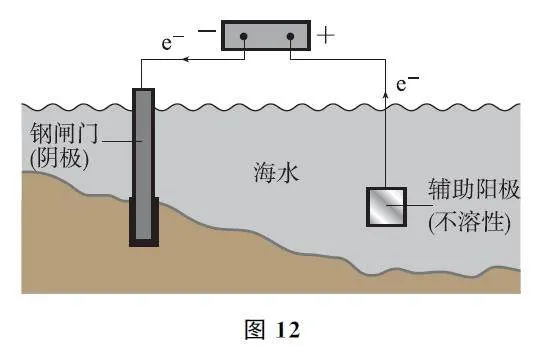
电化学防护的迁移应用如表4所示.
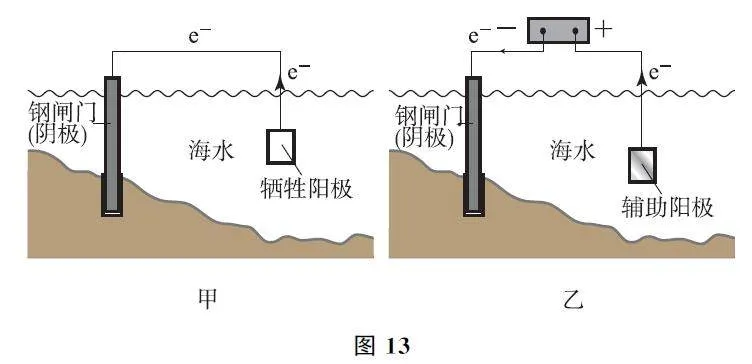
例5 (2024年6月浙江卷)金属腐蚀会对设备产生严重危害,腐蚀快慢与材料种类、所处环境有关.图13为2种对海水中钢闸门的防腐措施示意图,下列说法正确的是( ).
A.两图中,阳极材料本身均失去电子
B.图13G乙中,外加电压偏高时,钢闸门表面可发生反应:O2+4e- +2H2O=4OH-
C.图13G乙中,外加电压保持恒定不变,有利于提高对钢闸门的防护效果
D.两图中,当钢闸门表面的腐蚀电流为零时,钢闸门、阳极均不发生化学反应
答案 B.
【考题溯源】图13G甲为牺牲阳极的阴极保护法,牺牲阳极一般为较活泼的金属,作为原电池的负极,失去电子被氧化;图13G乙为外加电流的阴极保护法,阳极材料为辅助阳极,其通常是惰性电极,本身不失去电子,选项A、D均不正确.图13G乙中,外加电压偏高时,钢闸门表面积累的电子很多,除了海水中的H+放电外,海水中溶解的O2也会竞争放电,故可发生反应:O2+4e- +2H2O=4OH- ,选项B正确.图13G乙为外加电流的阴极保护法,理论上只要能对抗钢闸门表面的腐蚀电流即可,当钢闸门表面的腐蚀电流为零时保护效果最好;腐蚀电流会随着环境的变化而变化,若外加电压保持恒定不变,则不能保证抵消腐蚀电流,不利于提高对钢闸门的防护效果,选项C不正确.
【思维模型】金属防护分析的思维模型如下.
1)2种防护方法.
2)解题模型.首先,判断防护类型;其次,根据原电池原理和电解池原理分析防护原理,结合生活实际对选项做出合理判断.
5 教材习题与高考试题的关联
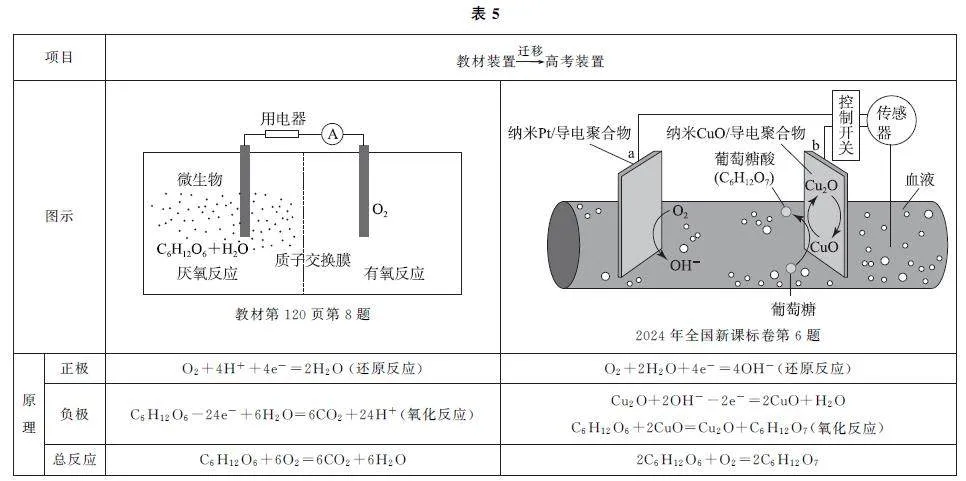
教材及高考试题的装置和反应原理如表5所示.
例6 (2024年全国新课标卷)一种可植入体内的微型电池工作原理如图(表5中)所示,通过CuO催化消耗血糖发电,从而控制血糖浓度.当传感器检测到血糖浓度高于标准,电池启动.血糖浓度下降至标准,电池停止工作.(血糖浓度以葡萄糖浓度计)电池工作时,下列叙述错误的是( ).
A.电池总反应为2C6H12O6+O2=2C6H12O7
B.b电极上CuO 通过Cu(Ⅱ)和Cu(Ⅰ)相互转变起催化作用
C.消耗18 mg 葡萄糖,理论上a 电极有0.4mmol电子流入
D.两电极间血液中的Na+ 在电场驱动下的迁移方向为b→a
答案 C.
【考题溯源】对比教材习题和高考题可以看出,教材题中采用了质子交换膜即H+ 可以移动向正极,故正极方程式需要兼顾真实的离子环境进行书写.教材习题的负极反应是葡萄糖的完全氧化,生成CO2,而高考题是控制氧化,生成葡萄糖酸,要求考生建立有机物的氧化反应理念,即加氧去氢为氧化.根据反应2C6H12O6+O2=2C6H12O7 可知,1molC6H12O6参加反应时转移2mol电子,18mgC6H12O6 的物质的量为0.1mmol,则消耗18mg葡萄糖时,理论上a电极有0.2mmol电子流入,选项C错误.
【思维模型】零价法书写有机物负极反应的规则:若负极有机物燃料为CxHyOz ,产物中C元素为+4价的CO23- 或 HCO3-,则转移电子数为 C原子数×4+H 原子数×1+O 原子数×(-2),若有机阴离子在负极反应(如CH3COO- ),转移电子数则为C原子数×4+H 原子数×1+O 原子数×(-2)+电荷数.
由此可以看出,高考试题的核心知识点均源于教材,但又不拘泥于教材,而是将教材知识进行深加工后再进行考查.学生在平日的学习过程中一定要紧扣教材,分析教材知识原型,进行知识的横向与纵深挖掘,将知识的内涵与外延烂熟于心,这样才能熟练应用知识解决问题.
(完)
