聚集诱导发光材料:生物医学成像中的新视野
2024-09-30龚晚君刘勇王志明
作为一种先进的手段,生物医学成像技术能够精确捕捉生物体内部的结构、功能及代谢信息。在医学领域,这项技术发挥着至关重要的作用。例如,在疾病的诊断与监测方面,医生们依赖生物医学成像技术来识别肿瘤、心血管疾病以及神经系统疾病等。这些图像不仅有助于医生对病情进行准确判断,还能监测疾病的发展态势以及评估治疗效果。此外,在药物研发过程中,生物医学成像技术也扮演着举足轻重的角色。基于该技术,科学家们能够直观地观察药物在动物模型或人体内的分布、代谢及效果,从而极大加速新药的开发速度并降低研发成本。值得一提的是,生物医学成像技术为科学家们提供了深入研究疾病发生机制的窗口:能够更深入地探索病理生理过程,为疾病的预防和治疗提供坚实的理论支撑和实验依据。这推动了医学领域的进步,特别是对于个性化医疗——基于患者的个体差异和病情特点,制定出更加精准的治疗方案,从而提高治疗效果并提升患者的生存质量。
生物医学成像通常通过各种成像设备来实现,如X射线、超声波、磁共振成像(MRI)、计算机断层扫描(CT)、正电子发射断层扫描(PET)、单光子发射计算机断层扫描(SPECT)、光学成像,等等。这其中,光学生物医学成像,特别是基于荧光的生物医学成像技术,凭借着非入侵式、高时空分辨率、实时成像、多模态成像等优势,已经成为基础研究、临床诊断不可或缺的工具。
在光学生物成像领域,多代科学家曾倚重传统荧光材料,包括有机荧光染料和无机荧光材料,对其研究目标进行观测。然而,随着对生命科学研究的深入,这些传统材料在检测灵敏度、亮度和光稳定性等方面显现出一定的局限性。因此,为推动该领域技术的进步,亟需涌现一类新型荧光材料。在这一背景下,聚集诱导发光(aggregation-induced emission, AIE)材料应运而生,构成了一种全新的荧光材料体系。AIE是一种有别于传统发光的荧光现象,因此AIE材料展现出有别于传统荧光材料的特性,可显著提升生物检测和荧光成像的灵敏度、特异性和分辨率。可以说,AIE材料在生物医学成像领域崭露头角,成为一匹技术上的“黑马”。
在单分散状态下,AIE材料表现出较低的荧光强度;然而,一旦发生聚集,其荧光强度显著提升。这种“越聚集越亮”的特性是AIE材料与其他材料最显著的差异之一。在此基础上衍生出的其他特性,如免洗和高稳定性等,共同使AIE分子成为更适合生物医学成像的荧光材料。生物医学成像的对象主要是生物样本,复杂的前处理过程会极大地影响成像的灵敏度与准确性。为了最大程度还原或保留生物样品的信息,减少对其处理的步骤是一种简单、经济且高效的手段,AIE材料的免洗优势正好符合这一需求。AIE材料只有在生物样本上聚集时才会产生强烈的荧光信号,而在其他位置保持“黑暗”,因此具有较高的信噪比,无须在样本前处理过程中进行多次洗涤,对生物样本更加友好。另外,相较于传统的荧光染料,AIE材料在工作时通常处于聚集态,能够更好地抵挡激光照射引发的材料破坏,因此具有更好的光稳定性和更广的成像浓度范围,能够在长时间的扫描成像中保持稳定的信号输出,为动态过程的观察提供了便利。
看透细胞的“超级眼睛”——AIE细胞成像探针
在生命科学领域,研究者常常需要深入单个细胞内部,观察和研究细胞器的动态和功能。然而,细胞器的体积微小,且分布密集,这给研究者的观察带来了极大的挑战。细胞器作为细胞内的基本功能单元,其形态和动态变化对于理解细胞生命活动至关重要。传统的荧光显微技术为细胞器成像提供了有力工具,但荧光物质的性能仍需进一步优化。AIE材料免洗、高稳定性、越聚集越亮的特点在细胞器成像领域有极为突出的优势,研究者可以通过精密的分子调控,使得AIE材料能够快速穿透细胞膜,进入细胞内部,而AIE材料上特定的靶向基团如三苯基膦、吗啉及AIE分子独特的结构则可以将材料牵引到特定的细胞器上,从而实现精准的定位和成像[1]。
在细胞器成像研究中,尽管罗丹明、荧光素等传统荧光材料仍被广泛使用,但基于AIE性质开发的探针往往具有宽成像浓度范围、高抗漂白能力以及免洗等优势,更适合用于细胞器的长期动态追踪。例如,线粒体作为细胞中的“能量工厂”,其结构与功能的完整性对维持细胞正常生理活动至关重要。众多疾病,特别是神经系统疾病和代谢性疾病,均与线粒体功能的异常紧密相关。借助AIE线粒体靶向荧光探针,研究者能够清晰地揭示其微观结构和形态变化,并进一步分析线粒体的形态动力学[2]、膜电位波动[3]等关键特征,做到疾病的早期诊断。除此之外,AIE线粒体靶向荧光探针在药物筛选和治疗监测方面也展现出巨大潜力。通过观察线粒体的状态变化,研究人员可以评估药物对细胞能量代谢和线粒体功能的影响,从而筛选出具有潜在治疗效果的药物。溶酶体作为细胞的“废物处理中心”,负责细胞内废弃物和老化细胞器的分解与消化,利用AIE溶酶体探针可以使其结构在细胞内得以清晰呈现。通过结合不同颜色的AIE荧光染料,研究人员可以同时标记线粒体和溶酶体,并利用荧光显微镜观察它们之间的融合过程[4]。
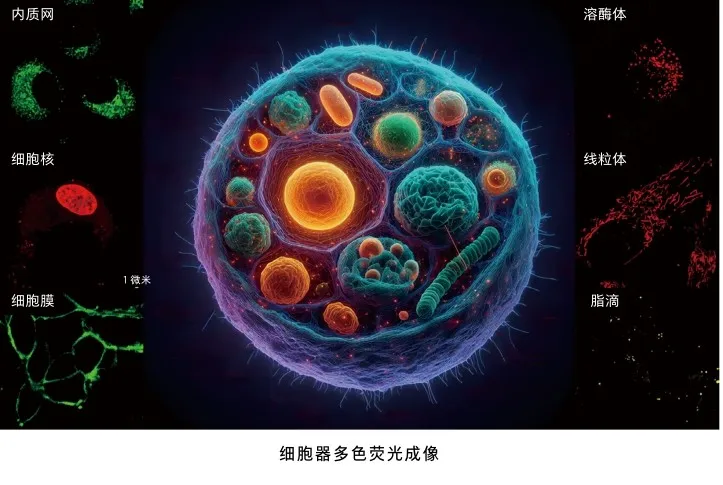
值得注意的是,随着医学的发展进步,细胞器荧光探针的应用已不仅限于人体活细胞的成像,研究人员正不断为其赋予新的用途,使其与传统医学影像技术形成互补,并在疾病的诊断和治疗中发挥不可或缺的作用。例如,有研究表明,核酸染料可以用于血细胞分析用染色液的开发,细胞线粒体荧光探针也可以用于精子线粒体染色。
病原体的“验钞机”——AIE微生物成像探针
微生物遍布于我们的环境,其中许多微生物在人体内形成微生态系统的一部分。在这个微生态系统中,一些微生物可看作是人体的“共生伴侣”,例如正常生理状态下存在的微生物菌群。这些微生物在协助人体消化食物和合成所需营养物质方面发挥着重要作用。然而,也存在一些可被视为“寄生异客”的微生物,如病毒和致病菌,它们在侵袭人体后可能引发多种疾病。为了维护人体健康,必须持续监测微生物的存在和状态,以及时察觉并应对潜在问题。为实现这一目标,需要一种能够高效“审视”微小微生物的高分辨显微技术,而AIE技术就是其中之一。
在临床诊断、药物开发、食品加工和环境科学等多个领域,快速检测细菌具有重要的实用价值。相较于传统的细菌检测和鉴定方法,如标准平板计数法、PCR和高分辨率显微镜,基于荧光的方法提供了一种更为简便的途径,实现了直接的实时细菌检测和鉴定。而实现这种技术的关键在于开发具有高灵敏度和特异性的荧光染料。多项研究表明[6],使用带正电的AIE荧光染料可以轻松实现对细菌的荧光检测。然而,荧光染料上过多的正电荷可能引起细菌状态的严重改变,同时,基于静电吸附的荧光标记会对所有微生物进行染色,无法做到特异性,因此,基于另外一种原理的AIE材料——含有TPE核心的硼酸类化合物(TPE-2BA),被开发出来用于死活细菌的鉴别[7]。另外,除了单种细菌的检测外,多个AIE材料还可以组合到一起形成阵列,一次性对多种细菌进行检测[8]。
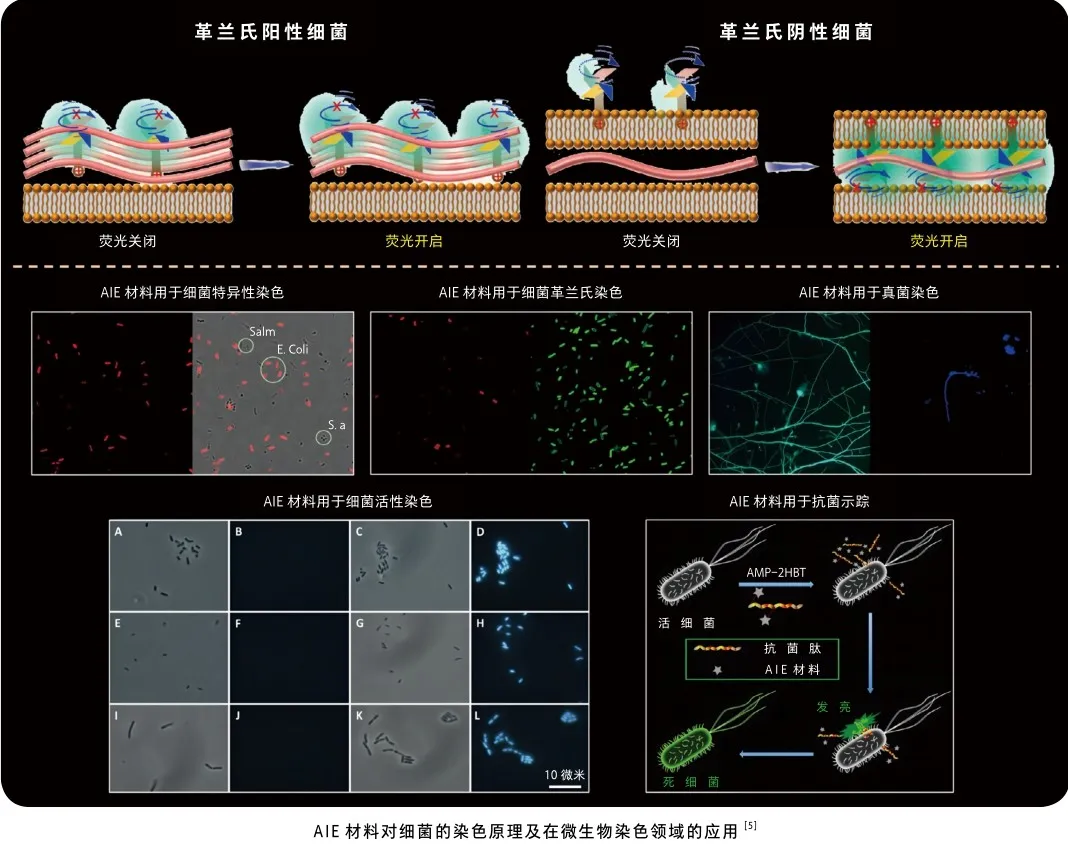
随着人们对个体健康和环境安全越来越关注,AIE材料在辅助医学诊断领域的应用正经历着迅猛的发展。在这一领域,AIE材料大显身手。基于AIE材料研发的革兰氏荧光染色液,能够通过荧光信号的差异迅速区分革兰氏阳性菌和阴性菌。相较于传统的革兰氏染色法的四步法,AIE革兰氏荧光染色液充分利用AIE材料的优势,仅需一步便可获得更为清晰的图像。在此基础上研发的微生物双重荧光染色液,可对包含细胞、细菌、真菌等多种成分的复杂样品进行荧光多色成像,并通过颜色和形态对不同组分进行快速区分。另外,AIE材料还可以与噬菌体进行有机结合,实现对大肠杆菌、结核杆菌、沙门菌、铜绿假单胞菌等的精准识别。
微生物检测和鉴定是多个领域的一个重要课题,涉及人体健康、环境安全、食品质量等方面。不仅仅是检验,随着人们对“多合一”材料需求的提升,AIE材料在微生物领域的应用还有很大的发展空间,如AIE荧光材料也能实现药敏检测、抗菌杀菌等多项功能,还可用于研究微生物的生理和代谢过程,如监测微生物的生长、分化、交流、感染等,从而揭示微生物的机制和规律,为微生物学和生命科学提供新的视角和方法。
肿瘤手术的“GPS”——AIE近红外成像探针
肿瘤的成像在癌症研究和临床实践中具有深远的意义,它贯穿了患者治疗的整个流程。早期,通过对肿瘤细胞和组织的高分辨成像,可以及早发现病变,从而采取更早期、更有效的治疗手段,提高治疗成功率,降低病死率。治疗方案定制期间,通过深入了解肿瘤的类型、分级和分子特征,医生可以制定更为精准的治疗方案,选择最适合患者的治疗药物,减少不必要的治疗副作用。治疗阶段,医生可以通过观察肿瘤的大小、形态和代谢等变化,及时调整治疗方案,确保患者得到最佳的治疗。如果涉及手术治疗,那么肿瘤的成像可用于导航和定位,帮助医生更准确地切除肿瘤组织,最大限度地保留健康组织,降低手术风险。 治疗后,成像还对治疗效果的评估和患者预后起到关键作用,帮助医生为患者规划长期的治疗和随访计划。因此,肿瘤的成像可以说为癌症的研究、诊断和治疗提供了不可或缺的技术手段,而只有荧光成像技术能够做到实时成像,为手术导航和治疗监测提供及时信息。
肿瘤荧光成像的成功依赖于两个核心要素:一是荧光材料能够精确地定位到肿瘤组织;二是这些材料产生的荧光信号足够强烈,可以穿透深层组织。相较于目前广泛应用的近红外一区小分子荧光剂吲哚菁绿(ICG),近红外二区的AIE材料不仅展现出更深的组织穿透能力,其独特的“越聚集越亮”特性更使得AIE材料更适合纳米化,它不仅优化了成像效果,还结合了高渗透长滞留效应(EPR 效应),实现了对肿瘤的精准靶向,此外,研发人员通过灵活调整包裹剂的种类和纳米粒子尺寸,实现了血液滞留时间的调控。
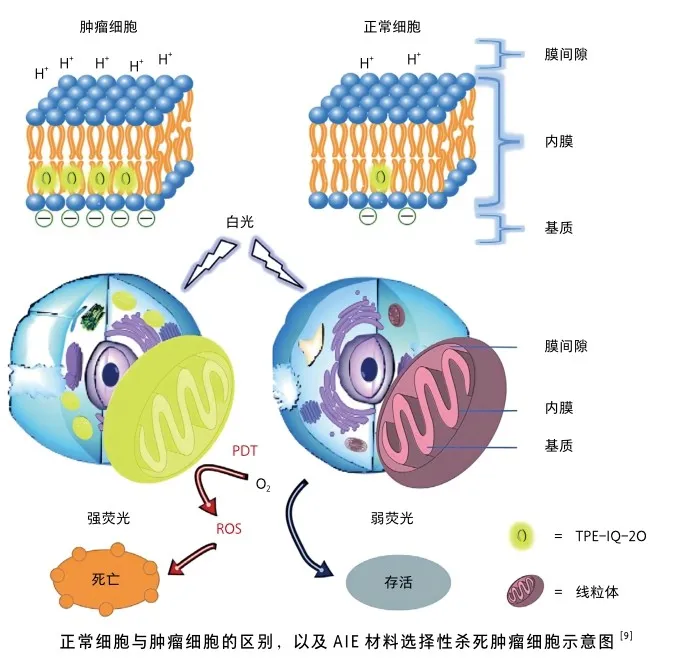
纳米工程的优势不仅体现在纳米制剂的制备上,更在于其多组分特性以及进一步加工后所能获得的额外功能。以膀胱癌研究为例,AIE材料与化疗药物顺铂的结合形成了一种创新的多组分抗癌材料。这种材料不仅能被膀胱癌细胞高效吸收,而且在还原酶的作用下能够释放铂(Ⅱ),从而确保化疗的有效性。此外,结合近红外荧光成像引导的光增强癌症化疗(PECC)技术,可以显著提高膀胱癌对顺铂化疗的敏感性,同时减少副作用[10]。除此之外,通过对纳米制剂进行表面修饰,可以赋予其新的特性。例如对纳米粒子进行蛋白修饰,在利用EPR效应实现肿瘤富集的同时,进一步通过表面蛋白修饰,如添加肿瘤特异性的靶向蛋白,显著提升了纳米粒子的肿瘤靶向性。
AIE近红外成像材料更大的应用价值在术中监测。对于外科医生而言,外科手术往往如同是在黑暗环境中进行的精细修复工作,任何疏忽都可能造成不可逆的损伤,这通常需要主刀医生具备丰富的临床经验。AIE分子探针能够在术中实时标记癌细胞,通过荧光信号的引导,医生能够迅速且清晰地识别出病灶部位与正常组织的界限[11]。这种技术为外科手术提供了“地图”般的指引,显著减少了盲目操作的风险。此外,荧光影像技术还能对手术过程进行实时成像,帮助医生精准判断需要进一步加强处理的区域,从而避免了患者的不必要多次创伤。可以说,AIE近红外成像材料的引入,大幅降低了手术对医生经验的要求,不仅提高了外科手术的精准度和速度,还极大地增强了手术的安全性,为现代医学的发展带来了革命性的进步。
小分子“探测仪”——AIE小分子探针
小分子是指分子量较小的有机或无机化合物,如金属离子、体内的活性分子等。这些小分子在生物体内起着重要的作用,如调节细胞的生长、分化和凋亡,参与代谢和信号传导等。除了影响人体健康外,一些有危害的小分子如爆炸物、剧毒性物质,也对公共安全产生了很大威胁。对这些小分子的常规检测方法——液相和气相色谱法、质谱法,通常需要昂贵的仪器。而最近几十年来,分析化学领域取得了巨大进展,不仅能够使用先进的仪器进行高灵敏度的化学分析,还涌现了许多新型的小分子“探针”以实现低成本的检测。其中,AIE材料形成的聚集态具有高灵敏度和选择性,为便捷的现场检测提供了新的可能性。
AIE材料可以检测的小分子种类繁多[12],针对生物体内的小分子,其检测方式可以分为两种:对血液、尿液等生物样本,可以进行体外检测;基于荧光的非侵入性特点,在细胞、组织、器官甚至整个生物体内进行体内检测,这种原位的小分子检测更具有生物学意义。AIE材料大多数可以进行第二类检测,比如一些炎症探针——H2O2探针,可以在细胞水平上对环境中的过氧化氢进行监测。而针对生物体外的小分子,则可以在溶液或者气体环境中进行检测(上述第一种方式),如检测饮用水中包括重金属在内的污染物等。此外,还可以将AIE材料制成检测纸状的材料用于检测气态的污染物,如腐败食物散发的胺类物质等。
小分子检测是分析化学领域的一个重要课题,涉及生物医学、环境科学、公共安全等多个领域。小分子的检测方法有很多,但是传统的仪器分析方法往往需要高昂的成本、复杂的操作和长时间的等待。为了实现快速、灵敏、简便和低成本的小分子检测,近年来出现了许多基于荧光的小分子探针,其中AIE材料因具有高效的荧光发射、良好的生物相容性和多样的功能化方式,成为一种非常有前景的小分子检测平台。虽然AIE材料在小分子检测方面的应用已经取得了一些重要成果,但是仍然存在一些挑战和问题,例如,提高探针的稳定性和特异性、降低探针的毒性和干扰、扩大探针的检测范围和灵敏度,以及实现探针的可视化和信号放大等。这些问题需要进一步的研究和探索,以期开发出更加高效和智能的AIE材料,为小分子检测提供更多的可能。
未来展望
自2001年唐本忠教授及其研究团队首次揭示AIE材料以来,这类材料凭借其异常的光学特性和广泛的应用前景,在材料科学、生物医学成像、光电子学等多个学科领域引发了浓厚的研究兴趣。传统染料在稀溶液中展现出较强的荧光,却在聚集态时遭遇荧光猝灭,而AIE材料则在聚集形态下展现出显著的荧光增强,这一独特性质极大地增强了其在生物医学成像领域的应用价值。在过去20多年的发展中,AIE材料逐渐被科学研究者所接受,并应用于基础及临床研究,并在细胞器成像、微生物检测及抗菌材料开发、肿瘤细胞检测及消融、小分子检测等领域取得了一系列成果。
未来,AIE材料有望在医学诊断、生物医学研究和环境监测等领域发挥更为重要的作用。AIE材料的独特荧光特性为生物医学领域提供了创新的技术手段,支持精准医疗、疾病早期诊断和治疗,同时在环境监测和生物分析等领域也有广泛应用。然而,要充分发挥AIE的优势,科学家们需要不断探索与优化,包括精准控制AIE探针进入特定的细胞/组织区域,提高材料的生物相容性,设计更多特异性探针以监测更多生物过程,以及克服多靶标成像的技术难题,等等。这些挑战的解决不仅需要材料学科的努力,更是需要与其他学科如生物学、医学、化学、物理科学等的交叉和融合,以实现更高效、更安全的生物医学应用。
[1]Song N, Xiao P, Ma K, et al. Recent advances of AIEgens for targeted imaging of subcellular organelles. Chemical Research in Chinese Universities, 2021, 37: 52-65.
[2]Xu F Z, Zhu L, Han H H, et al. Molecularly engineered AIEgens with enhanced quantum and singlet-oxygen yield for mitochondriatargeted imaging and photodynamic therapy. Chemical Science, 2022, 13(32): 9373-9380.
[3]Zhang L, Liu W, Huang X, et al. Old is new again: A chemical probe for targeting mitochondria and monitoring mitochondrial membrane potential in cells. Analyst, 2015, 140(17): 5849-5854.
[4]Wong Y C, Ysselstein D, Krainc D. Mitochondria–lysosome contacts regulate mitochondrial fission via RAB7 GTP hydrolysis. Nature, 2018, 554(7692): 382-386.
[5]Bai H, He W, Chau J H C, et al. AIEgens for microbial detection and antimicrobial therapy. Biomaterials, 2021, 268: 120598.
[6]Feng X, Tong B, Shi J, et al. Recent progress of aggregation- induced emission luminogens (AIEgens) for bacterial detection and theranostics. Materials Chemistry Frontiers, 2021, 5(3): 1164-1184.
[7]Luo J, Xie Z, Lam J W Y, et al. Aggregation-induced emission of 1-methyl-1, 2, 3, 4, 5-pentaphenylsilole. Chemical Communications, 2001 (18): 1740-1741.
[8]Feng G, Yuan Y, Fang H, et al. A light-up probe with aggregationinduced emission characteristics (AIE) for selective imaging, naked-eye detection and photodynamic killing of Gram-positive bacteria. Chemical Communications, 2015, 51(62): 12490-12493.
[9]Gui C, Zhao E, Kwok R T K, et al. AIE-active theranostic system: selective staining and killing of cancer cells. Chemical Science, 2017, 8(3): 1822-1830.
[10]Ding K, Wang L, Zhu J, et al. Photo-enhanced chemotherapy performance in bladder cancer treatment via albumin coated AIE aggregates. ACS Nano, 2022, 16(5): 7535-7546.
[11]He W, Zhang Z, Luo Y, et al. Recent advances of aggregationinduced emission materials for fluorescence image-guided surgery. Biomaterials, 2022, 288: 121709.
[12]Fang G, Liu D, Zhang M, et al. Single-organelle localizationbased super-resolution imaging for subcellular molecules microdynamics. Coordination Chemistry Reviews, 2024, 504: 215670.
关键词:聚集诱导发光 细胞成像 微生物成像 近红外成像小分子探针 ■
